Lever, februari 2014 (website versie)
-
Upload
nvh-hepatologie -
Category
Documents
-
view
216 -
download
1
description
Transcript of Lever, februari 2014 (website versie)

NIEUWSBLAD VAN DE NEDERLANDSE VERENIGING VOOR HEPATOLOGIE
JAARGANG 38 NR. 1 FEBRUARI 2014
Lever Nieuws 4 Beleidsplan NVMDL 5 In de Schijnwerpers: Karel van Erpecum en
Jan Monkelbaan 6 Hoe gaat het eigenlijk met Meritxell Huch 7 Casus Morbus Wilson 10
Lever Alert: Celdeling van belang voor galkanaalvorming in de lever 11 Lever Ingezonden:
Verslag AASLD 2013 12 Lever De Eerste Keer 13 Lever uit de oude doos: De school
van Schalm 13 Lever Van Eigen Bodem 15 Lever proefschriften 19
Interviewers geïnterviewd

2 LEVER NR 1 FEBRUARI 3
LEVE
R
VO
OR
WO
OR
D
congresagenda
Allereerst wil ik u een heel gezond en succesvol 2014
toewensen. Zoals gebruikelijk in de eerste LEVER
van het jaar geef ik u een kort jaarverslag van 2013.
En om het ‘kort’ te houden is niet eenvoudig, aangezien de
Nederlandse Vereniging voor Hepatologie zeer actief is en
op vele vlakken nog steeds aan het groeien is! Die groei wil ik
illustreren aan de hand van een aantal grafiekjes.
In figuur A is te zien dat de werkadressen van NVH leden goed
verspreid liggen over het hele land, met ‘concentratie hot-
spots’ in Amsterdam, Rotterdam en Groningen. Dit maakt een
gevarieerd ledenbestand waarin zowel de academische centra
als vele perifere ziekenhuizen zijn vertegenwoordigd. Neem
ook bijvoorbeeld het ledenaantal; in de laatste 5 jaar van het
36-jarige bestaan van onze vereniging is het ledenaantal van
400 naar 600 leden gestegen, wat naar mijn mening een goede
illustratie is hoe actief de vereniging is (B). Ondanks de ver-
grijzing van de Nederlandse bevolking, is de NVH allerminst
aan het vergrijzen, want meer dan 50% van de leden (waarvan
we de geboorte datum weten, ongeveer 80%), is jonger dan 40
jaar (C). Het jongste lid is 24 jaar, de oudste 83. We zijn een
multidisciplinaire vereniging, met MDL-artsen, internisten,
infectiologen, kinderartsen, basaal/translationeel onderzoe-
kers, maar ook pathologen, radiologen, chirurgen en veteri-
naire artsen. Om elkaar toch snel te kunnen vinden, bracht de
NVH begin 2013 i.s.m. Medicom Medische Uitgeverij B.V. het
eerste NVH smoelenboek uit, zodat we elkaar heel gemakkelijk
kunnen vinden.
Sponsors van de NVHIn 2013 had de NVH vier hoofdsponsors welke een belang-
rijke ondersteuning voor de NVH hebben geleverd: Gilead,
Janssen-Cilag B.V., MSD en Roche. Daarnaast werden bijdra-
gen ontvangen van Bristol-Myers Squibb, Dr. Falk Farma en
Norgine.
De NVH is alle sponsors zeer erkentelijk voor hun voort-
durende financiële steun, vooral in het huidige financiële
klimaat. Het stelt de NVH in staat om de contributie aantrek-
kelijk te houden, vooral voor artsen in opleiding en jonge on-
derzoekers. Ook kunnen we mede dankzij de sponsoren onze
meetings, zoals de DLW, DLR, DEGH en klinische najaars-
vergadering steeds weer verder laten groeien. En zijn wij in
staat om nieuwe initiatieven te ondersteunen met als doel de
Hepatologie in Nederland te verbeteren en te promoten, zoals
bijvoorbeeld met de oprichting van de werkgroepen HCC en
auto-immuun hepatitis. Komend jaar zullen er twee nieuwe
initiatieven worden uitgedacht, een rondom NASH en een
V A N D E S E C R E T A R I S2 0 1 4
OrganisatOren van cOngressen/sympOsia wOrden verzOcht data tijdig dOOr te geven en zOveel mOgelijk rekening te
hOuden met reeds geplande activiteiten.
Omslagfoto: jan monkelbaan en karel van erpecum, mdl-artsen te utrecht.Overname van gegevens uit deze nieuwsbrief is toegestaan met bronvermelding.correspondentie kan worden gestuurd naar het redactieadres. de redactie behoudt zich het recht voor om te bewerken.Vormgeving: m.art, haarlem. issn nr.: 1574-7867. deze uitgave is mede mogelijk gemaakt door gilead, roche, janssen-cilag B.v. en norgine.
■ 20 - 21 MAART 2014 voorjaarsvergadering nederlandse
vereniging voor gastroenterologie en
hepatologie
Locatie: nh koningshof te veldhoven
Inlichtingen: secretariaat nvge,
postbus 657 - 2003 rr haarlem
tel.: 023 - 551 3016
Fax: 023 - 551 3087
e-mail: [email protected]
■ 09 - 13 APRIL 2014 easl
Locatie: international convention centre
excel, londen
■ 16 APRIL 2014 nvmdl symposium
Locatie: koninklijk instituut voor de tropen
te amsterdam
Inlichtingen: secretariaat nvmdl,
postbus 657 - 2003 rr haarlem
tel.: 023 - 551 3016
Fax: 023 - 551 3087
e-mail: [email protected]
■ 3 - 6 MEI 2014ddw 2014
Locatie: mccormick place, chicago,
illinois
website: www.ddw.org
■ 24 – 27 JUNI 2014 dutch liver week
(echocursus op dinsdag 24 juni)
Locatie: mövenpick hotel te amsterdam
Inlichtingen: secretariaat nvh,
postbus 657 - 2003 rr haarlem
tel.: 023 - 551 3016
Fax: 023 - 551 3087
e-mail: [email protected]
■ 9 - 10 OKTOBER 2014najaarsvergadering nederlandse
vereniging voor gastroenterologie en
hepatologie
Locatie: nh koningshof te veldhoven
Inlichtingen: secretariaat nvge,
postbus 657 - 2003 rr haarlem
tel.: 023 - 551 3016
Fax: 023 - 551 3087
e-mail: [email protected]
■ 18 - 22 OKTOBER 2014ueg week 2014
Locatie: acv vienna, Oostenrijk
website: www.ueg.eu/week
■ 30 – 31 OKTOBER 2014 dutch liver retreat
Locatie: kasteel schortinghuis, spier
Inlichtingen: secretariaat nvh,
postbus 657 - 2003 rr haarlem
tel.: 023 - 551 3016
Fax: 023 - 551 3087
e-mail: [email protected]
■ 7 - 11 NOVEMBER 2014aasld the liver meeting
Locatie: Boston, ma
website: www.aasld.org
nieuwsbrief van de nederlandse vereniging voor hepatologie.verschijnt vier maal per jaar.
de nederlandse vereniging voor hepatologie is opgericht op 30 september 1977.
Redactie:dr. l.c. Baakmw. dr. m.j. coenraaddr. s.c.d. van ijzendoornmw. dr. s.w.c. van milmw. m.j. van gijtenbeek
Redactie adres:redactie nieuwsbrief nvhpostbus 6572003 rr haarlemFax: 023 - 5513087
Bestuur: prof. dr. u.h.w. Beuers, voorzittermw. dr. s.w.c. van mil, secretarisdr. j.t. Brouwer, penningmeesterdr. l.c. Baakdr. m.j. coenraadprof. dr. h.j. metselaar
dr. c.c. paulusmaprof. dr. r.j. portemw. dr. j. verheijdr. s.c.d. van ijzendoorn
Lidmaatschap:aanmeldingen bij de secretaris:dr. s.w.c. van milpostbus 6572003 rr haarlemfax: 023-5513087
COLOFON
Beste leden van de NVH,
Lees verder op pagina 4.

4 LEVER NR 1 FEBRUARI 5
rondom PSC. Naast de sponsoren willen we ook Ulrich Beuers
(voorzitter), maar vooral Hans Brouwer (penningmeester)
hartelijk danken voor hun inzet om sponsoren te interesseren
voor de NVH.
Nieuwsblad Lever en NVH-websiteOnder het bezielende redacteurschap van Sven van
IJzendoorn, Minneke Coenraad, Bert Baak en Marie José
van Gijtenbeek blijft de Lever maar groeien. In Figuur E is te
zien hoe de groei van het blad van 12 pagina’s in 2004 naar
nu soms 28-32 pagina’s nu is gestegen. Dankzij de financiële
steun van onze sponsoren, hebben we vanaf 2009 ook het
maximale aantal pagina’s losgelaten; hoe dik de LEVER wordt,
hangt nu af van de aangeboden kopij. Ook in ons magazine
is nog volop groei te zien, in dit blad starten we ook weer een
nieuwe rubriek (zie pagina 13) over ‘de eerste keer’ in het
leven van een aios, waarin een aios een bijzondere patiënt,
een zeldzame diagnose of een opvallend ziektebeloop vanuit
persoonlijk perspectief beschrijft. De NVH-website is nu in
dezelfde stijl als het nieuwsblad en zal komend jaar nog verder
worden verbeterd.
Proefschrift/congres deelname sponsoringDe NVH sponsort de uitgave van proefschriften en con-
gresdeelnames. Afgelopen jaar zijn 15 proefschriften en vier
reisbeurzen door de NVH met € 500,- gesubsidieerd.
NVH bijeenkomsten Ook dit jaar zijn onze meetings weer succesvol te noemen. De
DEGH (69 ingezonden abstracts, 30 orals, 39 posters), Dutch
Liver Week 2013 (67 deelnemers), klinische najaarsvergade-
ring (35 ingezonden abstracts/18 orals) en de DLR (44 inzen-
dingen, 30 praatjes geselecteerd, 88 deelnemers). Komend
jaar zal de DEGH een iets ander format krijgen om nog beter
een brug te gaan slaan tussen clinici en onderzoekers, met vijf
Vervolg voorwoord.
Discrepantie‘momenteel lijkt er een discrepantie te zijn tussen het aantal
leverpatiënten en het aantal leverspecialisten. dat geldt overigens
ook voor andere deelgebieden als ‘motiliteit’ en ‘voeding’. er gaat
momenteel veel tijd en aandacht naar endoscopie en de colorec-
tale maligniteiten en voorstadia in het kader van het bevolkings-
onderzoek darmkanker. veel ziekenhuizen zijn geïnteresseerd om
de colonscreening binnen te halen omwille van de ‘productie’ c.q.
groei en financiën. tegelijkertijd moet de mdl in nederland de
reguliere taken daarvan niet de dupe laten worden. daar ligt een
spanningsveld, dat besef ik heel goed’.
Beleidsdoel 4De opleiding tot MDL-arts is zodanig vormgegeven,dat het aantal op te leiden MDL-artsen, de structuuren inhoud van de opleiding optimaal aansluiten bijde behoefte en wensen uit de MDL-praktijk
in het conceptbeleidsplan wordt aangestuurd op een brede basis
(‘excelleren in de breedte’), waarbij de mdl in geheel nederland
goed is vertegenwoordigd en daarnaast ook binnen allerlei
aandachtsgebieden. toch is er een breuk met het verleden. ‘de
opleiding tot mdl-arts zal meer ‘behoefte’-gestuurd moeten gaan
worden. de mdl praktijk zal dan moeten bepalen of dit endolumi-
nale mdl zal zijn of wellicht een andere soort. waarschijnlijk moe-
ten we gepland en gericht meer leverspecialisten gaan opleiden
dan nu het geval is’.
‘in het beleidsplan wordt verder gesteld dat de mdl-arts ook de
regisseur moet zijn in multidisciplinaire samenwerking, overleg en
behandeling van patiënten met mdl-ziekten. dit vraagt om een
brede basis maar ook om sterke aanwezigheid van deelgebieden.’
hoe zal dat in de praktijk gaan? ‘Ook paul Fockens heeft tijdens
de jubileumbijeenkomst in veldhoven (najaar 2013) aangegeven
dat endoscopie geen doel op zich moet zijn maar ondersteu
nend aan deelgebieden. dat geeft mijns inziens aan dat er bin-
nen de mdl-wereld voldoende draagvlak aanwezig is om binnen
de opleiding te gaan sturen op ‘behoefte’. en dat betekent ook
dat de aios naast een brede basis nadrukkelijk meer kan gaan
kiezen’.
Beleidsdoel 2De MDL-arts is kernspecialist op het gebied van aandoeningen van het maagdarmkanaal, lever en galwegen en alvleesklier en treedt daarbij op als regisseur in multidisciplinaire samenwerking, over-leg en behandeling van MDL-patiënten.
Kansen voor de hepatologiewat betekent dit voor de hepatologie? en hoe gaat die hepatolo-
gie inhoudelijk eruit zien? ‘ik denk dat er in de mdl basisopleiding
meer aandacht moet zijn voor de hepatologie. de aios moet een
goede training krijgen in de kliniek waarvan de lever een cruciaal
onderdeel is. daarbij hoort een flinke dosis water-zout-huishou-
ding, kennis van infectie ziekten, zaken die onterecht nu vaak als
erg ’internistisch’ worden ervaren. de verhouding met de interne
geneeskunde kan inniger worden. in maastricht werken we voor
de hepatitiszorg nauw samen met de infectiologen en dat bevalt
goed. tegelijkertijd moet de hepatologie misschien wel vaker
gecombineerd worden tot afdeling ‘hpB’ (hepato-pancreatico-
biliaire)- aandoeningen. dat zou dan inclusief ercp kunnen zijn.
we moeten er naar toe dat de hepatologie ook interessant is en
blijft voor mensen die kunnen scopiëren’.
door Bert Baak
‘Translational Science Teaching Sessions’ rondom de thema’s
Barrett’s Esophagus, darmkanker, IBD, Hepatitis C en nog een
lever thema. In deze sessies zal een clinicus en een onderzoeker
een compleet beeld van de ziekte, medicatie, patho(bio/fysio)
logie schetsen, waarna een aantal ingediende abstracts rond
deze thema’s zullen worden gepresenteerd.
NVH prijzen De jaarlijkse Young Hepatologist prijzen gingen naar Ad van
der Meer (Klinisch, Rotterdam) en Veerle Bieghs (Basaal,
Maastricht). Ramadhan Matondo (UU) en Alexandra Milona
(UMCU) wonnen de eerste prijs, bestaande uit twee iPads en €
2500 aan benchfee met de speed date sessie tijdens de DLR.
NVH als sponsor Naast de ondersteuning van werkgroepen, ondersteunt de
NVH ook andere meetings, wanneer het aannemelijk is dat
deze meetings de Hepatologie in Nederland verder bevorde-
ren. Zo heeft de NVH dit jaar steun gegeven aan de organisatie
van de Nuclear Receptor Research Network meeting op 21
november in Utrecht, waar Antonio Moschetta vertelde over
de rol van FXR in de darm in het ontstaan van HCC.
NVH bestuur In 2013 hebben er ook weer bestuurswisselingen plaats
gevonden: Joanna Verheij en Herold Metselaar hebben Klaas
Nico Faber en Ger Koek opgevolgd. Ikzelf heb het secretariaat
van Klaas Nico Faber overgenomen. We willen Klaas Nico en
Ger nogmaals heel hartelijk danken voor hun inzet voor onze
verening. De groei en bloei van de NVH zou onmogelijk zijn
geweest zonder de hulp van Van Gijtenbeek secretariaatszaken
en congresbegeleiding, gevormd door Marja Weber, Jeanine
Gies en natuurlijk Marie José van Gijtenbeek zelf. Ik wil be-
sluiten met hen bedanken voor hun niet aflatende inzet om de
NVH te laten groeien!
Saskia van Mil, secretaris
DLW 2014De Dutch Liver Week 2014 zal plaatsvinden van 24 tot 27 juni in Amsterdam.
De week begint op dinsdag traditiegetrouw met een
1-daagse echocursus. samen met de medizinische
hochschule hannover zullen de beginselen van de abdominale
echografie worden bijgebracht. het programma bestaat uit
een theoretische introductie en oefening op gezonde vrijwilli-
gers; daarna kan het geleerde in de praktijk worden gebracht
op computersimulatoren.
hierna volgen drie dagen klinische hepatologie. dit jaar zullen
weer enkele vlaamse sprekers en voorzitters een bijdrage leveren
aan de cursus. wij hopen met hen wederom Belgische collega’s
te mogen verwelkomen als deelnemers aan de cursus. de dlw
zal een goed overzicht geven over de belangrijkste leveronder-
werpen, op maat gepresenteerd voor mdl-artsen, internisten,
kinderartsen, radiologen etc., al dan niet in opleiding.
deze cursus dient door aios mdl eenmaal verplicht te worden
gevolgd in het vervolgdeel van de opleiding.
Rob de Knegt en Minneke Coenraad
LEVE
R
NIE
UW
S
LEVE
R
NIE
UW
S
excelleren in de breedte. Beleidsplan mdl 2013-2018:
‘hoeveel leverpatiënten zijn er in nederland en hoeveel leverspecialisten? we moeten veel meer aandacht geven aan de hepatologie binnen de mdl. daar liggen kansen’. aan het woord is prof. dr. ad masclee, als hoogleraar mdl werkzaam in het maastricht universitair medisch centrum (mumc) en voorzitter van de nvmdl. hij verwoordt de visie die nvmdl samen met nvge en nvh in het beleidsplan mdl 2013-2018 heeft opgesteld.
nieuwe kansen voor de hepatologie

6 LEVER NR 1 FEBRUARI 7
Hoe het begonIn 2003 gingen er stemmen op om het
blad LEVER maar af te schaffen en te
volstaan met een website. Karel was het
daar als kersvers NVH-bestuurslid niet
mee eens. Hij is toen gestart met het
aantrekken van verschillende gastschrij-
vers, veelal uit het buitenland zoals
Duitsland en zelfs Mexico. Het enthou-
siasme van deze schrijvers gaf de eerste
impuls om door te gaan. Al snel ont-
stond daarna het idee om interviews te
gaan afnemen, een gezamenlijk initiatief
van Karel en zijn buurman in het CMH,
Jan Monkelbaan.
OpbouwDe rolverdeling was snel gemaakt: Karel
en Jan stelden de vragen en Jan schreef
het op. Daarbij stelde Karel vooral vra-
gen over ‘research’; de inbreng van Jan
had te maken met de ‘achtergrondinfor-
matie’ en het ‘persoonlijke aspect’.
Het hele gesprek werd opgenomen,
waarna Jan aan het schrijven ging en
Karel de tekst nog wat aanpaste. Er volg-
den vaak verschillende versies voordat
het goed was.
Er was een vast format: de vragen waren
altijd hetzelfde en het moest in een uur
klaar zijn. Er waren zowel vragen over
het persoonlijke leven en de politieke
voorkeur alsook de wetenschappelijke
en medische carrière. Door de vaste
format wisten beide interviewers waar
het over zou gaan en kon er ‘snel ge-
schakeld’ worden. Hierdoor zat er een
beetje ‘druk’ op. Het gevolg was dat er
vaak iets ‘controversieels’ naar boven
kwam. Zo heeft Harry Jansen nog heel
wat te stellen gehad met Ernst Kuipers,
naar aanleiding van zijn interview in
LEVER. Een interview met Ulrich
Beuers, toen nog werkzaam in Duits-
land, was ook heel bijzonder wanneer
gedacht wordt aan het laatste boek dat
Ulrich op dat moment gelezen had,
‘Nachttrein naar Lissabon’’.
Alle toenmalige MDL-hoogleraren ston-
den op de lijst en kwamen aan de beurt.
Voorwaarde: er moest “face to face”
contact zijn. Anders ging het niet door.
Daan Hommes kon alleen gestrikt
worden voor een ingelast gesprek
voorafgaande aan de casuïstische con-
ferentie (van de NVGE) in Utrecht. Het
interview voelde alsof het op Schiphol
werd afgenomen.
Wat ook indruk maakte was dat zowel
Sander van Deventer als Cock Lamers
binnen enkele weken na hun interview
vertrokken uit respectievelijk het AMC
en het LUMC. Teruglezend komt zo’n
gesprek dan wel in een speciaal licht
te staan. Het interview-duo zocht de
prikkeling; het gesprek moest wel ‘jeu’
hebben.
AfbouwDe samenwerking ging voortreffelijk.
Jan als 100% Fries en Karel als 50%
Fries, dat klopte gewoon. Het afnemen
en maken van de interviews bracht met
zich mee dat Karel en Jan een paar maal
per jaar met zijn tweeën op stap gingen.
Juist tijdens deze activiteit leerden zij
In adult mammals, self-renewal is
required for the maintenance of
tissue homeostasis and for tissue
repair after injury. This process occurs
throughout the entire lifespan of an
organism and depends mainly on small
reservoirs of tissue-specific stem cells.
Rapidly self-renewing tissues, such as
small intestine and stomach, harbor
actively cycling stem cell populations
to maintain tissue homeostasis. In such
highly proliferative tissues, keeping the
fragile equilibrium between prolifera-
tion and differentiation is essential in
order to prevent hyperproliferation and
cancer or loss of stem cells and tissue
degeneration2. Wnt signalling activation
is critical for cell fate specification and
to maintain the self-renewal status of
adult intestinal and stomach stem cells2.
In that regard, during my postdoctoral
stage in Prof Hans Clevers lab, together
with Dr Nick Barker, we identified that
the Wnt target Lgr5 was marking a stem
cell population in the pyloric region of
the stomach. We found that hyperacti-
vation of the Wnt pathway, exclusively
in these gastric stem cells, resulted in
tumour initiation, thus proving that
the cells-of-origin of gastric cancer are
indeed gastric stem cells1.
Having identified that Lgr5 was a stem
cell marker in several proliferative or-
gans (1-2), I became very interested on
understanding the role of stem cells in
adult tissue regeneration. My personal
background, a PhD with Honors on
Pancreatic Cancer and Liver Metastasis,
at the CRG (Centre for Genomic Regu-
lation, Barcelona, Spain) prompted me
to turn my interests into the liver and
pancreas.
In the liver, physiological turnover is
largely achieved via de-novo replication
of its mature cell types, hepatocytes and
cholangiocytes (ductal cells), without
any direct involvement of stem/proge-
nitor populations4. However, following
injury, the liver displays a remarkable
capacity to regenerate. This regeneration
is achieved via two different mecha-
nisms, depending on the type of tissue
injury: (a) fully differentiated hepato-
cytes and ductal cells can re-enter the
cell cycle to rapidly compensate for the
tissue loss OR (b) a progenitor response
is put into action when hepatocyte pro-
liferation is impaired4. I found that in
the liver, upon damage, Wnt signaling
becomes highly upregulated in the areas
of active regeneration. The Wnt target
Lgr5 cannot be detected in physiologi-
cal conditions, however, marks a new
population of stem/progenitor cells
that rapidly restores the lost tissue and
reinstalls homeostasis3. This was the first
evidence that a Wnt-responsive stem
cell contributes to the regeneration of
LEVE
R
BA
SALI
ST
meritxell huch
HOE GAAT HET EIGENLIJK MET...?
Lees verder op pagina 9.
LEVE
R
IN
DE
SCH
IJN
WER
PER
S
van 2003 tot 2009
verzorgden zij de interviews
in lever. karel van erpecum,
mdl-arts in het universitair
medisch centrum utrecht en
jan monkelbaan, mdl-arts
in het universitair medisch
centrum utrecht en tevens
mdl-arts in het naburige
centraal militair hospitaal.
ze zijn de twee hepatologen
van het umc utrecht. een
duo-interview door het duo
paulusma-Baak.
Een interview met Karel van Erpecum en Jan Monkelbaan
dOOr COEN PAULUSMA en BERT BAAK
yesterday once moreelkaar beter kennen: tijdens een van
de reizen bleek bijvoorbeeld dat ze op
dezelfde middelbare school hadden
gezeten en daarmee ook gezamenlijke
kennissen uit die tijd hadden. Overi-
gens is Friesland de laatste jaren goed
vertegenwoordigd geweest binnen het
NVH-bestuur: ook Klaas-Nico Faber
is van oorsprong uit “Snits” afkomstig.
Volgens Jan kan hij zo goed als MDL-
arts in het CMH werken juist van-
wege de goede samenwerking met zijn
MDL-collegae in het UMCU. Maar hoe
bevredigend ook, de interviews waren
wel energievretend. Toen Karel in 2009
na zijn termijn uit het NVH-bestuur
ging was het tijd om het stokje door te
geven aan een ander duo.
Boodschap voor de LEVER lezerDesgevraagd heeft het duo nog wat
adviezen en boodschappen. Het zou
een idee zijn om de lezers van LEVER
middels een enquête eens te vragen of
ze het concept van het blad nog leuk
genoeg vinden. Misschien moet de
insteek weer wat meer internationaal
worden. Karel is blij dat de laatste 12
jaar zo goed zijn gegaan voor de NVH.
Financieel is het uitstekend gelopen. Er
is verder wat meer evenwicht tussen de
basalisten en de clinici. De kunst zal zijn
om deze winst blijvend te maken. Bij Jan
leeft de wens om de hepatologie binnen
de MDL-opleiding sterker te maken en
meer aandacht te geven. Hij vraagt zich
daarbij af of de uitgebreide hepatologie-
stage altijd gekoppeld moet zijn aan een
transplantatiecentrum.
Na een rondleiding over de prachtig
verbouwde endoscopieafdeling kon het
duo Paulusma-Baak het UMCU achter
zich laten. Het “face to face” contact had
niet veel langer dan een uur geduurd.
utrechtse kerstballen

9
TWICE-DAILY DOSINGMORE SIMPLICITY*1, MORE CONVENIENCE*1
* Compared to INCIVO dosing every 8 hours.1. INCIVO SPC * see INCIVO SPC for important information on safety, possible interactions and pharmacodynamic characteristics.
INCIVO, 6 tablets a day, can now also be dosed in 2 intakes of 3 tablets each, instead of 3 intakes
of 2 tablets. See SmPC for more information.1 ©Ja
nsse
n-Ci
lag
B.V.
– P
HNL/
INC/
1013
/000
5The ONLY AVAILABLE PROTEASE INHIBITOR to offer a morning and evening dose for your chronic hepatitis C genotype 1 patients1
MorningDose
EveningDose
MorningDose
EveningDose
NEW
Janssen-Cilag B.V.
JAN 0860 adv_A4_NED_DEF 01.indd 1 30/10/13 09:30
the liver tissue upon damage3.
Despite the enormous replication po-
tential of the liver, functional hepatocy-
tes can be maintained only for very few
days in culture, thus precluding their
application for cell therapy treatments.
To obtain a source of functional hepato-
cytes, a variety of in vitro systems have
been described, ranging from culturing
fetal and neonatal liver progenitors to
obtaining hepatocytes by directed dif-
ferentiation of either Embryonic Stem
cells (ES) or induced Pluripotent Stem
Cells (iPS). Liver stem cells have the
potential to self-renew and differentiate
into the functional hepatic lineages4.
However, it was proven difficult to
expand these cells beyond a few days
in culture4. The knowledge acquired
from the in vivo regeneration studies,
allowed me to establish a new culture
system that maintains the self-renewal
status of liver stem cells in vitro. That
is, these stem cells expand unlimitedly
in culture, into long-lived 3D structures
that we have called organoids3. Liver
Primary organoid cultures expand in
the absence of a mesenchymal niche (>1
year in expansion in culture) even from
adult liver single cells. Importantly,
isolated adult hepatic cells retain their
differentiation potential over time when
cultured into organoids3. The cultured
cells express ductal markers and, when
subjected to a differentiation protocol,
~33-50% of the cells differentiate into
functional hepatocytes in vitro. The
huge expansion and differentiation
capacity of the liver organoid cultures
facilitated the engraftment and repo-
pulation of the livers of mice with in-
herited metabolic disease (Tyrosinemia
type I) and partially restored its hepatic
function3.
In the pancreas, I have also described
similar damage-induced activation of
stem cells5. Also in the pancreas, Wnt
becomes highly upregulated upon da-
mage, and ductal progenitors establish
pancreas organoid cultures that expand
unlimitedly in vitro, while maintain the
characteristics of the tissue-of-origin.
Importantly, expanded ductal cultures
retain their potential to differenti-
ate into insulin+ cells in vivo when
transplanted into the kidney capsule,
an achievement never accomplished
before5.
The finding that Wnt-responsive proge-
nitor cells become activated exclusively
upon damage, while cannot be detected
in the normal tissue, led me to continue
my future research on understanding
Personal details:
Name: meritxell huch
Nationality: spanish
Birth: 15th january 1978
Education:group leader
02/2014-present: group leader
wellcome-trust gurdon institute, university
of cambridge
Postdoctoral research
09/2008-02/2014: postdoctoral fellow
(marie curie Fellow).
hubrecht institute. utrecht, the nether-
lands.
Advisor: professor hans clevers
07/2007-09/2008: postdoctoral fellow.
centre for genomic regulation-crg- Barce-
lona, spain.
Advisor: dr cristina Fillat
Doctoral research
01/2002–07/2007: phd (spanish ministry
of health Fellow),
centre for genomic regulation-crg-,
Barcelona, spain.
Advisor: dr cristina Fillat
Qualification: excellent cum-laude
09/2003 master of advanced studies
(dea) university of Barcelona-uB
Undergraduate
09/1996–07/2001: Bsc in pharmaceuti-
cal science, university of Barcelona (uB)
Qualification: excellent First-class honors
Publications:
1: Barker n*, huch m*, kujala p, van de
wetering m, snippert hj, van es jh,
sato t, stange de, Begthel h, van den
Born m, danenberg e, van den Brink
s, korving j, abo a, peters pj, wright
n, poulsom r, clevers h. lgr5(+ve)
stem cells drive self-renewal in the
stomach and build long-lived gastric
units in vitro. cell stem cell (2010) jan
8;6(1):25-36.
2: vries rg*, huch m*, clevers h. stem
cells and cancer of the stomach and
intestine. molecular Oncology (2010)
Oct;4(5):373-84. (review).
3: huch m, dorrell c, Boj sF, van es jh,
li vsw, van de wetering m, sato t,
hamer k, sasaki n, Finegold mj, haft
a, vries r, grompe m, clevers h. in
vitro expansion of single lgr5+ liver
stem cells induced by wnt-driven rege-
neration. nature (2013) Feb 14;494:
247-50.
4: huch m, Boj sF, clevers h. lgr5+ liver
stem cells, hepatic organoids and
regenerative medicine. regenerative
medicine (2013) jul 8 (4):1-3
5: huch m*, Bonfanti p*, Boj sF*,
sato t*, loomans cj, van de wetering
m, sojoodi m, li vs, schuijers j, gra-
canin a, ringnalda F, Begthel h, hamer
k, mulder j, van es jh, de koning
e, vries rg, heimberg h, clevers h.
unlimited in vitro expansion of adult
bi-potent pancreas progenitors through
the lgr5/r-spondin axis. emBO j.
(2013) Oct 16;32(20):2708-21.
*equal contribution
the molecular mechanisms implicated
in tissue regeneration. Since February
2014, I have been appointed a Group
Leader position at the Wellcome-
Trust-Gurdon Institute (University of
Cambridge) where I will pursue my
independent research career trying to
understand the mechanisms behind
liver regeneration and their implications
in liver disease and liver cancer.
Vervolg van pagina 7.

10 LEVER NR 1 FEBRUARI 11
Drie maanden na deze
episode presenteerde de
patiënt zich opnieuw met
een zelfde klinisch beeld. Ditmaal
waren er echter ook leverbiochemie
afwijkingen en een trombopenie.
Aanvullend onderzoek toonde tevens
een verhoogde koperuitscheiding in
de 24-uurs urine. Met de verdenking M. Wilson werd patiënt
verwezen naar ons centrum voor verdere analyse.
Bij presentatie zagen wij een licht icterische jonge man. Hij
was helder en adequaat. Bij lichamelijk onderzoek had hij een
spoor ascites en perifeer oedeem. Laboratorium onderzoek
toonde de volgende bevindingen (referentiewaarden tussen
haakjes) €-glutamyltransferase (€GT) 142 U/L (<55 U/L),
alkalische fosfatase (AF) 75 U/L (<115 U/L), totaal bilirubine
51 µmol/L (<17 µmol/L), geconjugeerd bilirubine 29 µmol/L
(<5 µmol/L), aspartaat aminotransferase (ASAT) 87 U/L (<35
U/L), alanine aminotransferase (ALAT) 168 U/L (<45 U/L),
hemoglobine 5.6 mmol/L (8.5-11.0 mmol/L), haptoglobine <
0.1 g/L ( 0.3-2.0 g/L), trombocyten 50x109/L (150-400x109/L),
ureum 7.1 mmol/L (2.5-7.5 mmol/L), lactaatdehydrogenase
(LDH) 270 U/L (<248 U/L), albumine 25 g/L (34-48 g/L),
protrombinetijd (PT) 30.3 seconden (12.9-14.5 sec). Directe
Coombstest was negatief. De ceruloplasmine-concentratie
was normaal met 0.19 g/L ( 0.15-0.30 g/L). Koperuitscheiding
in 24-uurs urine bedroeg 53.3 µmol/24 uur (0.2-1.7 µmol/24
uur).
Er was derhalve sprake van leverfunctiestoornissen, een
Coombs-negatieve hemolytische anaemie en een sterk ver-
hoogde koperuitscheiding in de urine. Op een CT abdomen
was er hepatosplenomegalie te zien met een beeld passend
bij levercirrose. Aanvullend laboratoriumonderzoek naar
immunologische oorzaken en virale hepatitis leverden geen
afwijkende bevindingen op. De oogarts werd gevraagd om
te beoordelen of er Kayser-Fleischer ringen te zien waren. De
aanwezigheid hiervan is pathognomonisch voor de ziekte van
Wilson, maar het komt slechts bij 44-62% van de patiënten
voor. Bij deze patiënt waren er geen Kayser-Fleischer ringen
zichtbaar.
Om uitsluitsel te krijgen over de diagnose werd een leverbi-
opsie gedaan voor kwantitatieve koperbepaling. Het biopt liet
chronische actieve portale, septerende en lobulaire ontsteking
zien met enige septerende fibrose. Tevens cholestase en koper-
deposities, passend bij M. Wilson. Daarbij was de kwantitatie-
ve koperbepaling sterk verhoogd met 244 µg/g drooggewicht
(referentiewaarde 10-35 µg/g).
Op basis van de uitslag van het biopt werd de definitieve diag-
nose M. Wilson gesteld.
De behandeling van M. Wilson bestaat uit twee stappen, te
weten het verwijderen van geaccumuleerd koper uit de weef-
sels en het voorkomen van hernieuwde koperaccumulatie. De
eerste stap vindt plaats met behulp van zogenaamde chelato-
ren. Daarna vind het onderhoudstherapie plaats in de vorm
van zinkzouten, die interfereren met de intestinale koperab-
sorptie.
Bij deze patiënt werd gestart met penicillamine. Wegens leu-
kopenie werd dit vervangen door trientine. Omdat er sprake
was van progressief leverfalen en ernstige hemolyse onderging
de patiënt meerdere malen plasmaferese om op die wijze snelle
‘ontkopering’ te bereiken. Tevens werd hij gescreend voor
levertransplantatie en op de wachtlijst geplaatst. Ondanks de
medicamenteuze therapie, verbeterde de leverfunctie niet. Vier
maanden na presentatie onderging hij succesvol een lever-
transplantatie. Bij genetisch onderzoek werd er een homozy-
gote mutatie gevonden in het ATP7B gen (c.3207C>A).
M. Wilson is een zeldzame aandoening met een geschatte
prevalentie van 1:30.000. De ziekte wordt veroorzaakt door
mutaties in het ATP7B-gen en erft autosomaal recessief
over. De ziekte presenteert zich meestal tussen het 5e en 35e
levensjaar. Gezien de wisselende presentatie, variërend van
milde leverbiochemie afwijkingen tot acuut leverfalen kan de
diagnose soms lastig te stellen zijn. Onze patiënt presenteerde
zich met ernstige leverfunctiestoornissen en een Coombs
negatieve hemolyse. De hemolyse wordt veroorzaakt door de
aanwezigheid van excessief koper in de circulatie, hetgeen leidt
tot accumulatie van koper in erythrocyten.
Indien de ziekte van Wilson vroeg wordt ontdekt, hebben
patiënten, mits adequaat behandeld, een normale levensver-
wachting. Ook bij patiënten die een levertransplantatie nodig
hebben is de overleving na transplantatie goed.
Drs. N.C. Siegersma, aios MDL
Afd. Maag-, Darm- en Leverziekten van het Leids Universitair
Medisch Centrum
Referenties: 1. jhang js, schilsky ml, lefkowitch jh, schwartz j. thera-
peutic plasmapheresis as a bridge to liver transplantation in
fulminant wilson disease. j clin apher. 2007 Feb;22(1):10-4.
2. roberts ea, schilsky ml, american association for study of
liver diseases (aasld). diagnosis and treatment of wilson
disease: an update. hepatology 2008; 47:2089.
3. european association for study of liver. easl clinical prac-
tice guidelines: wilson’s disease. j hepatol 2012; 56:671.
de lever heeft een complex stelsel van galkanaaltjes dat de veilige afvoer van gal uit de levermassa waarborgt. alle hepatocyten dragen bij aan de vorming van het galkanaal stelsel. dit proces begint vroeg tijdens de embryonale ontwikkeling en gaat door na de geboorte.
Wanneer twee hepatocyten contact met elkaar
maken genereert dit een asymmetrie in beide
cellen. Deze asymmetrie is de voorbode voor de
vorming van een kleine holte tussen de buurcellen; het voor-
stadium van het galkanaal. De apicale plasmamembraan die
in contact staat met deze holte tussen cellen wordt voorzien
van eiwitten en vetten die een rol spelen in de vorming van
gal. Eiwitten en vetten die bestemd zijn voor de uitwisseling
van moleculen tussen de hepatocyte en het bloed worden van
deze apicale domein uitgesloten en bemannen de comple-
mentaire basolaterale plasmamembraan. Gespecialiseerde
adhesieve structuren vormen rondom de holtes en trekken de
plasma membranen van de buurcellen zo dicht tegen elkaar
aan dat gal en bloed niet met elkaar in contact kunnen komen
(Figuur 1A).
Tot zover is er in essentie weinig verschil met de vorming van
apicale holtes in andere embryonale organen. Echter, waar in
casusLE
VER
C
ASU
S
morbus wilson
alert
lEVE
R
ALE
RT
Figuur 1.
a. Oriëntatie van celdeling in hepatocyten.
B. Oriëntatie van celdeling in darm- en niere-
pitheelcellen. de oriëntatie van celdeling
in hepatocyten voorkomt de vorming van
cystes. in plaats daarvan promoot het
de verspreiding van apicale holtes in de
prolifererende levermassa, en daarmee,
zoals verondersteld, de vorming van van
een galkanaalnetwerk.
celdeling van belang voor galkanaalvorming in de lever
Lees verder op pagina 12.
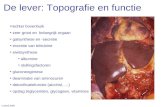
coupe van de lever, 5x vergroot met cu kleuring waardoor de koper-
deposities in het cytoplasma van de hepatocyten duidelijk zichtbaar
zijn.
een 32-jarige nederlandse man presenteerde zich in een ziekenhuis wegens algehele malaise, icterus en buikpijn. aanvullend onderzoek toonde nierinsufficiëntie en hemolyse waarbij in eerste instantie de diagnose ttp (trombotische trombocytopenische purpura) werd gesteld waarvoor hij werd behandeld met hoge dosis prednison en plasmaferese met goed resultaat.

12 LEVER NR 1 FEBRUARI 13
DE EERSTE KEER
bijvoorbeeld de darm en de nier deze kleine primordiale holtes
tussen twee cellen uitgroeien tot apicale cystes en vervolgens
tot grote buisachtige structuren (Figuur 1B), groeien deze in
de lever uit tot een fijnmazig netwerk van galkanaaltjes dat
zich snel in de zich ontwikkelende levermassa verspreidt (Fi-
guur 1A). De moleculaire mechanismen die een rol spelen in
deze belangrijke beslissing waren tot zeer recent onbekend.
Uit twee studies waarvan de resultaten onlangs zijn gepu-
bliceerd in twee artikelen in “PLoS Biology” (1) en “Journal
of Cell Biology” (2) blijkt nu een centrale rol voor het eiwit
Par1b. Uit de onderzoeken blijkt dat Par1b via het reguleren
van de extracellulaire matrix de oriëntatie van celdeling be-
paalt ten opzichte van de eerst gevormde apicale holte. Par1b
zorgt er in hepatocyten voor dat na de celdeling slechts één
dochtercel de apicale holte erft. De andere dochtercel vormt
een nieuwe holte met een andere buurcel. Door deze oriëntatie
van celdeling wordt voorkomen dat hepatocyten een apicale
cyste of grote buisstructuur vormen (Figuur 1B). In plaats
daarvan wordt in de groeiende massa hepatocyten een grote
hoeveelheid apicale holtes verspreid die door met elkaar te
fuseren samen de basis leggen voor een vertakkend galkanaal
netwerk (Figuur 1A).
Te weinig expressie van Par1b in hepatocyten leidt tot de vor-
ming van apicale cystes, en omgekeerd leidt teveel expressie
van Par1b in nierepitheel cellen tot een hepatocyte fenotype.
De studies tonen een onverwachte koppeling van proliferatie,
polariteit, en extracellulaire matrix in hepatocyten die afwijkt
van andere epitheliale celtypen. De bevindingen zijn van
belang voor het begrijpen van de functionele weefsel architec-
tuur in de lever en pathologische afwijkingen hierin. Inzicht
in de moleculaire aansturing van het galkanaalnetwerk is van
belang voor het genereren van functioneel leverweefsel buiten
het lichaam.
Dr. S.C.D. van IJzendoorn, Universitair Medisch Centrum
Groningen
Literatuur1. slim cl, lázaro-diéguez F, Bijlard m, toussaint mj, de Bruin a, du
Q, müsch a, van ijzendoorn sc. par1b induces asymmetric inheri-
tance of plasma membrane domains via lgn-dependent mitotic
spindle Orientation in proliferating hepatocytes. plos Biol. 2013
dec;11(12):e1001739.
2. lázaro-diéguez F, cohen d, Fernandez d, hodgson l, van ijzen-
doorn sc, müsch a. par1b links lumen polarity with lgn-numa
positioning for distinct epithelial cell division phenotypes. j cell
Biol. 2013 Oct 28;203(2):251-64.
Begin november 2013 bezocht
ik het AASLD congres in
Washington DC, VS. Op dit
congres presenteerde ik een poster
over mijn onderzoek genaamd ’Coffee
protects in liver disease: in vivo and in
vitro results’. Er was veel belangstel-
ling voor mijn poster, en er waren een
aantal kritische vragen en suggesties die
behulpzaam zijn bij onze plannen voor
vervolgonderzoek in deze studie. Om
mijn eigen onderzoek te presenteren
en kritische vragen te beantwoorden
op een groot internationaal congres
was erg leerzaam, naast het feit dat
het nieuwe inzichten en invalshoeken
opleverde.
Naast het presenteren van mijn eigen
poster, waren er vele interessante
voordrachten die direct of indirect ook
voor mijn eigen onderzoek relevant zijn
of waardoor nieuwe inzichten of ideeën
ontstaan. De early morning sessies
waren hier een goed voorbeeld van, in
een informele omgeving wordt hier de
laatste literatuur besproken of de laatste
ontwikkelingen worden besproken met
Deze rubriek wordt geschreven door
aios; gegrepen uit de dagelijkse hepato-
logie praktijk, een bijzondere patiënt,
een zeldzame diagnose of een opvallend
ziektebeloop.
Mijn eerste hepatologie dienst, ik wil het
ziekenhuis verlaten, fiets van het slot.
Dan word ik gebeld door mijn supervi-
sor: “Er is een leveraanbod”. Ik ga weer
naar binnen en zoek de patiëntgegevens
op. Ik bel patiënt: “Goedenavond, met
dr. Kuiper, Erasmus MC. Ik heb goed
nieuws. Er is een lever voor u. U mag nu
naar het ziekenhuis komen”. “Spreek ik
echt met de dokter? Is dit een grap? Echt
waar? Dus ik moet nu naar het zieken-
huis komen? Maar ik ben Sushi-all-you-
can eat aan het eten, ik ben niet nuchter,
ik heb geen vervoer, o jawel, vervoer zit
hier aan tafel, ik kom eraan”. “Prima, u
mag zich melden op de SEH”. Ander-
half uur later zie ik de 24-jarige patiënt
met PSC, samen met zijn moeder op de
SEH. Patiënt stuitert; is dolblij, maar
tegelijk heel nerveus, moeder is in tra-
nen. “Komt het goed dokter?” Ik knik.
Patiënt, moeder en ik weten dat hem
een zware operatie te wachten staat, met
risico op complicaties en levenslang
patiënt zijn, maar het is zijn enige kans.
Hij is in een relatief goede conditie, dat
is gunstig.
De chirurg neemt het van mij over, ik
ga naar huis, stap op de fiets. De donor
is net zo jong als mijn patiënt; omgeko-
men bij een fietsongeluk. Ik sta er liever
niet te lang bij stil, doe bewust mijn
lampjes aan en wacht op groen licht.
Edith Kuiper, aios MDL
Erasmus MC, Rotterdam
Voor de volgende uitgave geef ik “de
pen” door aan Wilmar de Graaf.
In de rubriek ‘Lever uit de oude doos’
blikken we terug in de tijd en laten
bijzondere personen, gebeurtenissen
en ontwikkelingen uit de hepatologi-
sche wereld de revue passeren. Dit kan
zowel op nationaal en internationaal
niveau zijn. Dit keer de opleiding he-
patologie in het Dijkzigt onder leiding
van Prof. dr. Solko Schalm.
BERT BAAK, LEVERZIEKTEN! Zo heb
ik in 1997 maandenlang mijn pieper
in het Dijkzigt ziekenhuis beantwoord.
Ik wilde duidelijk maken dat ik geen
interne meer deed en ook geen gas-
troenterologie. Hoe was ik als Hagenaar,
Leienaar en Utrechter eigenlijk in Rot-
terdam verzeild geraakt?
Het had alles te maken met een korte
advertentie vanuit de groep hepato-
logen rondom Prof. Solko Schalm in
1996. Nog voordat er zoiets als een
‘etalageproject’ bestond had een aantal
visionairen besloten de leverkliniek
open te zetten voor geïnteresseerden.
Voor een buitenstaander als ik, net klaar
met de opleiding Interne Geneeskunde
in Utrecht, was het een prachtige kans
om een tijdje te werken in één van de
grootste levertransplantatiecentra in
Nederland.
De stagebeschrijving was kort en helder.
Vier tot zes maanden op zaal, 4 midden
oost. Daar lagen de meeste leverpatiën-
ten, aangevuld met wat algemene gas-
troenterologie. Supervisie was in handen
van een aantal internisten en MDL-
artsen met een leverprofiel. Op 4 mid-
den west lagen alleen gastroenterologie
patiënten, gesuperviseerd door de MD
(zonder L). Van een kruisbestuiving en
oost-west verkeer was nauwelijks sprake,
hoewel de samenwerking op persoonlijk
vlak vaak prima was.
De volgende vier tot zes maanden
werden doorgebracht op de transplan-
tatieafdeling inclusief IC. Verder waren
er spoedpoli’s , klinische consulten en
mogelijkheden tot het verrichten van
(laparoscopische) leverbiopten. Voor
huisvesting kon worden gezorgd. Er wa-
ren geen onregelmatigheidsdiensten, tot
verbijstering van de aios interne. Hier
was blijkbaar eenzijdig een statement
gemaakt waar de rest van de organisatie
niets van wist. Zo kon het dus ook. Een
leermoment voor mij, zelf afkomstig uit
een overlegcultuur.
Het zijn voor mij zeer waardevolle
maanden geweest die mij een onuitwis-
bare ‘leverkleur’ hebben gegeven. Na mij
kwam Adriaan Tan en daarna nog vele
anderen. Op de kaart van Nederland
staan inmiddels heel wat leverkleurige
vlaggetjes geplant, met daarop in kleine
letters ‘been to Rotterdam’.
De stageperiode staat sinds 2010 in de
opleidingsetalage van het EMC. Ik zeg:
niets meer aan doen.
Door Bert Baak
Vervolg van pagina 11.
LEVE
R
IN
GEZ
ON
DEN aasld 2013 in washington dc
een link naar abstracts die op AASLD
2013 werden gepresenteerd.
Tot slot spraken mij de vele mogelijk-
heden tot interactie tussen basaal en
klinisch onderzoek erg aan. Als MD/
PhD student houd ik me bezig met
basaal onderzoek, met een interesse
voor wat zich in de kliniek afspeelt. Op
dit congres was er veel ruimte om deze
interactie mee te maken en hierdoor
onverwachte, maar interessante links te
ontdekken.
Kortom, een erg leerzame en inspire-
rende ervaring die iedere PhD student
mee zou moeten maken.
M.H. Tiebosch, MD/PhD student
Universitair Medisch Centrum
Groningen
lEVE
R
UIT
DE
OU
DE
DO
OS de school van schalm
de rotterdamse school

15
NIE
UW
Robuuste bescherming tegenrecidiverende episodes vanhepatische encefalopathie 1
* In de hoofdstudie 1 werd gelijktijdig lactulose gebruikt door 91% van de patiënten. Zie elders in deze uitgave voor referenties en verkorte SPC.
Dagelijkse behandeling met XIFAXAN® 550 geeft in vergelijking met de huidige standaardtherapie* de volgende significante voordelen:
58% relatieve risicoreductie op doorbraakepisodes van HE (p<0,001) 1
50% relatieve risicoreductie op ziekenhuisopnames door HE (p=0,01) 1
verbetert de gezondheidsgerelateerde kwaliteit van leven bij patiënten met recidiverende HE (P=0,0093) 2
Product onder licentie van Alfa Wassermann S.p.A.XIFAXAN is een handelsmerk van de Alfa Wassermann groep dat in licentie gegeven is aan de Norgine groep.
Rationale of personalized immunosuppressive medication
for hepatocellular carcinoma patients after liver
transplantation
Chen K, Man K, Metselaar HJ, Janssen HL, Peppelenbosch MP,
Pan Q.
Liver Transpl. 2013 Dec 10. doi: 10.1002/lt.23806. PMID:
24376158.
Liver transplantation is a potentially curative treatment for he-
patocellular carcinoma (HCC). Immunosuppressants that are
universally used after transplantation to prevent graft rejection
could potentially have significant impact on HCC recurrence.
This article aims to provide a comprehensive overview of the
potential effects as well as mechanism-of-action of different
types of immunosuppressants on HCC recurrence. We further
propose a concept as well as approaches to develop persona-
lized immunosuppressive medication for either immunosup-
pression maintenance or during prevention/treatment of HCC
recurrence.
Inhibitory receptor molecules in chronic hepatitis B and C
infections: novel targets for immunotherapy?
Mohamad S. Hakim, Michelle Spaan, Harry L. A. Janssen en
Andre Boonstra.
Reviews in Medical Virology. 2013 Dec 19 Doi: 10.1002/
rmv.1779.
Voor effectieve klaring van hepatitis B en C zijn virus-specifie-
ke T cellen nodig. Deze T cellen zijn echter zwak of zelfs afwe-
zig in chronische hepatitis B en C. In vitro en in vivo studies
hebben aangetoond dat de verzwakte T cellen kunnen worden
gestimuleerd door het blokkeren van inhiberende T-cel
specifieke receptoren, waardoor de virus-specifieke antivirale
immuun respons versterkt wordt. Antilichamen gericht tegen
deze receptoren worden momenteel getest in klinische trials
voor HCV patiënten. In dit review bespreken we de veelbelo-
vende strategie van het blokkeren van deze receptoren als een
immunomodulerende therapie voor genezing van chronische
hepatitis B en C.
Obeticholic acid, a farnesoid-X receptor agonist, improves
portal hypertension by two distinct pathways in cirrhotic
rats.
Verbeke L, Farre R, Trebicka J, Komuta M, Roskams T, Klein S,
Vander Elst I, Windmolders P, Vanuytsel T, Nevens F,
Laleman W.
Hepatology 2013 Nov 20. doi:10.1002/hep.26939.
The farnesoid X receptor (FXR) is a nuclear transcription
factor involved in enterohepatic bile and lipid metabolism.
We studied the effect of short-term treatment with obeticholic
acid (INT-747), a potent selective FXR agonist, on intrahepa-
tic hemodynamic dysfunction in both a toxic and biliary rat
model of cirrhosis. In both models, we have demonstrated
FXR-pathway deficiency and we have shown that INT-747
reduces portal hypertension by decreasing intrahepatic vascu-
lar resistance. This is related to a selective increase in eNOS-
activity in the hepatic endothelium. Interestingly, in toxic
cirrhosis this related to down-regulation of Rho-kinase and in
biliary cirrhosis to up-regulation of DDAH-2.
Maternal western diet primes non-alcoholic fatty liver
disease in adult mouse offspring
Pruis MG, Lendvai A, Bloks VW, Zwier MV, Baller JF, de Bruin
A, Groen AK, Plösch T.
Acta Physiol (Oxf). 2014 Jan;210(1):215-27. doi: 10.1111/
apha.12197.
AIM: Metabolic programming via components of the mater-
nal diet during gestation may play a role in the development
of different aspects of the metabolic syndrome. Using a mouse
model, we aimed to characterize the role of maternal western-
type diet in the development of non-alcoholic fatty liver
disease (NAFLD) in the offspring. METHODS: Female mice
were fed either a western (W) or low-fat control (L) semisyn-
thetic diet before and during gestation and lactation. At we-
aning, male offspring were assigned either the W or the L diet,
van eigen bodem
LEVE
R
VA
N E
IGEN
BO
DEM
in deze rubriek vindt u de samenvattingen van artikelen die recent door nvh leden zijn gepubliceerd en subsidies en prijzen die aan
nvh leden zijn toegekend.
voor de artikelen geldt dat 1) de eerste dan wel laatste auteur lid is van de nederlandse vereniging voor hepatologie, 2) er een duide-
lijke link is met een hepatologisch onderwerp, en 3) de impact factor van het journal ≥ 4. samenvattingen zijn maximaal 100 woorden.
uit alle inzendingen in deze rubriek worden komende maand weer de basale en klinische nvh young hepatologist verkozen, die dan
tijdens de voorjaarsvergadering op 20 en 21 maart in het zonnetje worden gezet en de prijs, een certificaat met daaraan verbonden
een geldbedrag van € 1.000, - in ontvangst zullen nemen
Sven van IJzendoorn
Lees verder op pagina 17.

17 65
-201
3-N
L
Ursofalk® 500 mg Tablet bij Primaire Biliare Cirrose Het resultaat van steeds beter willen worden
Productinformatie zie elders in dit blad
Elke dag opnieuw zoeken we naar nog betere oplos-singen in de strijd tegen darm- en leverziekten. In de wetenschap dat zelfs de kleinste stap vooruit al een wereld van verschil kan maken. Vanaf heden zijn er nu ook Ursofalk® 500 mg fi lmomhulde tabletten in 100 stuks verpakking verkrijgbaar. Ursofalk® 500 mg, met als actief bestanddeel ursodeoxycholzuur, is geïndiceerd
voor onder andere Primaire Biliaire Cirrose (PBC)1. Dankzij de 500 mg fi lmomhulde tabletten hoeven patiënten minder tabletten in te nemen. Hiermee kan een posi-tieve bijdrage worden geleverd aan een verbeterde therapietrouw.4 Met de introductie van de 500 mg tablet heeft Ursofalk® nu de meeste ursodeoxycholzuur toedieningsvormen.1-3 www.drfalkpharma.nl
Ursofalk® 500 mg
Nieuwgenerating four experimental groups: WW, WL, LW and LL
offspring. Biochemical, histological and epigenetic indicators
were investigated at 29 weeks of age.
RESULTS: Male offspring exposed to prenatal and post-
weaning western-style diet (WW) showed hepatomegaly
combined with accumulation of hepatic cholesterol and trigly-
cerides. This accumulation was associated with up-regulation
of de novo lipid synthesis, inflammation and dysregulation
of lipid storage. Elevated hepatic transaminases and incre-
ased expression of Tnfa, Cd11, Mcp1 and Tgfb underpin the
severity of liver injury. Histopathological analysis revealed
the presence of advanced steatohepatitis in WW offspring. In
addition, alterations in DNA methylation in key metabolic
genes (Ppara, Insig, and Fasn) were detected. CONCLU-
SION: Maternal dietary fat intake during early development
programmes susceptibility to liver disease in male offspring,
mediated by disturbances in lipid metabolism and inflamma-
tory response. Long-lasting epigenetic changes may underlie
this dysregulation.
Maternal Western-style high fat diet induces sex-specific
physiological and molecular changes in two-week-old mouse
offspring
Mischke M, Pruis MG, Boekschoten MV, Groen AK, Fitri AR,
van de Heijning BJ, Verkade HJ, Müller M, Plösch T*, Steegenga
WT*. PLoS One. 2013 Nov 5;8(11):e78623. doi: 10.1371/jour-
nal.pone.0078623.
Maternal diet is associated with the development of meta-
bolism-related and other non-communicable diseases in
offspring. Underlying mechanisms, functional profiles, and
molecular markers are only starting to be revealed. Here, we
explored the physiological and molecular impact of maternal
Western-style diet on the liver of male and female offspring.
C57BL/6 dams were exposed to either a low fat/low cholesterol
diet (LFD) or a Western-style high fat/high cholesterol diet
(WSD) for six weeks before mating, as well as during gestation
and lactation. Dams and offspring were sacrificed at postnatal
day 14, and body, liver, and blood parameters were assessed.
The impact of maternal WSD on the pups’ liver gene expres-
sion was characterised by whole-transcriptome microarray
analysis. Exclusively male offspring had significantly higher
body weight upon maternal WSD. In offspring of both sexes
of WSD dams, liver and blood parameters, as well as hepatic
gene expression profiles were changed. In total, 686 and 604
genes were differentially expressed in liver (p≤0.01) of males
and females, respectively. Only 10% of these significantly
changed genes overlapped in both sexes. In males, in parti-
cular alterations of gene expression with respect to develop-
mental functions and processes were observed, such as Wnt/
beta-catenin signalling. In females, mainly genes important for
lipid metabolism, including cholesterol synthesis, were chan-
ged. We conclude that maternal WSD affects physiological
parameters and induces substantial changes in the molecular
profile of the liver in two-week-old pups. Remarkably, the ob-
served biological responses of the offspring reveal pronounced
sex-specificity.
Lipotoxicity and the role of maternal nutrition
Pruis MG, van Ewijk PA, Schrauwen-Hinderling VB, Plösch T.
Acta Physiol (Oxf). 2013 Oct 1. doi: 10.1111/apha.12171. [Epub
ahead of print].
Intrauterine malnutrition predisposes the offspring towards
the development of type 2 diabetes and cardiovascular disease.
To explain this association, the Developmental Origins of
Health and Disease (DOHaD) hypothesis was introduced,
meaning that subtle environmental changes during embryonic
and fetal development can influence postnatal physiological
functions. Different mechanisms, including epigenetics, are
thought to be involved in this fetal programming, but the link
between epigenetics and disease is missing. There is increasing
evidence that ectopic lipid accumulation and/or lipotoxicity
is induced by fetal programming. The aim of this review is to
provide insights into the mechanisms underlying lipotoxicity
through programming which contributes to the increase in
hepatic and cardiac metabolic risk.
Grant: MLDS Career Development Grant 2013
Toegekend aan: Dr. Qiuwei Pan
Afdeling: Department of Gastroenterology and Hepatology,
Erasmus University Medical Center Rotterdam
Titel: Identification of remedies against emerging gastroin-
testinal and hepatic viruses by high-throughput screening of
off-patent drug library
Abstract: Rotavirus and hepatitis E virus (HEV) mainly infect
the gut and the liver, respectively. Although both are recog-
nized as emerging infectious diseases, there is currently no
proven antiviral treatment. This project will perform a high-
throughput screening of compounds that are FDA proved
drugs, with particular focus on off-patent drugs. It is expected
to discover effective but cheap therapeutic candidates against
these two viruses.
Vervolg van pagina 15.

19
proefschriften
LEVE
R
PR
OEF
SCH
RIF
T
medicaleducation about
HEPATICENCEPHALOPATHY
CME accreditation by EACCME©
This educational programme is funded by a grant from Norgine. Norgine has no involvement in the content of the programme, which is developed independently by an expert faculty. Norgine provides logistical support, where required, for the associated live meetings.
This educational website includes a number of educational programs:
• Interactivecasescenario-basedactivitiestoexploreyourmanagement, that of your peers and the Faculty
• Educationalpresentations(audio)onHE
• ImpactofHE
• ExploringtheunderlyingcausesandriskfactorsforHE
• Bestpracticediagnosisandmanagement
• HighlightsofkeypublicationsonHE
www.hepaticencephalopathy.infoSC
ORE
Com
munication•XIF103
2•01/2014
XIF1032 Lever adv A4#1.indd 1 30-01-14 09:41
Promotiedatum: 28 oktober 2013
rijksuniversiteit groningen
Promotor: prof. dr. k.n. Faber
prof. dr. a.j. moshage
Opname van vetoplosbaar vitamine A
in de darm is afhankelijk van galzou-
ten, deze worden geproduceerd door
de lever en geven gal haar emulgerende
eigenschap. Galzouten zijn potentieel
toxische moleculen, synthese en trans-
port in de enterohepatische kringloop
wordt daarom nauwkeurig gereguleerd.
Galzouten zijn liganden voor de gal-
zoutsensor FXR (farnesoid X receptor),
een ligand geactiveerde transcriptie-
factor, en reguleren op deze manier
expressie van genen betrokken bij gal-
zoutsynthese en -transport. FXR moet
echter een heterodimeer vormen met
de vitamine A receptor RXR (retinoid
X receptor) om dit te bewerkstelligen.
Op deze manier zou vitamine A invloed
kunnen hebben op galzouthomeostase.
Daarnaast wordt vitamine A in de lever
opgeslagen en gaan leverziekten vaak
gepaard met vitamine A deficiëntie
(VAD). Zo ontstaat een netwerk van in-
teracties tussen galzouten en vitamine A.
Uit het onderzoek dat in dit proefschrift
wordt beschreven wordt duidelijk dat
vitamine A invloed heeft op de expressie
van FXR-targetgenen en dus galzout-
homeostase. De galzoutexportpomp
BSEP/ABCB11 (bile salt export pump)
in de lever komt maximaal tot expres-
sie in de afwezigheid van vitamine A.
Terwijl andere FXR-genen zoals SHP
(small heterodimer partner) en FGF19
(fibroblast growth factor 19), welke
beide galzoutsynthese remmen, juist
maximaal tot expressie komen in de
aanwezigheid van vitamine A. VAD op
zich zorgde voor een verhoogde galzout-
concentratie in bloedplasma bij ratten.
Omgekeerd gaat cholestase vaak gepaard
met VAD en bovenstaande resultaten
suggereren dat VAD kan bijdragen aan
een cholestatisch ziektebeeld. Daarom
hebben wij in een diermodel het effect
van VAD bestudeerd op obstructieve
cholestase. VAD verergerde het ziek-
tebeeld dramatisch, terwijl vitamine A
therapie bij vitamine A deficiënte dieren
het ziektebeeld normaliseerde.
Deze resultaten impliceren een belang-
rijke rol voor vitamine A in het behou-
den van galzouthomeostase en sturen
aan op het nauwgezet monitoren van
de vitamine A status van cholestatische
patiënten, omdat een vitamine A tekort
de toestand van deze patiënten snel zou
kunnen doen verergeren.
Promotiedatum: 13 november 2013
rijksuniversiteit groningen
Promotor: prof. dr. r.j. porte
prof. dr. j.a. lisman
Levertransplantatie is een succesvolle
behandeling voor eindstadium leverfa-
len, maar helaas ontstaan er regelmatig
galwegcomplicaties na levertransplanta-
tie. Het meest berucht zijn de zoge-
noemde non-anastomotische galweg-
stricturen (NAS), dit zijn vernauwingen
in de galwegen binnen of buiten de lever
die moeilijk te behandelen zijn en vaak
leiden tot ziekte en de noodzaak tot re-
transplantatie.
In dit proefschrift worden nieuwe
inzichten met betrekking tot de etiologie
(de oorzaken) van deze aandoening be-
schreven, waaropvolgend de potentieel
beschermende rol van machineperfusie
ter voorkoming van galwegschade en
NAS. Samenvattend kan de etiologie van
NAS worden onderverdeeld in galweg-
schade veroorzaakt door 1) ischemie
(zuurstofgebrek), 2) een veranderde
samenstelling van gal en 3) immuun-
gemedieerde galwegschade. Van deze
oorzaken blijkt ischemie de belangrijkste
rol te spelen in de ontwikkeling van
de galwegstricturen. Men ziet dat ook
terug in de zeer hoge incidentie van
NAS (21-33%) na non-heartbeating
leverdonatie (geen circulatie) in te-
genstelling tot donatie na hersendood
SAMENVATTING PROEFSCHRIFT MARTIJN O. HOEKE
‘De rol van vitamine A in galzoutsynthese en –transport; en de relevantie voor cholestase’
SAMENVATTING PROEFSCHRIFT SANNA OP DEN DRIES
‘Bile duct injury in liver transplantation: studies on etiology and the protective role of machine perfusion’
Lees verder op pagina 21.

20 LEVER NR 1 FEBRUARI 21
(1-13%). Men heeft lang gedacht dat
er na het implanteren van de lever in
de ontvanger in sommige levers meer
(reperfusie-)schade ontstaat in de gal-
wegen waardoor NAS zich in deze levers
ontwikkeld. Echter, het blijkt uit dit
proefschrift dat het overgrote deel van
de galwegen al behoorlijk beschadigd
is aan het einde van de koude bewaar-
tijd en er wordt bewijs aangeleverd dat
niet zozeer de initiële schade aan het
galwegepitheel (de binnenbekleding van
de galwegen) bepalend is voor het al dan
niet ontwikkelen van NAS, maar het
vermogen tot regeneratie (herstel) van
het galwegepitheel.
Om de regeneratiecapaciteit van de
galwegen te behouden, is het belangrijk
om kwetsbare levers (ouder, vetter,
non-heartbeating) beter te beschermen
tegen koude ischemie. In dit proefschrift
wordt aangetoond dat een alternatieve
preservatiemethode in de vorm van
machineperfusie veel mogelijkheden
biedt, waaronder het beschermen van
de kwetsbare galwegen door het bieden
van o.a. een zuurstofrijk milieu en de
mogelijkheid tot beoordeling van het
donororgaan om te bepalen of die wel of
niet getransplanteerd kan worden.
Tenslotte wordt besproken op welke
manier Nederlandse leverpatiënten ge-
informeerd willen worden en betrokken
willen zijn bij het beslissingsproces om
een (risicovolle) donorlever te accepte-
ren voor levertransplantatie.
Promotiedatum: 15 november 2013
universiteit van amsterdam
Promotor: prof. dr. r.p.j. Oude elferink
Co-promotor:dr. c.c. paulusma
Progressive familial intrahepatic cho-
lestasis (PFIC) is een ernstige erfelijke
vorm van cholestase. Er zijn 3 typen
bekend (PFIC1-3) die worden veroor-
zaakt door mutaties in respectievelijk
ATP8B1, ABCB11 en ABCB4. Deze
genen coderen voor transporteiwitten
in het canaliculaire membraan van de
hepatocyt die nodig zijn voor de juiste
galvorming. Muismodellen met een
gelijke mutatie vertonen echter een min-
der ernstig ziektebeeld dan patiënten.
Het is onze hypothese dat dit verschil
tussen muis en mens is te danken aan
een verschil in hydrofobiciteit en toxi-
citeit van de circulerende galzouten in
mens en muis. We hebben geprobeerd
een meer humaan muismodel te creëren
door een muismodel te gebruiken met
een verminderde galzout (re)hydroxyle-
ringscapaciteit.
Doordat muizen in staat zijn galzouten
te (re)hydroxyleren zullen zij altijd een
meer hydrofiele galzoutpool hebben
in vergelijking tot mensen. Wij heb-
ben gekeken naar een muismodel met
verminderde galzoutsynthese en (re)
hydroxylatie capaciteit. Deze muizen
(hepatic reductase null; Hrn) missen
95% van alle cytochroom p450 activi-
teit in de lever en hebben daardoor een
sterk verminderde galzoutpool (~30%
vergeleken met WT muizen) bestaande
uit relatief hydrofobe galzouten. Door
deze muizen een dieet met (hydrofoob)
galzout te geven krijgen zij een meer
hydrofobe galzoutpool. Het kruisen van
deze muizen met Atp8b1G308V/G308V
en Abcb4-/- muizen (respectievelijk
modellen voor PFIC1 en PFIC3) laat
zien dat beide dubbeltransgene model-
len ontvankelijker zijn voor cholestase
en dat de ernst van het ziektebeeld
wordt bepaald door hydrophobiciteit
van plasma of gal in respectievelijk
Atp8b1G308V/G308V /Hrn en Abcb4-
/-/Hrn muizen. Echter de ernst van het
ziektebeeld is nog altijd niet zo ernstig
als in de mens.
Tevens heb ik in dit proefschrift laten
zien dat de natuurlijke steatose die Hrn
muizen hebben afneemt door het voeren
van een galzoutdieet. Deze verminde-
ring van levervet is FXR-afhankelijk.
INCIVO® (telaprevir) - Verkorte Productinformatie voor gebruik in Nederland
Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via www.lareb.nl.
Samenstelling: INCIVO® filmomhulde tabletten. Elke tablet bevat 375 mg telaprevir. Farmaceutische vorm: Gele, capsulevormige tablet van ongeveer 20 mm lang, waarop aan één kant ‘T375’ staat. Indicaties: INCIVO, in combinatie met peginterferon alfa en ribavirine, is geïndiceerd voor de behandeling van genotype 1 chronische hepatitis C bij volwassen patiënten met gecompenseerde leverziekte (waaronder cirrose) (1) die nooit eerder behandeld werden (therapienaïef), of (2) die eerder behandeld werden met interferon alfa (gepegyleerd of niet gepegyleerd) als monotherapie of in combinatie met ribavirine, waaronder patiënten met een recidief, partiële responders en patiënten zonder respons (null responders). Dosering en wijze van toediening: INCIVO, 1125 mg (drie filmomhulde tabletten van 375 mg) dient tweemaal daags (b.i.d.) oraal met voedsel te worden ingenomen. Als alternatief kan 750 mg (twee tabletten van 375 mg) iedere 8 uur (q8h) oraal met voedsel ingenomen worden. De totale dagelijkse dosis is 6 tabletten (2.250 mg). INCIVO moet worden toegediend in combinatie met ribavirine en ofwel peginterferon alfa-2a ofwel -2b. Aanbevolen wordt dat patiënten met ribonucleïnezuur van het hepatitis C virus (HCV-RNA) > 1.000 IE/ml in week 4 of week 12 met de behandeling stoppen. Behandelduur: De behandeling met INCIVO moet worden gestart in combinatie met peginterferon alfa en ribavirine en gedurende 12 weken worden aangehouden. Patiënten zonder cirrose die therapienaïef zijn of een recidief hadden op een eerdere behandeling, en bij wie HCV-RNA ondetecteerbaar is in week 4 en 12, moeten additioneel nog 12 weken behandeld worden met alleen peginterferon alfa en ribavirine, voor een totale behandelingsduur van 24 weken. Voor alle andere patiënten wordt een additionele behandelingsperiode van 36 weken met alleen peginterferon alfa en ribavirine aanbevolen, voor een totale behandelingsduur van 48 weken. Contra-indicaties: Overgevoeligheid voor het werkzame bestanddeel of voor één van de hulpstoffen. Gelijktijdige toediening met werkzame stoffen die voor hun klaring sterk afhankelijk zijn van CYP3A en waarvan verhoogde plasmaconcentraties geassocieerd zijn met ernstige en/of levensbedreigende gebeurtenissen. Dit zijn onder andere de werkzame stoffen alfuzosine, amiodaron, bepridil, kinidine, astemizol, terfenadine, cisapride, pimozide, moederkoornalkaloïden (dihydro-ergotamine, ergonovine, ergotamine, methylergonovine), lovastatine, simvastatine, atorvastatine, sildenafil of tadalafil (alleen indien gebruikt voor de behandeling van pulmonale arteriële hypertensie), quetiapine en oraal toegediend midazolam of triazolam. Gelijktijdige toediening met klasse-Ia- of -III-antiaritmica, behalve intraveneus lidocaïne. Gelijktijdige toediening van INCIVO met werkzame stoffen die CYP3A sterk induceren, bijvoorbeeld rifampicine, sint-janskruid (Hypericum perforatum), carbamazepine, fenytoïne en fenobarbital en dus kunnen leiden tot lagere blootstelling en verlies van werkzaamheid van INCIVO. Raadpleeg de SPC van peginterferon alfa en van ribavirine voor een lijst met de contra-indicaties van deze producten, aangezien INCIVO in combinatie met peginterferon alfa en ribavirine gebruikt moet worden. Belangrijkste waarschuwingen en voorzorgen: Ernstige rash: Er zijn ernstige, mogelijk levensbedreigende en fatale huidreacties gemeld bij de INCIVO-combinatiebehandeling. Toxische epidermale necrolyse (TEN), inclusief fatale afloop, is waargenomen na het in de handel brengen. Fatale gevallen zijn gerapporteerd bij patiënten met progressieve rash en systemische symptomen die INCIVO-combinatiebehandeling bleven krijgen nadat een ernstige huidreactie geïdentificeerd was. In placebogecontroleerde fase-2- en fase-3-studies had 0,4% van de patiënten vermoedelijk Drug Rash with Eosinophilia and Systemic Symptoms (DRESS). In de klinische praktijk met INCIVO had minder dan 0,1% van de patiënten stevensjohnsonsyndroom (SJS). In placebogecontroleerde fase-2- en fase-3-studies werd ernstige rash (voornamelijk eczemateus, met jeuk en die meer dan 50% van het lichaamsoppervlak beslaat) gemeld bij 4,8% van de patiënten die behandeld werden met de INCIVO-combinatiebehandeling tegenover 0,4% van degenen die behandeld werden met peginterferon alfa en ribavirine. Voorschrijvers dienen ervoor te zorgen dat de patiënten volledig geïnformeerd zijn over het risico op ernstige rash en dat ze hun voorschrijvend arts onmiddellijk moeten raadplegen zodra ze een nieuwe rash krijgen of als een bestaande rash verergert. Alle gevallen van rash moeten regelmatig gecontroleerd worden op progressie tot de rash is verdwenen. In het geval van een ernstige huidreactie, moet stopzetting van andere geneesmiddelen waarvan bekend is dat zij geassocieerd zijn met ernstige huidreacties overwogen worden. Anemie: In placebogecontroleerde fase-2- en fase-3-studies namen de totale incidentie en de ernst van anemie toe bij de INCIVO-combinatiebehandeling in vergelijking met een behandeling met alleen peginterferon alfa en ribavirine. Voor de behandeling van anemie dient men de SPC van ribavirine te raadplegen voor de richtlijnen over de dosisverlaging. Als de behandeling met ribavirine wordt stopgezet voor de behandeling van anemie, moet ook de behandeling met INCIVO definitief worden stopgezet. Als de behandeling met INCIVO wordt stopgezet voor anemie, kunnen patiënten verdergaan met de behandeling met peginterferon alfa en ribavirine. Hemoglobine dient voor en tijdens de INCIVO-combinatiebehandeling op regelmatige tijdstippen gecontroleerd te worden. De dosis van INCIVO mag niet worden verlaagd en de behandeling met INCIVO mag niet worden hervat indien stopgezet. Zwangerschap en anticonceptie bij mannen en vrouwen: INCIVO wordt niet aanbevolen voor gebruik tijdens de zwangerschap en bij vrouwen die zwanger kunnen worden en geen anticonceptie toepassen. Zowel vrouwelijke patiënten die zwanger kunnen worden en hun mannelijke partners, als mannelijke patiënten en hun vrouwelijke partners moeten tijdens en na de behandeling met INCIVO twee effectieve anticonceptiemethoden gebruiken, zoals wordt aanbevolen in de SPC van ribavirine. Hormonale anticonceptiva kunnen worden voortgezet, maar zijn wellicht niet betrouwbaar tijdens gebruik van INCIVO en gedurende maximaal twee maanden na het stoppen met INCIVO. Cardiovasculair: Gebruik van INCIVO moet worden vermeden bij patiënten met congenitale QT-verlenging, of met een familiale voorgeschiedenis van congenitale QT-verlenging of plotse dood. Algemeen: INCIVO mag niet als monotherapie worden toegediend en mag alleen worden voorgeschreven in combinatie met zowel peginterferon alfa als ribavirine. De SPC van peginterferon alfa en van ribavirine moeten daarom worden geraadpleegd voordat de behandeling met INCIVO wordt gestart. Interacties: INCIVO is een sterke, tijdsafhankelijke remmer van CYP3A4 (d.w.z. remming kan sterker zijn tijdens de eerste twee weken van behandeling) en remt P-gp ook aanzienlijk. Gelijktijdige toediening van INCIVO en geneesmiddelen die CYP3A en/of P-gp induceren, kan de plasmaconcentraties van telaprevir verlagen. Gelijktijdige toediening van INCIVO en geneesmiddelen die CYP3A en/of P-gp remmen, kan de plasmaconcentraties van telaprevir verhogen. Toediening van INCIVO kan de systemische blootstelling aan geneesmiddelen die substraat zijn van CYP3A of P-gp verhogen, wat het therapeutisch effect en bijwerkingen van die middelen kan verhogen of verlengen. Telaprevir remt de organisch anion-transporterende polypeptiden OATP1B1 en OATP2B1. Op basis van de resultaten van klinische geneesmiddelinteractiestudies, kan inductie van metabole enzymen door telaprevir niet worden uitgesloten. Voor een overzicht van interacties en doseringsaanbevelingen met andere geneesmiddelen, zie SPC. Bijwerkingen: op INCIVO (ingenomen in combinatie met peginterferon alfa en ribavirine): Zeer vaak (≥1/10): anemie, pruritus, rash, nausea, diarree, braken, hemorroïden, proctalgie. Vaak (≥1/100 tot <1/10): trombocytopenie, lymfopenie, hyperurikemie, dysgeusie, syncope, anale pruritus, rectale hemorragie, anale fissuur, eczeem, gezwollen gezicht, exfoliatieve uitslag, orale candidiasis, hypothyreoïdie, hypokaliëmie, hyperbilirubinemie, perifeer oedeem, productsmaak abnormaal. Soms (≥1/1000 tot <1/100): jicht, retinopathie, proctitis, DRESS, urticaria, creatinine in bloed verhoogd, pre-renale azotemie met of zonder acuut renaal falen. Zelden (≤1/1000): SJS, TEN, erythema multiforme. Farmacotherapeutische categorie: Direct werkende antivirale middelen. ATC code: J05AE11. Afleverstatus: UR. Registratiehouder: Janssen Cilag International NV, Turnhoutseweg 30, B2340 Beerse, België. Uitgebreide productinformatie: zie voor volledige SPC www.janssennederland.nl. Datum: 18/12/2013
Janssen-Cilag B.V.
Productinformatie behorende bij advertentie elders in dit blad
Telefoon: 0800-242 42 42 • E-mail: [email protected] • Website: www.janssennederland.nl
PHNL
/INC/
0114
/000
1
JAN 0892 bijsluiter 88x116_DEF.indd 1 30/01/14 09:50
INCIVO® (telaprevir) - Verkorte Productinformatie voor gebruik in Nederland
Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via www.lareb.nl.
Samenstelling: INCIVO® filmomhulde tabletten. Elke tablet bevat 375 mg telaprevir. Farmaceutische vorm: Gele, capsulevormige tablet van ongeveer 20 mm lang, waarop aan één kant ‘T375’ staat. Indicaties: INCIVO, in combinatie met peginterferon alfa en ribavirine, is geïndiceerd voor de behandeling van genotype 1 chronische hepatitis C bij volwassen patiënten met gecompenseerde leverziekte (waaronder cirrose) (1) die nooit eerder behandeld werden (therapienaïef), of (2) die eerder behandeld werden met interferon alfa (gepegyleerd of niet gepegyleerd) als monotherapie of in combinatie met ribavirine, waaronder patiënten met een recidief, partiële responders en patiënten zonder respons (null responders). Dosering en wijze van toediening: INCIVO, 1125 mg (drie filmomhulde tabletten van 375 mg) dient tweemaal daags (b.i.d.) oraal met voedsel te worden ingenomen. Als alternatief kan 750 mg (twee tabletten van 375 mg) iedere 8 uur (q8h) oraal met voedsel ingenomen worden. De totale dagelijkse dosis is 6 tabletten (2.250 mg). INCIVO moet worden toegediend in combinatie met ribavirine en ofwel peginterferon alfa-2a ofwel -2b. Aanbevolen wordt dat patiënten met ribonucleïnezuur van het hepatitis C virus (HCV-RNA) > 1.000 IE/ml in week 4 of week 12 met de behandeling stoppen. Behandelduur: De behandeling met INCIVO moet worden gestart in combinatie met peginterferon alfa en ribavirine en gedurende 12 weken worden aangehouden. Patiënten zonder cirrose die therapienaïef zijn of een recidief hadden op een eerdere behandeling, en bij wie HCV-RNA ondetecteerbaar is in week 4 en 12, moeten additioneel nog 12 weken behandeld worden met alleen peginterferon alfa en ribavirine, voor een totale behandelingsduur van 24 weken. Voor alle andere patiënten wordt een additionele behandelingsperiode van 36 weken met alleen peginterferon alfa en ribavirine aanbevolen, voor een totale behandelingsduur van 48 weken. Contra-indicaties: Overgevoeligheid voor het werkzame bestanddeel of voor één van de hulpstoffen. Gelijktijdige toediening met werkzame stoffen die voor hun klaring sterk afhankelijk zijn van CYP3A en waarvan verhoogde plasmaconcentraties geassocieerd zijn met ernstige en/of levensbedreigende gebeurtenissen. Dit zijn onder andere de werkzame stoffen alfuzosine, amiodaron, bepridil, kinidine, astemizol, terfenadine, cisapride, pimozide, moederkoornalkaloïden (dihydro-ergotamine, ergonovine, ergotamine, methylergonovine), lovastatine, simvastatine, atorvastatine, sildenafil of tadalafil (alleen indien gebruikt voor de behandeling van pulmonale arteriële hypertensie), quetiapine en oraal toegediend midazolam of triazolam. Gelijktijdige toediening met klasse-Ia- of -III-antiaritmica, behalve intraveneus lidocaïne. Gelijktijdige toediening van INCIVO met werkzame stoffen die CYP3A sterk induceren, bijvoorbeeld rifampicine, sint-janskruid (Hypericum perforatum), carbamazepine, fenytoïne en fenobarbital en dus kunnen leiden tot lagere blootstelling en verlies van werkzaamheid van INCIVO. Raadpleeg de SPC van peginterferon alfa en van ribavirine voor een lijst met de contra-indicaties van deze producten, aangezien INCIVO in combinatie met peginterferon alfa en ribavirine gebruikt moet worden. Belangrijkste waarschuwingen en voorzorgen: Ernstige rash: Er zijn ernstige, mogelijk levensbedreigende en fatale huidreacties gemeld bij de INCIVO-combinatiebehandeling. Toxische epidermale necrolyse (TEN), inclusief fatale afloop, is waargenomen na het in de handel brengen. Fatale gevallen zijn gerapporteerd bij patiënten met progressieve rash en systemische symptomen die INCIVO-combinatiebehandeling bleven krijgen nadat een ernstige huidreactie geïdentificeerd was. In placebogecontroleerde fase-2- en fase-3-studies had 0,4% van de patiënten vermoedelijk Drug Rash with Eosinophilia and Systemic Symptoms (DRESS). In de klinische praktijk met INCIVO had minder dan 0,1% van de patiënten stevensjohnsonsyndroom (SJS). In placebogecontroleerde fase-2- en fase-3-studies werd ernstige rash (voornamelijk eczemateus, met jeuk en die meer dan 50% van het lichaamsoppervlak beslaat) gemeld bij 4,8% van de patiënten die behandeld werden met de INCIVO-combinatiebehandeling tegenover 0,4% van degenen die behandeld werden met peginterferon alfa en ribavirine. Voorschrijvers dienen ervoor te zorgen dat de patiënten volledig geïnformeerd zijn over het risico op ernstige rash en dat ze hun voorschrijvend arts onmiddellijk moeten raadplegen zodra ze een nieuwe rash krijgen of als een bestaande rash verergert. Alle gevallen van rash moeten regelmatig gecontroleerd worden op progressie tot de rash is verdwenen. In het geval van een ernstige huidreactie, moet stopzetting van andere geneesmiddelen waarvan bekend is dat zij geassocieerd zijn met ernstige huidreacties overwogen worden. Anemie: In placebogecontroleerde fase-2- en fase-3-studies namen de totale incidentie en de ernst van anemie toe bij de INCIVO-combinatiebehandeling in vergelijking met een behandeling met alleen peginterferon alfa en ribavirine. Voor de behandeling van anemie dient men de SPC van ribavirine te raadplegen voor de richtlijnen over de dosisverlaging. Als de behandeling met ribavirine wordt stopgezet voor de behandeling van anemie, moet ook de behandeling met INCIVO definitief worden stopgezet. Als de behandeling met INCIVO wordt stopgezet voor anemie, kunnen patiënten verdergaan met de behandeling met peginterferon alfa en ribavirine. Hemoglobine dient voor en tijdens de INCIVO-combinatiebehandeling op regelmatige tijdstippen gecontroleerd te worden. De dosis van INCIVO mag niet worden verlaagd en de behandeling met INCIVO mag niet worden hervat indien stopgezet. Zwangerschap en anticonceptie bij mannen en vrouwen: INCIVO wordt niet aanbevolen voor gebruik tijdens de zwangerschap en bij vrouwen die zwanger kunnen worden en geen anticonceptie toepassen. Zowel vrouwelijke patiënten die zwanger kunnen worden en hun mannelijke partners, als mannelijke patiënten en hun vrouwelijke partners moeten tijdens en na de behandeling met INCIVO twee effectieve anticonceptiemethoden gebruiken, zoals wordt aanbevolen in de SPC van ribavirine. Hormonale anticonceptiva kunnen worden voortgezet, maar zijn wellicht niet betrouwbaar tijdens gebruik van INCIVO en gedurende maximaal twee maanden na het stoppen met INCIVO. Cardiovasculair: Gebruik van INCIVO moet worden vermeden bij patiënten met congenitale QT-verlenging, of met een familiale voorgeschiedenis van congenitale QT-verlenging of plotse dood. Algemeen: INCIVO mag niet als monotherapie worden toegediend en mag alleen worden voorgeschreven in combinatie met zowel peginterferon alfa als ribavirine. De SPC van peginterferon alfa en van ribavirine moeten daarom worden geraadpleegd voordat de behandeling met INCIVO wordt gestart. Interacties: INCIVO is een sterke, tijdsafhankelijke remmer van CYP3A4 (d.w.z. remming kan sterker zijn tijdens de eerste twee weken van behandeling) en remt P-gp ook aanzienlijk. Gelijktijdige toediening van INCIVO en geneesmiddelen die CYP3A en/of P-gp induceren, kan de plasmaconcentraties van telaprevir verlagen. Gelijktijdige toediening van INCIVO en geneesmiddelen die CYP3A en/of P-gp remmen, kan de plasmaconcentraties van telaprevir verhogen. Toediening van INCIVO kan de systemische blootstelling aan geneesmiddelen die substraat zijn van CYP3A of P-gp verhogen, wat het therapeutisch effect en bijwerkingen van die middelen kan verhogen of verlengen. Telaprevir remt de organisch anion-transporterende polypeptiden OATP1B1 en OATP2B1. Op basis van de resultaten van klinische geneesmiddelinteractiestudies, kan inductie van metabole enzymen door telaprevir niet worden uitgesloten. Voor een overzicht van interacties en doseringsaanbevelingen met andere geneesmiddelen, zie SPC. Bijwerkingen: op INCIVO (ingenomen in combinatie met peginterferon alfa en ribavirine): Zeer vaak (≥1/10): anemie, pruritus, rash, nausea, diarree, braken, hemorroïden, proctalgie. Vaak (≥1/100 tot <1/10): trombocytopenie, lymfopenie, hyperurikemie, dysgeusie, syncope, anale pruritus, rectale hemorragie, anale fissuur, eczeem, gezwollen gezicht, exfoliatieve uitslag, orale candidiasis, hypothyreoïdie, hypokaliëmie, hyperbilirubinemie, perifeer oedeem, productsmaak abnormaal. Soms (≥1/1000 tot <1/100): jicht, retinopathie, proctitis, DRESS, urticaria, creatinine in bloed verhoogd, pre-renale azotemie met of zonder acuut renaal falen. Zelden (≤1/1000): SJS, TEN, erythema multiforme. Farmacotherapeutische categorie: Direct werkende antivirale middelen. ATC code: J05AE11. Afleverstatus: UR. Registratiehouder: Janssen Cilag International NV, Turnhoutseweg 30, B2340 Beerse, België. Uitgebreide productinformatie: zie voor volledige SPC www.janssennederland.nl. Datum: 18/12/2013
Janssen-Cilag B.V.
Productinformatie behorende bij advertentie elders in dit blad
Telefoon: 0800-242 42 42 • E-mail: [email protected] • Website: www.janssennederland.nl
PHNL
/INC/
0114
/000
1
JAN 0892 bijsluiter 88x116_DEF.indd 1 30/01/14 09:50
Verkorte samenvatting van de productkenmerken van Pegasys®
Samenstelling: Pegasys® bevat peginterferon alfa-2a, gevormd door conjugatie van PEG-reagens (molecuulmassa 40 KD) aan interferon alfa-2a. Pegasys is beschikbaar in voorgevulde wegwerpspuit met 90, 135 of 180 μg peginterferon alfa-2a per 0,5 ml en voorgevulde pen met gebruiksklare oplossing voor injectie (alleen 135 of 180 μg). Indicatie: 1. chronische hepatitis C (CHC) bij niet eerder behandelde kinderen en adolescenten van 5 jaar en ouder en bij volwassen patiënten die positief zijn voor HCV-RNA in het serum, inclusief volwassen patiënten met gecompenseerde cirrose en/of co-infectie met klinisch stabiele HIV. De optimale behandeling is in combinatie met ribavirine. Voor volwassenen is deze combinatie geïndiceerd bij naïeve patiënten en patiënten bij wie eerdere behandeling met interferon alfa (gepegyleerd of niet-gepegyleerd) ontoereikend was. Bij behan-deling tijdens de kindertijd is het van belang er rekening mee te houden dat groeiremming wordt geïnduceerd. Het is onduidelijk of deze groeiremming omkeerbaar is. 2. HBeAg-positieve of -negatieve chronische hepatitis B (CHB) bij volwassen patiënten met gecompenseerde leverziekte en bewijs van virale replicatie, verhoogd ALT en histologisch bevestigde leverontsteking en/of fibrose. Contra-indicaties: overgevoeligheid voor alfa interferonen of een van de hulp stoffen, auto-immuun hepatitis, ernstige leverdisfunctie of gedecompenseerde levercirrose, ernstige al bestaande hartaandoening in de anamnese en HIV-CHC patiënten met cirrose en een Child-Pugh score ≥6 behalve als deze volledig toegeschreven kan worden aan indirecte hyperbilirubinemie veroorzaakt door geneesmiddelen zoals atazanavir en indinavir, combinatie met telbivudine, neonaten en kinderen tot 3 jaar oud vanwege de hulpstof benzylalcohol en de aanwezigheid of voorgeschiedenis van een ernstige psychiatrische aandoening bij pediatrische patiënten. Dosering en wijze van toediening: de aanbevolen dosering Pegasys voor pediatrische patiënten is afhankelijk van het lichaamsoppervlak (minimaal 0,7 m2) en voor volwassen patiënten de aanbevolen dosering 180 μg eenmaal per week, subcutaan toegediend in buik of dij. De therapieduur is o.a. afhankelijk van het genotype, basale ‘viral load’ en de respons. Belangrijkste waarschuwingen: ernstige effecten op het centrale zenuwstelsel, voornamelijk depressie, suïcidale gedachten en pogingen tot suïcide, zijn waargenomen bij enkele patiënten tijdens en soms nog tot 6 maanden na Pegasys-behandeling. Pegasys-behandeling werd in verband gebracht met anemie (in combinatie met ribavirine), trombo-cytopenie, leukopenie, neutropenie en lymfopenie. Pancytopenie en beenmergsuppressie werden in verband gebracht met Pegasys in combinatie met ribavirine en azathioprine. Bij gebruik van alfa interferonen zijn schildklierfunctie-afwijkingen of verergering van schildklieraandoeningen gemeld. Hypertensie, supraventriculaire aritmieën, decompensatio cordis, pijn op de borst en myocardinfarct zijn in verband gebracht met alfa-interferontherapie. Indien tijdens behandeling aanwijzingen voor leverdecompensatie ontstaan dient de behandeling met Pegasys onmiddellijk gestaakt te worden. Ernstige, acute overgevoeligheidsreacties zijn zelden waargenomen tijdens behandeling met alfa interferonen. Auto-immuunziekte en gevallen van het Vogt-Koyanagi-Harada syndroom zijn gemeld. Ernstige infecties zijn gemeld tijdens behandeling met alfa interferonen. Bij Pegasys zijn hypogly-kemie, hyperglykemie, diabetes mellitus, retinopathie en pulmonale symptomen waargenomen. Tevens zijn exacerbatie en provocatie van psoriasis en sarcoïdose waargenomen. Lever- en niertrans-plantaatafstotingen zijn gemeld met Pegasys, alleen of in combinatie met ribavirine. In combinatie met ribavirine zijn er dentale en periodontale aandoeningen gemeld. Voorzichtigheid is geboden als Pegasys en ribavarine toegevoegd worden aan een HAART therapie. Pegasys mag alleen tijdens de zwangerschap gebruikt worden wanneer het mogelijke voordeel het mogelijke risico voor de foetus rechtvaardigt. Borstvoeding moet voorafgaand aan de behandeling worden gestopt. Bijwerkingen: in studies bleek het veiligheidsprofiel van Pegasys bij CHB gelijk aan dat bij CHC. Met uitzondering van pyrexie was de frequentie van de meerderheid van de bijwerkingen opmerkelijk lager bij patiënten met CHB dan bij patiënten met CHC. Bij patiënten met HIV-CHC co-infectie waren de klinische bijwerkingprofielen gemeld voor Pegasys, alleen of in combinatie met ribavirine, gelijk aan die bij patiënten met CHC mono-infectie. Zeer vaak (≥1/10) voorkomende bijwerkingen tijdens Pegasys monotherapie of in combinatie met ribavirine i.h.g. van CHC zijn anorexie, hoofdpijn, angst, verminderde concentratie, dyspnoe, hoesten, alopecia, pruritus, dermatitis, droge huid, myalgie, artralgie, vermoeidheid, pyrexie, en asthenie. Bijwerkingen zeer vaak, tijdens behandeling met Pegasys in combinatie met ribavirine bij CHC, of vaak (>1/100 tot <1/10) bij Pegasys monotherapie bij CHB, voor komend zijn depressie, slapeloosheid, duizelig heid, diarree, misselijkheid, buikpijn, rillingen, pijn, reacties op de injectieplaats en prikkel-baarheid. Afleverstatus: U.R. Pegasys wordt volledig vergoed. Volledige productinformatie is beschikbaar bij Roche Nederland B.V., Postbus 44, 3440 AA WOERDEN. Telefoon: 0348-438171, www.roche.nl (03/2013, v1)
Voor meer informatie: zie www.rochevirology.nl
2013-01-07 Pegasys bijsluiter 83x119mm.indd 1 07-01-14 17:37
Verkorte SPC XIFAXAN® 550 mg Filmomhulde TablettenNaam van het geneesmiddel XIFAXAN® 550 mg filmomhulde tabletten. Registratiehouder Norgine BV, Hogehilweg 7, Amsterdam. Kwalitatieve en kwantitatieve samenstelling Elke filmomhulde tablet bevat 550 mg rifaximine. Farmacotherapeutische groep Intestinale, anti-infectiemiddelen-antibiotica. Farmaceutische vorm Filmomhulde tablet. Therapeutische indicaties XIFAXAN® is geïndiceerd voor de vermindering van recidiverende episodes van manifeste hepatische encefalopathie bij patiënten ≥ 18 jaar. Contra-indicaties Overgevoeligheid voor rifaximine, rifamycine-derivaten of voor de hulpstoffen van XIFAXAN®, Gevallen van darmobstructie. Bijzondere waarschuwingen en voorzorgen bij gebruik Clostridium difficile geassocieerde diarree (CDAD) is gemeld bij het gebruik van bijna alle antibacteriële middelen, inclusief rifaximine. De kans dat een rifaximine behandeling gepaard gaat met CDAD en pseudomembraneuze colitis (PMC) kan niet worden uitgesloten. Vanwege het gebrek aan gegevens en de kans op ernstige verstoring van de darmflora met onbekende gevolgen, wordt gelijktijdige toediening van rifaximine met andere rifamycines niet aanbevolen. Patiënten dienen te worden ingelicht dat, ondanks de verwaarloosbare absorptie van het geneesmiddel (minder dan 1%), rifaximine net zoals alle rifamycine-derivaten een roodachtige verkleuring van de urine kan veroorzaken. Verminderde leverfunctie: met voorzichtigheid gebruiken bij patiënten met ernstige (Child-Pugh C) leverfunctiestoornis en bij patiënten met MELD (Model for End-Stage Liver Disease) score > 25. Vanwege de effecten op de darmflora zou de werkzaamheid van oestrogeen bevattende orale anticonceptiva kunnen afnemen na inname van rifaximine. Echter, dergelijke interacties zijn niet vaak gemeld. Het wordt aanbevolen om aanvullende anticonceptiemaatregelen te nemen, in het bijzonder wanneer het oestrogeengehalte van orale anticonceptiva lager is dan 50 mg. Bijwerkingen Infecties en parasitaire aandoeningen: Soms: Clostridia-infectie, urineweginfectie, candidiasis. Zelden: Pneumonie, cellulitis, bovenste luchtweg-infecties, rhinitis. Bloed- en lymfestelselaandoeningen: Soms: Anemie. Niet bekend: Trombocytopenie. Voedings- en stofwisselingsstoornissen: Soms: Anorexie, hyperkaliëmie. Zelden: Dehydratie. Psychische stoornissen: Vaak: Depressie. Soms: Verwarde toestand, angst, hypersomnie, insomnia. Zenuwstelselaandoeningen: Vaak: Duizeligheid, hoofdpijn. Soms: Evenwichts-stoornissen, amnesie, convulsie, aandachtsstoornissen, hypo-esthesie, geheugen vermindering. Niet bekend: Anafylactische reacties, angio-oedeem, overgevoeligheid. Bloedvataandoeningen: Soms: Opvliegers. Zelden: Hypertensie, hypotensie. Niet bekend: Presyncope, syncope. Ademhalingsstelsel-, borstkas- en mediastinumaandoeningen: Vaak: Dyspneu. Soms: Pleurale effusie. Zelden: Chronische obstructieve longziekte. Maagdarmstelsel-aandoeningen: Vaak: Bovenbuik-pijn, abdominale distensie, diarree, misselijkheid, braken, ascites. Soms: Abdominale pijn, oesofagusspataderen-bloeding, droge mond, maagongemak. Zelden: Constipatie. Lever- en galaandoeningen: Niet bekend: Abnormale leverfunctietests. Huid- en onderhuidaandoeningen: Vaak: Huiduitslag, pruritus. Niet bekend: Dermatitis, eczeem. Skeletspierstelsel- en bindweefselaandoeningen: Vaak: Spierspasmen, artralgie. Soms: Myalgie. Zelden: Rugpijn. Nier- en urinewegaandoeningen: Soms: Dysurie, pollakisurie. Zelden: Proteïnurie. Algemene aandoeningen en toedieningsplaats-stoornissen: Vaak: Oedeem perifeer. Soms: Oedeem, pyrexie. Zelden: Asthenie. Onderzoeken: Niet bekend: Abnormale INR-waarden (International Normalised Ratios). Letsels, intoxicaties en verrichtingscomplicaties: Soms: Val. Zelden: Kneuzing, procedurepijn. Kanalisatie UR. Prijs Voor prijzen zie Z-index. Datum 28 januari 2013. Volledige SPC is op aanvraag verkrijgbaar.
1. Bass, N.M., et al. N Engl J Med, 2010; 362(12):1071-81. 2. Sanyal, A., et al. Aliment Pharmacol Ther, 2011; 34(8):853-61.
NIE
UW
SCORE Communication • XIF1027
SAMENVATTING PROEFSCHRIFT CINDy KUNNE
‘Mouse Models of cholestatic liver disease; pfic revisited’
Vervolg van pagina 19.
Proefschriftenservice
Het is voor leden van de vereni-
ging mogelijk om via het secre-
tariaat recente proefschriften
aan te vragen. Aan toekomstige
promovendi wordt verzocht om
een exemplaar van hun proef-
schrift toe te zenden aan het
secretariaat onder vermelding
van correspondentieadres, zodat
aanvragen doorgestuurd kunnen
worden naar de promovendus.
Lees verder op pagina 23.
Ursofalk® 500 mg filmomhulde tabletten.Kwalitatieve en kwantitatieve samenstelling: Ursofalk® 500 mg filmomhulde tabletten bevatten 500 mg ursodeoxycholzuur (UDCA) per tablet. Therapeutische indicaties: Het oplossen van cholesterolgalstenen bij patiënten: die één of meer röntgendoorschijnende (röntgennegatieve) galstenen, bij voorkeur met een doorsnede van niet meer dan 2 cm, in een goed functionerende galblaas hebben; die een chirurgische ingreep weigeren of waarbij chirurgisch ingrijpen niet is geïndiceerd; bij wie een oververzadiging van cholesterol is aangetoond door een chemisch onderzoek van de gal verkregen door duodenumsondage. Als adjuvante medicatie vóór en na galsteenvergruizing (lithotripsie). Primaire biliaire cirrose (PBC). Behandeling van chronische (≥ 6 maanden) milde tot matig-ernstige hepatobiliaire aandoeningen (leveraandoeningen tenminste 2-3 maal de bovenste normwaarde) ten gevolge van cystische fibrose bij kinderen en jong-volwassenen. Dosering: Oplossen van galstenen (al dan niet in combinatie met lithotripsie): 8 - 10 mg UDCA per kg lichaamsgewicht per dag. De filmomhulde tabletten moeten in zijn geheel met wat vloeistof geslikt worden ’s avonds tegen bedtijd. Ze moeten regelmatig ingenomen worden. Behandeling van PBC: stadia I - III: De dagelijkse dosis is afhankelijk van het lichaamsgewicht en varieert van 1½ tot 3½ filmomhulde tabletten (12 – 16 mg ursodeoxycholzuur per kg lichaamgewicht). Gedurende de eerste 3 maanden van de behandeling dienen Ursofalk 500 mg filmomhulde tabletten in verdeelde doses te worden ingenomen tijdens de dag. Wanneer de leverfunctie verbetert kan de totale dagelijkse dosis eenmaal daags ’s avonds worden ingenomen. De filmomhulde tabletten moeten in zijn geheel met wat vloeistof geslikt worden ’s avonds tegen bedtijd. Ze moeten regelmatig ingenomen worden. Stadium IV: in combinatie met een verhoogd serumbilirubinegehalte (> 40 μg/L; geconjugeerd) dient in eerste instantie slechts de helft van de normale dosering (zie dosering voor stadia I - III) te worden gegeven (6-8 mg UDCA per kg lichaamsgewicht per dag, overeenkomend met ongeveer 1 tot 1,5 tablet Ursofalk®). Aan patiënten met PBC (stadium IV) zonder verhoogd serum bilirubinegehalte is het toegestaan direct de normale aanvangsdosering (zie dosering stadia I -III) te geven. Behandeling van hepatobiliaire aandoeningen ten gevolge van cystische fibrose: de dosering van UDCA bij de behandeling van hepatobiliaire aandoeningen ten gevolge van cystische fibrose, bedraagt 15-20 mg/kg/dag, overeenkomend met 1 tot 2-3 tabletten, in te nemen in 2 tot 3 porties gedurende de dag. Voor lagere doseringen dan 500 mg zijn Ursofalk® capsules van 250 mg beschikbaar. Wijze van toediening: oraal. Bijwerkingen: Maagdarmstelselaandoeningen: (vaak, ≥ 1/100, <1/10) kleverige ontlasting of diarree; (zeer zelden <1/10.000) ernstige pijn in de rechter bovenbuik tijdens de behandeling van PBC. Lever- en galaandoeningen: (zeer zelden <1/10.000) verkalking van galstenen; decompensatie van levercirrose tijdens de behandeling van gevorderde stadia van PBC die gedeeltelijk afnam na het staken van de behandeling. Overgevoeligheidsreacties: (zeer zelden <1/10.000) urticaria. Contra-indicaties: acute ontstekingen aan de galblaas of de galwegen; occlusie van de galwegen (occlusie van de ductus choledochus of een ductus cysticus); veelvuldige galkolieken; röntgenondoorschijnende verkalkte galstenen; verminderde contractiliteit van de galblaas; overgevoeligheid voor galzuren of voor één van de hulpstoffen. Waarschuwingen: Ursofalk® 500 mg filmomhulde tabletten dienen onder medisch toezicht te worden gebruikt. Tijdens de eerste drie maanden van de behandeling dienen elke 4 weken de leverfunctiewaarden AST, ALT en γ-GT te worden gecontroleerd, daarna elke 3 maanden. Naast het onderscheid kunnen maken tussen wel of niet reagerende patiënten die behandeld worden voor PBC, maakt deze controle ook een vroege detectie mogelijk van potentiële verslechtering van de leverfunctie, met name bij patiënten met gevorderde PBC. Bij gebruik voor het oplossen van galstenen: om de therapeutische progressie van het oplossen van galstenen te kunnen beoordelen, en om tijdig eventuele verkalking van de stenen te kunnen vaststellen moet de galblaas, afhankelijk van de afmeting van de stenen, 6 tot 10 maanden na aanvang van de behandeling worden gevisualiseerd (orale cholecystografie) met totaalbeeld en occlusies in staande en liggende houding (ultrasone controle). Indien de galblaas op röntgenfoto’s niet kan worden gevisualiseerd, of in geval van verkalkte stenen, verminderde contractiliteit van de galblaas of frequente episodes van galkoliek, moet de behandeling met Ursofalk® worden gestaakt. Bij gebruik voor de behandeling van gevorderde PBC: in zeer zeldzame gevallen is decompensatie van levercirrose waargenomen, die gedeeltelijk afnam na het staken van de behandeling. Indien diarree optreedt moet de dosering worden verlaagd, en in geval van aanhoudende diarree moet de behandeling worden gestaakt. Verpakking: doordrukstrip van transparante, kleurloze PVC/PVDC en aluminiumfolie; 100 filmomhulde tabletten in een doos. Afleverstatus en vergoeding: U.R. en volledig vergoed. RVG 112405. Registratiehouder: Dr. Falk Pharma Benelux B.V., Claudius Prinsenlaan 136A, NL-4818CP Breda, Nederland. Voor informatie: Dr. Falk Pharma Benelux B.V., Breda, 076-5244200, of raadpleeg de volledige SPC. Versie verkorte SPC-tekst: 20130516.
Referentie: 1. SPC Ursofalk® 500 mg tabletten RVG 112405. 2. SPC Ursofalk® 250 mg capsules RVG 08384.3. SPC Ursofalk® 50 mg/ml suspensie RVG 101647.4. Kane S, et al. American Journal of Medicine 2003; 114: 39-43.
65-2
013-
NL

Eén lever. Eén leven.
Eénmaal daags één tablet VIREAD.
Viread™ bij chronische hepatitis BSnelle en aanhoudende suppressie1-3
Toenemende HBsAg seroconversie1-3
Geen resistentie na 6 jaar1-3
Viread® labelwijziging: gebruik bij zwangerschap Het gebruik van tenofovirdisoproxilfumaraat tijdens
de zwangerschap kan zo nodig worden overwogen1
Gilead Sciences Netherlands B.V.www.gilead.comVoor productinformatie zie elders in dit blad
right from the start
174/NL/13-01/PM/1014
23
Verkorte productinformatie Viread 245 mg filmomhulde tablettenSamenstelling: Elke filmomhulde tablet bevat 245 mg tenofovirdisoproxil (als fumaraat), overeenkomend met 300 mg tenofovirdisoproxilfumaraat of 136 mg tenofovir. Farmacotherapeutisch groep: Nucleoside en nucleotide reverse transcriptase-remmers, ATC-code: J05AF07. Indicaties: HIV-1-infectie: Viread is geïndiceerd in combinatie met andere antiretrovirale geneesmiddelen voor de behandeling van met HIV-1 geïnfecteerde volwassenen van meer dan 18 jaar oud. Hepatitis B-infectie: Viread is geïndiceerd voor de behandeling van chronische hepatitis B bij volwassenen met: 1) gecompenseerde leverziekte, met aangetoonde actieve virale replicatie, aanhoudend verhoogde serum-alanineaminotransferase (ALAT)-spiegels en histologisch aangetoonde actieve ontsteking en/of fibrose. 2) gedecompenseerde leverziekte. Viread 245 mg filmomhulde tabletten zijn geïndiceerd voor de behandeling van chronische hepatitis B bij adolescenten in de leeftijd van 12 tot < 18 jaar met gecompenseerde leverziekte en aangetoonde immuun-actieve ziekte, d.w.z. actieve virale replicatie, aanhoudend verhoogde serum-ALAT-spiegels en histologisch aangetoonde actieve ontsteking en/of fibrose. Contra-indicaties: Bekende overgevoeligheid voor tenofovir, tenofovirdisoproxilfumaraat of voor één van de hulpstoffen. Waarschuwingen en voorzorgen: Het wordt aanbevolen de nierfunctie (creatinineklaring en serumfosfaat) te berekenen voordat wordt begonnen met de behandeling met Viread. Het eerste jaar behandeling moet de nierfunctie iedere vier weken gecontroleerd en daarna elke drie maanden. Bij patiënten met het risico op nierfunctiestoornis, dient overwogen te worden om de nierfunctie vaker te controleren.Indien bij patiënten, het serumfosfaat gehalte < 1,5 mg/dl (0,48 mmol/l) is of de creatinineklaring < 50 ml/min afgenomen is, moet de nierfunctie binnen één week opnieuw beoordeeld worden, inclusief metingen van glucose- en kaliumgehalted in het bloed an van het glucosegehalte in de urine. Bij patiënten met een afname van het serum fosfaatgehalte naar < 1,0 mg/dl (0,32 mmol/l) of een afname van het creatinineklaring naar <50 ml/min ,dient het onderbreken van de behandeling met Viread overwogen te worden. Bij patiënten met milde tot matige nierinsufficiëntie, moeten de mogelijke voordelen van behandeling worden afgenomen tegen de mogelijke risico’s. Indien gelijktijdig gebruik van Viread en nefrotoxische middelen, of van Viread en geneesmiddelen met hetzelfde renale transportsysteem (hOAT1 en 3 of MRP4 ) onvermijdelijk is, dient de renale functie wekelijks gecontroleerd te worden. Om het risico van lactaatacidose te minimaliseren bij toediening van nucleoside-analogen in combinatie met Viread moeten de patiënten nauwgezet worden gevolgd. Bij gelijktijdig gebruik van Viread en didanosine moet nauwgezet gecontroleerd worden op bijwerkingen van didanosine. Bij patiënten die voor chronish hepatisB behandeld worden, moet voorzichtigheid en controle geboden worden, voor tekenen van exacerbaties van hepatitis, in het bijzonderlijk na het stoppen van de behandeling. Indien geschikt, kan hervatting van de behandeling gerechtvaardigd zijn. Viread bevat lactose. Daarom moet Viread niet gebruikt worden bij patiënten met galactose intolerantie, Lapp lactase-deficiëntie of glucose-galactose malabsortie. Zwangerschap: Een matige hoeveelheid gegevens over zwangere vrouwen (tussen 300 en 1.000 zwangerschapsuitkomsten) duidt erop dat tenofovirdiso proxilfumaraat niet tot afwijkingen leidt of foetaal/neontaal toxisch is. De resultaten van dieronderzoek duiden niet op reproductietoxiciteit (zie rubriek 5.3). Het gebruik van tenofovirdisoproxilfumaraat tijdens de zwangerschap kan zo nodig worden overwogen. Bijwerkingen: De meest gerapporteerde, zeer vaak (≥ 1/10) bijwerkingen zijn: hypofosfatemie, duizeligheid, diarree, braken, misselijkheid, uitslag, asthenie. Vaak (≥ 1/100, < 1/10) werden de volgende bijwerkingen waargenomen: hoofdpijn, abdominale pijn, opgezette buik, flatulentie, verhoogde transaminasen, vermoeidheid; Soms (≥ 1/1.000, < 1/100): hypokaliëmie, pancreatitis, rabdomyolyse, spierzwakte, verhoogd creatinine; Zelden(≥ 1/10.000, < 1/1.000): lactaatacidose, hepatische steatose, hepatitis, angio-oedeem, osteomalacie (die zich manifesteert als botpijn en zelden bijdraagt aan het ontstaan van fracturen), myopathie, acuut nierfalen, nierfalen, acute tubulaire necrose, proximale niertubulopathie (waaronder syndroom van Fanconi), nefritis (waaronder acute interstitiële nefritis), nefrogene diabetes insipidus. Deze bijwerking kan optreden als gevolg van proximale niertubulopathie. Er wordt vanuit gegaan dat dit bij afwezigheid van deze aandoening niet in een oorzakelijk verband staat met tenofovirdisoproxilfumaraat. Verpakking: Doos met 1 of 3 flacons met 30 filmomhuldetabletten. Afleverstatus: UR. Vergoeding: volledige vergoeding. Prijs: zie Z-index. Registratiehouder: Gilead Sciences International Limited, Cambridge CB21 6GT, Verenigd Koninkrijk. Bestudeer de samenvatting van productkenmerken alvorens Viread voor te schrijven in het bijzonder vanwege dosering, bijwerkingen, waarschuwingen en voorzorgen bij gebruik, en interacties. Neem voor meer inlichtingen contact op met de lokale vertegenwoordiger: Gilead Sciences Netherlands BV, WTC, Toren D, 7e Verdieping, Strawinskylaan 779, 1077 XX Amsterdam.
De volledige informatie kunt u aanvragen bij Gilead Sciences.
Referenties 1. VIREAD, summary of Product Characteristics, november 2012. 2. Marcellin et al. AASLD 2012, Poster #374. 3. Marcellin et al. Regression of cirrhosis during treatment with tenofovir disoproxil fumarate for chronic hepatits B: a 5-year open-label follow-up study, Lancet (in press).
174/NL/13-01/PM/1014
Verkorte productinformatie Viread 245 mg filmomhulde tablettenSamenstelling: Elke filmomhulde tablet bevat 245 mg tenofovirdisoproxil (als fumaraat), overeenkomend met 300 mg tenofovirdisoproxilfumaraat of 136 mg tenofovir. Farmacotherapeutisch groep: Nucleoside en nucleotide reverse transcriptase-remmers, ATC-code: J05AF07. Indicaties: HIV-1-infectie: Viread is geïndiceerd in combinatie met andere antiretrovirale geneesmiddelen voor de behandeling van met HIV-1 geïnfecteerde volwassenen van meer dan 18 jaar oud. Hepatitis B-infectie: Viread is geïndiceerd voor de behandeling van chronische hepatitis B bij volwassenen met: 1) gecompenseerde leverziekte, met aangetoonde actieve virale replicatie, aanhoudend verhoogde serum-alanineaminotransferase (ALAT)-spiegels en histologisch aangetoonde actieve ontsteking en/of fibrose. 2) gedecompenseerde leverziekte. Viread 245 mg filmomhulde tabletten zijn geïndiceerd voor de behandeling van chronische hepatitis B bij adolescenten in de leeftijd van 12 tot < 18 jaar met gecompenseerde leverziekte en aangetoonde immuun-actieve ziekte, d.w.z. actieve virale replicatie, aanhoudend verhoogde serum-ALAT-spiegels en histologisch aangetoonde actieve ontsteking en/of fibrose. Contra-indicaties: Bekende overgevoeligheid voor tenofovir, tenofovirdisoproxilfumaraat of voor één van de hulpstoffen. Waarschuwingen en voorzorgen: Het wordt aanbevolen de nierfunctie (creatinineklaring en serumfosfaat) te berekenen voordat wordt begonnen met de behandeling met Viread. Het eerste jaar behandeling moet de nierfunctie iedere vier weken gecontroleerd en daarna elke drie maanden. Bij patiënten met het risico op nierfunctiestoornis, dient overwogen te worden om de nierfunctie vaker te controleren.Indien bij patiënten, het serumfosfaat gehalte < 1,5 mg/dl (0,48 mmol/l) is of de creatinineklaring < 50 ml/min afgenomen is, moet de nierfunctie binnen één week opnieuw beoordeeld worden, inclusief metingen van glucose- en kaliumgehalted in het bloed an van het glucosegehalte in de urine. Bij patiënten met een afname van het serum fosfaatgehalte naar < 1,0 mg/dl (0,32 mmol/l) of een afname van het creatinineklaring naar <50 ml/min ,dient het onderbreken van de behandeling met Viread overwogen te worden. Bij patiënten met milde tot matige nierinsufficiëntie, moeten de mogelijke voordelen van behandeling worden afgenomen tegen de mogelijke risico’s. Indien gelijktijdig gebruik van Viread en nefrotoxische middelen, of van Viread en geneesmiddelen met hetzelfde renale transportsysteem (hOAT1 en 3 of MRP4 ) onvermijdelijk is, dient de renale functie wekelijks gecontroleerd te worden. Om het risico van lactaatacidose te minimaliseren bij toediening van nucleoside-analogen in combinatie met Viread moeten de patiënten nauwgezet worden gevolgd. Bij gelijktijdig gebruik van Viread en didanosine moet nauwgezet gecontroleerd worden op bijwerkingen van didanosine. Bij patiënten die voor chronish hepatisB behandeld worden, moet voorzichtigheid en controle geboden worden, voor tekenen van exacerbaties van hepatitis, in het bijzonderlijk na het stoppen van de behandeling. Indien geschikt, kan hervatting van de behandeling gerechtvaardigd zijn. Viread bevat lactose. Daarom moet Viread niet gebruikt worden bij patiënten met galactose intolerantie, Lapp lactase-deficiëntie of glucose-galactose malabsortie. Zwangerschap: Een matige hoeveelheid gegevens over zwangere vrouwen (tussen 300 en 1.000 zwangerschapsuitkomsten) duidt erop dat tenofovirdiso proxilfumaraat niet tot afwijkingen leidt of foetaal/neontaal toxisch is. De resultaten van dieronderzoek duiden niet op reproductietoxiciteit (zie rubriek 5.3). Het gebruik van tenofovirdisoproxilfumaraat tijdens de zwangerschap kan zo nodig worden overwogen. Bijwerkingen: De meest gerapporteerde, zeer vaak (≥ 1/10) bijwerkingen zijn: hypofosfatemie, duizeligheid, diarree, braken, misselijkheid, uitslag, asthenie. Vaak (≥ 1/100, < 1/10) werden de volgende bijwerkingen waargenomen: hoofdpijn, abdominale pijn, opgezette buik, flatulentie, verhoogde transaminasen, vermoeidheid; Soms (≥ 1/1.000, < 1/100): hypokaliëmie, pancreatitis, rabdomyolyse, spierzwakte, verhoogd creatinine; Zelden(≥ 1/10.000, < 1/1.000): lactaatacidose, hepatische steatose, hepatitis, angio-oedeem, osteomalacie (die zich manifesteert als botpijn en zelden bijdraagt aan het ontstaan van fracturen), myopathie, acuut nierfalen, nierfalen, acute tubulaire necrose, proximale niertubulopathie (waaronder syndroom van Fanconi), nefritis (waaronder acute interstitiële nefritis), nefrogene diabetes insipidus. Deze bijwerking kan optreden als gevolg van proximale niertubulopathie. Er wordt vanuit gegaan dat dit bij afwezigheid van deze aandoening niet in een oorzakelijk verband staat met tenofovirdisoproxilfumaraat. Verpakking: Doos met 1 of 3 flacons met 30 filmomhuldetabletten. Afleverstatus: UR. Vergoeding: volledige vergoeding. Prijs: zie Z-index. Registratiehouder: Gilead Sciences International Limited, Cambridge CB21 6GT, Verenigd Koninkrijk. Bestudeer de samenvatting van productkenmerken alvorens Viread voor te schrijven in het bijzonder vanwege dosering, bijwerkingen, waarschuwingen en voorzorgen bij gebruik, en interacties. Neem voor meer inlichtingen contact op met de lokale vertegenwoordiger: Gilead Sciences Netherlands BV, WTC, Toren D, 7e Verdieping, Strawinskylaan 779, 1077 XX Amsterdam.
De volledige informatie kunt u aanvragen bij Gilead Sciences.
Referenties 1. VIREAD, summary of Product Characteristics, november 2012. 2. Marcellin et al. AASLD 2012, Poster #374. 3. Marcellin et al. Regression of cirrhosis during treatment with tenofovir disoproxil fumarate for chronic hepatits B: a 5-year open-label follow-up study, Lancet (in press).
174/NL/13-01/PM/1014
Promotiedatum: 21 november 2013
universiteit utrecht
Promotor: prof. p.d. siersema
prof. a.i.h. hoepelman
Co-promotor:dr. k.j. van erpecum
dr. j.e. arends
In dit proefschrift worden studies
beschreven die zich richten op het
voorspellen van de respons en bijwer-
kingen van antivirale behandeling van
chronische hepatitis C (CHC). Com-
binatietherapie met PEG-interferon en
ribavirine is bij 50-80% van de patiënten
succesvol en gaat tevens gepaard met
forse bijwerkingen. In dit proefschrift
tonen we aan dat steady-state ribavi-
rineconcentratie een onafhankelijke
voorspeller is van therapierespons en
dat ribavirine-afhankelijke factoren be-
langrijker voorspellers van non-respons
zijn dan PEG-interferon-gerelateerde
factoren (hoofdstuk 2). Tevens toonden
wij aan dat ribavirineconcentraties in de
vroege fase van antivirale behandeling
gebruikt kunnen worden om thera-
peutische steady-state concentraties te
voorspellen, zodat het mogelijk wordt
om tijdig dosisaanpassingen te doen met
potentiële gevolgen voor therapieres-
pons (hoofdstuk 3). Ook beschreven wij
dat het ferritine gehalte voor aanvang
van antivirale behandeling geen onaf-
hankelijke voorspeller van therapieres-
pons lijkt te zijn (hoofdstuk 4). Verder
toonden wij aan dat de endogene EPO-
productie bij CHC patiënten tijdens an-
tivirale therapie suboptimale respons is
in vergelijking met de normale humane
respons op anemie, een bevinding die
de toediening van EPO tijdens antivirale
behandeling ondersteunt (hoofdstuk 5).
In hoofdstuk 6 beschreven wij de kosten
die gepaard gaan met PEG-interferon
en ribavirine behandeling, op basis van
de databases van 2 grote Nederlandse
verzekeringsmaatschappijen. Verder
lieten wij in hoofdstuk 7 door middel
van een systematische review zien dat
therapieontrouw bij antivirale behande-
ling van zowel chronische hepatitis B als
C geen frequent fenomeen lijkt te zijn,
maar dat therapietrouw wel geassoci-
eerd was met een verhoogd risico op
falen van de behandeling. Vervolgens
beschreven wij in hoofdstuk 8 dat een
speciaal medicijndoosje met SMS herin-
neringen geen effect had therapietrouw,
ribavirine dalspiegels of virologische
respons van CHC patiënten tijdens
antivirale therapie. Tenslotte beschreven
wij dat 70% van de chronische hepatitis
B patiënten in onze prospectieve multi-
center studie een goede therapietrouw
had tijdens behandeling met entecavir,
waarbij jongere leeftijd en een negatieve
attitude ten opzichte van medicatie was
geassocieerd met therapieontrouw. Zelfs
in het geval van therapieontrouw leek de
virologische respons voldoende te zijn
(hoofdstuk 9).
De studies beschreven in dit proefschrift
kunnen gebruikt worden om de respons
op antivirale behandeling van CHC te
verbeteren. Ook met de introductie van
nieuwe antivirale middelen in de nabije
toekomst zal ribavirine immers een
hoeksteen blijven van de behandeling.
SAMENVATTING PROEFSCHRIFT LOTTE G. VAN VLERKEN
‘Antiviral treatment for chronic hepatitis C infection. Prediction of treatment response and side effects’
Vervolg van pagina 21.

DAAR HEB JE NU WAT AAN
Nieuwe behandelingen in HCVKan ik daar op wachten?
We verwachten straks weer een stap voorwaarts als de nieuwe generatie DAA’s er is. De eerste klinische studies zijn gepubli-ceerd. Kortom, een nieuwe behandeloptie. Tot het zover is heeft u bij iedere individuele patiënt dilemma’s. Zo heeft een patiënt in goede conditie een betere prognose. Maar is de patiënt gemotiveerd? Is er een zwangerschapswens? Et cetera. Daarover zijn we graag met u in gesprek. Zodat uiteindelijk de patiënt er beter van wordt. Nu nog met peginterferon, want daar heb je nu wat aan.
JaNee
JaNee
JaNee
JaNee
Zie
voo
r p
rod
uct i
nfo
rmat
ie e
lder
s in
dez
e ui
tgav
e.
P
EG13
1001
0D
e af
geb
eeld
e p
erso
nen
zijn
nie
t d
e p
erso
nen
waa
rove
r g
esp
roke
n w
ord
t.
2013-10-30 Pegasys HCV advertenties_A4.indd 1 30-10-13 12:26