Interuniversitaire cursus: Bijzondere bekwaamheid in de ... zorgaanbod/UROL_Mictie.… · 9...
Transcript of Interuniversitaire cursus: Bijzondere bekwaamheid in de ... zorgaanbod/UROL_Mictie.… · 9...

Interuniversitaire cursus:
Bijzondere bekwaamheid in de pelvische
reëducatie en perinatale kinesitherapie.
Thesis: Mictie problemen
Guffens Katrien
Jonniaux Marieke
Mertens Elien
Weynants Marlies
Wynants Mia
Promotor: Prof. Dr. Vermandel Alexandra
Promotiejaar: 2016-2017


Inhoudsopgave
Mictie problemen 7
1. Wat is normale mictie? 7
1.1. Definitie 7
1.2. Anatomie 8
1.2.1. Hogere urinewegen 8
1.2.2. Lagere urinewegen 8
1.2.3. Musculair 9
1.2.4. Neurogeen 10
1.2.4.1. Autonoom 11
1.2.4.2. Somatisch 12
1.3. Fysiologie 12
1.3.1. Adequate vullingsfase 12
1.3.1.1. Urineproductie 12
1.3.1.1.1. Overdag 12
1.3.1.1.2. ’s Nachts 12
1.3.1.2. Compliantie (rekbaarheid) 12
1.3.1.3. Lage intravesicale druk 13
1.3.1.4. Normaal blaasgevoel 13
1.3.1.5. Gesloten uitgang met stijging intra-abdominale druk 13
1.3.1.6. Afwezigheid onwillekeurige blaascontracties 14
1.3.1.7. Blaasvulling 14
1.3.2. Overgang naar mictie 14
1.3.3. Ledigingsfase 15
1.3.3.1. Beschrijven normaal plas patroon 15
1.3.3.2. Flow rate 15
1.3.3.3. Volledige lediging 15
1.3.4. Post-mictie fase 15
1.3.4.1. Residu 15

1.3.4.2. Verschillen man vs. vrouw, volwassenen vs. oudere (>65 jaar) en volwassenen vs.
kinderen 16
2. Afwijkingen van normale mictie 16
2.1. Definities 16
2.2. Oorzaken 17
2.2.1. Disfunctionele mictie 17
2.2.2. Mictie disfunctie 18
2.2.2.1. Persmictie door verminderde detrusoractiviteit 18
2.2.2.2. Persmictie door obstructie 18
2.2.2.3. Andere 19
2.2.2.4. Objectiveren van de oorzaak 19
2.2.3. Conclusie 19
2.3. Klinisch 19
2.3.1. Vulling stoornissen 19
2.3.2. Lediging stoornissen 19
2.3.2.1. Objectief te meten 19
2.3.2.2. Subjectieve klachten 20
2.4. Risico’s 21
2.5. Beïnvloedende factoren 22
2.5.1. Gedragsproblemen en psychiatrische stoornissen 22
2.5.2. Intellectuele functies 22
2.5.3. Constipatie 22
2.5.4. Toilethouding 23
2.5.5. Prolaps 23
2.5.6. Stress 23
2.6. Prevalentie 23
2.6.1. Kinderen 23
2.6.2. Volwassenen 23
2.6.3. Ouderen (>65j) 24
2.7. Diagnose 24

2.7.1. Anamnese 25
2.7.1.1. Plasdagboek 25
2.7.1.2. Stoelgang dagboek 25
2.7.1.3. Vragenlijsten 25
2.7.2. Klinisch onderzoek 26
2.7.3. Niet-invasief urodynamisch onderzoek: uroflowmetrie en EMG van de bekkenbodem 26
2.7.4. Verdere onderzoeken 28
2.8. Management 28
2.8.1. Educatie 28
2.8.2. Plasdisfunctie 30
2.8.2.1. Urotherapie 30
2.8.2.1.1. Levensstijlverandering 30
2.8.2.1.2. Klokplassen 30
2.8.2.1.3. Ledigingsmanoeuvers 31
2.8.3. Disfunctionele mictie 31
2.8.3.1. Urotherapie 31
2.8.3.1.1. Informatie en educatie over de normale functie van urinewegen 31
2.8.3.1.2. Gedragsverandering 31
2.8.3.1.3. Levensstijladvies 33
2.8.3.1.4. Plasschema 33
2.8.3.2. Bekkenbodemreëducatie 33
2.8.3.3. Biofeedback 35
2.8.3.4. Elektrostimulatie 35
2.8.3.5. Sacrale neurostimulatie 35
2.8.3.6. Psychologische- en omgevingsfactoren 35
2.8.3.7. Intermittente zelf-katheterisatie 35
3.Bronnen 36
4. Afkortingen 41

5. Bijlagen 42
5.1. Figuren 42
5.2. Documenten 49
5.2.1.Varia Tips 49
5.2.2.Praktische handleiding 50
5.2.3.Meetinstrumenten 55

7
Mictie problemen
1. Wat is normale mictie?
1.1. Definitie
De “International Continence Society” (ICS) definieert normale mictie als een vrijwillig geïnitieerde continue
detrusorcontractie die leidt tot een complete blaaslediging in een normale tijdspanne met de afwezigheid van
obstructie [1].
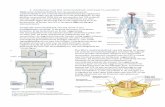
Mictie of urineren betekent letterlijk: het lozen van urine. Een normale mictie vraagt een synergistische reactie
tussen de m. detrusor en de externe urethrale sfincter. Dit wordt bereikt door een initiële vermindering van de
intra-urethrale druk door relaxatie van de externe urethrale sfincter en de bekkenbodemspieren. Deze wordt
meestal gevolgd door een continue detrusorcontractie die leidt tot complete blaaslediging in een normale
tijdspanne. Dit gebeurt in een sterke, continue flow. Normaal plassen doet geen pijn, er is geen obstructie en er
mag geen bloed bij de urine zitten [2-5].
Fig.1: Een normale mictie [6]

8
1.2. Anatomie
1.2.1. Hogere urinewegen
De hogere urinewegen bestaan uit de nieren en de ureters. De nieren zijn boonvormige organen gelegen in het
retroperineum, links en rechts van de wervelkolom t.h. T12-L3 (Fig. 2; zie bijlage). Het gewicht van de nieren
is in verhouding met het gewicht van het eigen lichaam. De twee nieren representeren 1/80 van het totale
lichaamsgewicht bij een pasgeborene en 1/240 bij een volwassen persoon.
De nieren hebben een filterfunctie, per dag wordt door beide nieren 180 liter bloed gezuiverd. Water, zout en
afvalstoffen worden via de twee ureters naar beneden gestuwd.
De ureters monden achter en van onderuit in de blaas, wordt de vesico-urethrale junctie genoemd (Fig. 3; zie
bijlage). De ureters zijn ongeveer 25 tot 30 cm lang en zes millimeter breed. Ze lopen schuin door de
blaaswand en worden dichtgedrukt wanneer de blaas samentrekt. Op die manier kan de urine vanuit de blaas
niet terugvloeien in de ureters [7, 8].
1.2.2. Lagere urinewegen
De blaas is een hol, musculair (m. Detrusor) orgaan, gelegen in het bekken onder het peritoneum of buikvlies,
achter het os pubis. De vorm en positie van de blaas worden beïnvloed door leeftijd, geslacht, en graad van
blaasvulling. Bij kinderen is de blaas conisch en komt boven het os pubis uit. Bij volwassenen is ze
komvormig en dieper in het bekken gelegen. In lege toestand is de blaas afgeplat, is ze gevuld, dan komt ze
boven het schaambeen uit.
Een gezonde blaas is gevoelig voor zowel urine volume als voor de chemische compositie. In de dorsale
blaaswand bevindt zich het trigonum, een driehoekig gebied dat bovenaan begrensd wordt door beide ureter
mondingen en onderaan door de urethra-opening. De blaashals vormt de verbinding tussen de blaas en de
urethra.
De urethra of urinebuis vormt de verbinding tussen de blaas en de buitenwereld. De lengte varieert bij de
vrouw van 2,5 tot 5 cm met een doorsnede van ongeveer 6 mm. De urethra loopt naar voren en caudaalwaarts
en mondt uit tussen de kleine schaamlippen. Bij de man is de urethra veel langer (15-29 cm), deze is ingedeeld
in de posterieure en de anterieure urethra. De posterieure urethra is de prostaat-urethra, deze loopt van de
blaashals tot aan en door het diafragma urogenitale. Dit deel is omgeven door de prostaat en lager door de
externe urethrale sfincter. De anterieure urethra is de caverneuze urethra, ze loopt door de penis om uit te
monden aan de top of de meatus van de penis.
Vanaf de leeftijd van vijf jaar staat de willekeurige controle van de blaas op punt. De ontwikkeling van
continentie en vrijwillige mictie vraagt rijping van het zenuwstelsel en een leerproces over toiletgedrag. De
blaas kent een hele evolutie gedurende de levensjaren. Er is nog veel onbekendheid over deze evolutie. De
blaaslediging van een baby is reflexmatig maar ondergaat een verandering naar vrijwillige controle als het

9
centraal zenuwstelsel controle krijgt over het urinestelsel. Dit is meestal afgerond op de leeftijd van vijf jaar.
Terwijl het volume aanzienlijk toeneemt met de leeftijd blijft het maximum debiet min of meer stabiel [7-9].
1.2.3. Musculair
Als de meest caudale grens van de abdominopelvische holte fungeert de bekkenbodem als het fundament van
het menselijk lichaam. Het perineum of de bekkenbodem bestaat uit verschillende lagen dwarsgestreepte
spieren, uit banden, fascia en pezen. Het gebied is begrensd door de schaambeenderen (os pubis) vooraan, het
staartbeen (os coccyx) achteraan en de zitbeenknobbels (tubera ischiadica) aan beide zijden. Alle spieren zijn
direct of indirect op deze beenderige bekkenring aangehecht, met uitzondering van de dwarsgestreepte
sfincters.
De dwarsgestreepte bekkenbodemspieren hebben een steunfunctie, een seksuele functie en een sluitfunctie.
Deze sluitfunctie is van belang bij continentie. Al deze spieren hebben een invloed op elkaar en moeten samen
in een goede conditie zijn. Klinisch gezien werken deze spieren als een functioneel geheel. Hiermee bedoelen
we dat deze spieren normaal simultaan contraheren, maar dat de kwaliteit en de bijdrage van de verschillende
spieren verschilt afhankelijk van de taak.
In onderstaande opsomming geven we aan welke functies van belang zijn voor normale mictie [7, 9, 10].
Oppervlakkige laag
● M. Sfincter ani externus, bij aanspannen van deze spier is het mogelijk om stoelgang op te houden.
Verder in dit werk wordt duidelijk dat mictie en defecatie nauw samenhangen.
● M. Bulbospongiosus, deze spier zorgt er bij de man voor dat de laatste druppels urine naar buiten geperst
worden.
● M. Ischiocavernosus
● M. Transversus perineum superficialis, deze spier stabiliseert het centrum tendineum. Door deze
stabiliteit kunnen de bekkenbodemspieren hun functie goed uitvoeren.
Middelste laag
● M. Transversus perineum profundus, deze spier heeft een steunfunctie, maar sluit ook het middelste
urethrale deel en de vaginale opening.
● M. Sfincter urethrae externus, deze spier omgeeft de urethra over een lengte van enkele centimeters. Ze
sluit de urethra en is dus belangrijk bij de mictie en de continentie.
● M. Sfincter ani, het diepe deel van deze spier behoort tot de middelste laag.

10
Diepe laag
Deze spieren vormen een kom die het bekken onderaan afsluit. De spieren hebben een belangrijke
ondersteunende functie en dragen bij tot de continentie.
● M. Levator ani: Deze spier is de primaire musculaire ondersteuning van de pelvische organen. Ze bestaat
uit drie delen:
M. Puborectalis
M. Iliococcygeus
M. Pubococcygeus
● M. Coccygeus
Fig. 4: Anatomische structuren van het perineum [10] Fig.5: De musculaire ondersteuning van het bekken [9]
1.2.4. Neurogeen
De blaas is uniek onder de autonoom geïnnerveerde organen door de hoge graad van vrijwillige controle die
dit lichaamsdeel heeft op zijn functie. Hierdoor is de bezenuwing van blaas, urethra en bekkenbodemspieren
complex. Deze bezenuwing moet een bepaalde rijping doormaken vooraleer ze volgroeid is. Daarom verschilt
een baby blaas van een normale blaas.
Verschillende centra in de pons (hersenstam) coördineren de mictie. Maar de hypothalamus en andere delen
van de hersenen, waaronder de frontale cortex, staan in voor de timing van het starten van de mictie. Ze
inhiberen de mictiereflex totdat dit sociaal acceptabel is.
Het pontien mictiecentrum (PMC) coördineert de activiteit van de motorneuronen van de blaas en de urethrale
sfincter. De centrale controle van de mictie functie is georganiseerd als een aan-uit knop die een reciproke
relatie behoud tussen de blaas en de outlet. Drie soorten zenuwen innerveren de blaas: sacrale
parasympatische, thoracolumbale sympathische en somatische zenuwen [7, 9].

11
Fig. 6: De invloed van de hersenen op de blaas [10]
1.2.4.1. Autonoom
Het autonoom zenuwstelsel bestaat uit de parasympatische sacrale en de sympathische thoracolumbale
zenuwen. Ze bevatten zowel efferente als afferente axonen die hun oorsprong hebben op thoracolumbale of
sacrale spinale niveaus.
De thoracolumbale sympathische bezenuwing, met hun oorsprong op niveaus T10-L2, vormen samen de n.
hypogastricus. Deze is met name belangrijk tijdens de vullingsfase. Bij directe sympathische stimulatie zullen
de blaashals en de proximale urethra (gladde spieren) gesloten blijven, terwijl het blaaslichaam gerelaxeerd is.
De parasympatische zenuwen, gelokaliseerd ter hoogte van zenuwwortels S2-S4, verenigen zich in de n.
pelvicus en zorgen voor een contractie van de m. detrusor.
De afferente bezenuwing begint bij de sensorische zenuwuiteinden in de blaaswand, welke gevoelig
of getriggerd worden door uitrekking[7, 9, 10].
Fig. 7: De invloed van de hersenen op de blaas [10]

12
1.2.4.2. Somatisch
Naast het autonome zenuwstelsel is er ook belangrijke somatische bezenuwing. De somatische efferente
zenuwen laten de externe urethrale sfincter contraheren en onderdrukken de activiteit van de m. detrusor.
Deze somatische bezenuwing is van belang om de mictiereflex uit te stellen tot een sociaal acceptabel
moment. De gestreepte spieren van de bekkenbodem, waaronder beide sluitspieren, worden bezenuwd door de
n. pudendus [7, 9, 10].
1.3. Fysiologie
1.3.1. Adequate vullingsfase
1.3.1.1. Urineproductie
1.3.1.1.1. Overdag
De blaasinhoud van een volwassen persoon bedraagt 350 tot 450 ml voor de mannen en 400 tot 500 ml voor
de vrouwen. De blaasvulling gebeurt, afhankelijk van vochtinname en diurese, aan een tempo van 5 tot 10 ml
per minuut.
Kinderen hebben een veel kleiner blaasvolume. De blaasinhoud wordt dan berekend met de volgende formule:
(30 + (leeftijd*30ml)), ook de formule ((lft+1) x 30ml) wordt gebruikt. De blaascapaciteit van een kind neemt
per jaar ongeveer met 30ml toe, rond de leeftijd van 12 tot 14 jaar bereikt deze de normale capaciteit van 450
ml [7, 11]. De plasfrequentie is variabel en wordt beïnvloed door leeftijd, diurese en vochtintake. Deze
frequentie wordt volgens ICS beschreven als normaal, zolang het voor de persoon in kwestie geen probleem
vormt. De meeste epidemiologische studies suggereren dat de normale mictie frequentie ongeveer acht keer
per dag is. De “International Children’s Continence Society” (ICCS) bepaalt wel een standaard voor kinderen.
Een frequentie van ≥ acht maal per dag wordt als verhoogd aangenomen en drie of minder keer per dag als
verminderd [3, 7, 9, 11].
1.3.1.1.2. ’s Nachts
Nachtelijke mictie wordt in de meeste artikels als niet normaal beschouwd. Volgens ICS mag de nachtelijke
mictiefrequentie één keer of minder bedragen [3]. De nachtelijke excretie verschilt tussen jongvolwassenen en
ouderen. Jongvolwassenen (21-35 jaar) zouden tussen 23.00 uur en 07.00 uur 14 ±4% van de totale
urineproductie plassen. Bij ouderen wordt dit geschat op 35 ±15% [12]. Normale nachtelijke urineproductie
wordt geacht als ≤ 20-33% van het 24 uur volume [13].
1.3.1.2. Compliantie (rekbaarheid)
De normale urineblaas is een hoog compliant elastisch orgaan en is in staat om urine op te slaan onder lage
druk. De mogelijkheid van de blaas om groter te worden in volume zonder een significant verschil in druk,
wordt de blaascompliantie genoemd [14].
Deze relatie tussen verandering in blaasvolume en verandering in detrusordruk wordt als volgt berekend:
(ΔV/ΔPdet) weergegeven in ml/cmH2O [9, 11]. De stijging in blaas druk is bij een normaal individu amper op

13
te merken wanneer er geen sprake is van onvrijwillige blaascontracties. Verschillende studies hebben
onderzoek gedaan naar normale compliantie waarden. De range tussen normaalwaarden was groot. Als
gemiddelde wordt een compliantie tussen 46 en 124 ml/cmH2O als normaal aangenomen [1].
1.3.1.3. Lage intravesicale druk
Normale detrusor functie laat vulling toe met weinig of geen drukstijging. Ook provocatie, zoals posturale
veranderingen, hoesten of niezen mogen geen onvrijwillige contracties opleveren. Elke detrusorcontractie voor
toestemming tot mictie wordt als pathologisch beschouwd.
Voor iedere detrusorcontractie tijdens mictie hangt de hoogte van de gegenereerde druk af van de mate van
weerstand aan de blaasuitgang [9].
Bij kinderen wordt een detrusordruk van minder dan 10 cmH2O als veilig beschouwd. Bij volwassenen is
bewezen dat een langdurige detrusordruk van meer dan 40 cmH2O schadelijk is voor de hogere urinewegen
[1].
1.3.1.4. Normaal blaasgevoel
Een normaal blaasgevoel kan beoordeeld worden aan de hand van drie gedefinieerde punten die tijdens de
vulling gemeten kunnen worden:
● Het eerste gevoel van blaasvulling, waarbij de bewustwording optreedt dat de blaas zich vult.
● Een eerste drang gevoel wordt gedefinieerd als een gevoel dat de blaas geledigd moet worden op een
volgend passend moment. Maar de mictie kan nog worden uitgesteld indien nodig.
● Een persisterende plasdrang zonder de angst voor verlies.
Volgens de richtlijn van ICS zijn de waarden voor normaal blaasgevoel bij gezonde volwassenen als volgt:
Eerste gevoel van vulling 170-200 ml, eerste drang gevoel ongeveer 250 ml, sterk drang gevoel rond 400 ml
met een maximale blaascapaciteit van om en bij de 480 ml. Dit is een richtlijn, de werkelijke waarden in de
“normale” populatie kan hiervan verschillen [1, 12].
1.3.1.5. Gesloten uitgang met stijging intra-abdominale druk
Vanaf 170-200 ml wordt een persoon zich progressief bewust van de blaasvulling. De urethrale druk zal verder
toenemen om urineverlies te vermijden. Dit noemen we de guarding reflex [7].
Bij continente personen zou er geen valsalva of abdominale lekpunt druk mogen zijn. Individuen met adequate
sfincterfunctie zullen geen urine verliezen bij fysiologische stijging van de abdominale druk [1].

14
1.3.1.6. Afwezigheid onwillekeurige blaascontracties
Wanneer de detrusor normaal is zijn er geen onvrijwillige blaascontracties ondanks provocatie door
activiteiten (posturele veranderingen, hoesten, stromend water horen lopen, handen wassen) [14]. Toch
worden deze onwillekeurige contracties of detrusoroveractiviteit gezien bij normale, asymptomatische
patiënten tijdens urodynamica, gemiddeld bij acht procent. Dit zou veroorzaakt kunnen worden door een
kleine beschadiging van de urethra bij het inbrengen van de katheter of het kan getriggerd worden door de
vullingssnelheid of de temperatuur van de vloeistof. De exacte oorzaak van deze onwillekeurige
blaascontracties is nog niet gekend. Hierdoor kunnen we stellen dat ook andere redenen dit in de hand kunnen
werken [1].
1.3.1.7. Blaasvulling
Tijdens de blaasvulling zorgt de parasympatische bezenuwing voor een inhibitie van de m. detrusor en de
gladde en gestreepte spieren van de urethrale sfincter worden geactiveerd om onvrijwillige blaaslediging te
voorkomen [15].
De urethrale druk is hoger dan de detrusor druk tijdens de vullingsfase [14]. Zoals eerder vermeld, bedraagt
het blaasvolume bij een volwassene tussen de 350 en 500 ml. Wanneer het volume in een normale blaas
toeneemt en de spiervezels van de m. detrusor progressief gestretched worden, is er een verhoging in de
potentiële blaaskracht geassocieerd met een contractie. Dit is het meest uitgesproken in de range van leeg tot
150-250 ml blaasvolume. Bij volumes hoger dan 400-500 ml, kan de m. detrusor overrekt geraken en de
contractiliteit kan dan terug dalen [1].
1.3.2. Overgang naar mictie [7, 11]
● Ontspannen externe urethrale sfincter (en andere bekkenbodemspieren): een normale urethrale functie
wordt gedefinieerd als een urethra die opent en continue
gerelaxeerd is, zodat de blaas onder een normale druk
geledigd kan worden.
● Wegvallen sympathische remming blaashals: de blaashals
krijgt geen prikkel meer om aan te spannen en zal dus
relaxeren.
● Wegvallen sympathische remming blaas: de blaas zal niet
meer aangestuurd worden om gerelaxeerd te blijven.
● Activatie parasympatische stimulatie blaas: de m. detrusor zal contraheren
Fig. 8: Plascurve [14]

15
1.3.3. Ledigingsfase
1.3.3.1. Beschrijven normaal plas patroon
Tijdens plassen contraheert de m. detrusor met relaxatie van de proximale urethra om het plassen te initiëren.
De manier van plassen kan gemeten worden middels een uroflow. De precieze vorm van de flow curve wordt
bepaald door de contractiliteit van de m. detrusor, de abdominale druk en de blaas outlet. Bij normale mictie is
er een sterke, continue flow. De uroflow curve is bij elk gezond persoon klokvormig en niet fluctuerend (Fig.
8). Dit is onafhankelijk van geslacht, leeftijd en geplast volume. Er vindt een complete lediging plaats in een
normale tijdspanne [1, 11, 14].
1.3.3.2. Flow rate
Een normale flow rate is >15 ml/sec. Het geplaste volume zou >150ml moeten zijn bij volwassen
personen [1, 16]. De maximale stroomsnelheid is de meest relevante variabele om blaaslediging te beoordelen
[11]. Een normale maximale stroomsnelheid varieert van 20-25 ml/sec bij vrouwen en 25-30 ml/sec bij jonge
mannen, maar bij deze laatste groep daalt dit met de leeftijd. Bij kinderen is het moeilijker om
normaalwaarden te bepalen, als grove regel wordt gesteld dat als het kwadraat van de maximale flow gelijk of
meer is dan het volume, heeft de mictie een normale maximale flow [9]. De accuraatheid van de uroflow is
afhankelijk van het geplaste volume. Voor de meest betrouwbare resultaten zou het geplast volume meer dan
50% van de maximale blaascapaciteit moeten zijn. Zoals eerder vernoemd, is deze bij kinderen afhankelijk van
de leeftijd. Ook is het aan te raden om de metingen meermaals uit te voeren om de accuraatheid,
betrouwbaarheid en interpretatie van de test te verbeteren [1, 9, 11].
1.3.3.3. Volledige lediging
Volgens de definitie moet de blaas volledig geledigd zijn om van een normale mictie te spreken [1].
1.3.4. Post-mictie fase
1.3.4.1. Residu
Volgens het ICS is er geen evidentie over een maximaal toelaatbaar postmictioneel residu.[1]. Toch wordt een
blaasresidu van minder dan 10% van de blaascapaciteit als grens toegelaten om van normale blaaslediging te
spreken [11].
Bij kinderen tussen vier en zes jaar wordt een verhoogd post-mictioneel residu (PMR) beschreven als een
eenmalig residu van ≻30ml of ≻21% van de te verwachte blaascapaciteit of een herhaaldelijk residu van
≻20ml of ≻10% van de verwachte blaascapaciteit. Bij kinderen tussen zeven en twaalf jaar is dit eenmalig
≻20ml of 15% of herhaaldelijk ≻10ml of zes procent. Om een PMR correct te meten moet voldaan zijn aan
volgende voorwaarden: de blaas mag niet <50% of >115% gevuld zijn en het residu moet onmiddellijk na
plassen gemeten worden (<5 min) [11].

16
1.3.4.2. Verschillen man vs. vrouw, volwassenen vs. oudere (>65 jaar) en volwassenen vs. kinderen
Bij het ouder worden, veranderen ook de blaas en de bekkenbodemspieren. Zo zien we een verminderde blaas
gevoeligheid en een verminderde contractiliteit tijdens plassen. Ouderen hebben ook een verminderde
spiertonus in de bekkenbodemspieren en een groter residueel volume. Ook komt detrusoroveractiviteit vaker
voor bij ouderen. Hoewel er voor de blaas en zijn functie leeftijd geassocieerde veranderingen plaatsvinden,
kunnen deze effecten makkelijk en minimaal gecompenseerd worden door aangepaste blaas gewoonten [3].
Zoals eerder vermeld, is er ook een verschil in nachtelijke excretie tussen jong volwassenen die ’s nachts
minder urine produceren en ouderen met hogere volumes [12].
Volgens Rovner & Koski verschilt de blaas gevoeligheid niet alleen tussen jongvolwassenen en ouderen,
maar ook tussen mannen en vrouwen. De drang gevoelens bij vrouwen zijn significant lager dan bij mannen
[1]. Tussen 40 – 50 jaar neemt de Qmax bij mannen af tot ongeveer 60 % van de vrouwelijke Qmax,
detrusordrukken en residueel volume nemen toe tot hogere waarden dan bij vrouwen [17].
Ook tussen volwassenen en kinderen zitten grote verschillen. Bij een pasgeborene bijvoorbeeld zal de blaas
vanaf een zekere vullingsgraad (20-50 ml) spontaan samentrekken. Progressief wordt dit meer en meer
gecontroleerd door de hersenen en zal het kind rond de leeftijd van twee tot drie jaar bewuste controle
verwerven over de mictiecyclus [7]. Ook de blaas compliantie verandert als de blaas groeit, en verandert dus
met de leeftijd. Hierover zijn er voor kinderen geen normaalwaarden. Als vuistregel geldt dat een druk van
minder dan 10 cmH2O aan het einde van de vulling als normaal beschouwd kan worden [1, 9].
Kinderen en baby’s zijn niet in staat om de verschillende fasen van blaasvulling aan te geven. Bij oudere
kinderen is het meestal wel mogelijk om ‘sterke drang’ aan te geven [9].
In studies bij gezonde kinderen en zuigelingen is aangetoond dat deze niet elke keer hun blaas volledig
ledigen. Ze doen dit wel minimaal één keer tijdens een vier uur durende observatie periode [11].
De waarden van maximale detrusordruk en detrusordruk bij maximale flow zijn verschillend tussen mannen en
vrouwen en ook tussen volwassenen, kinderen en tussen oudere en jongere kinderen [11].
2. Afwijkingen van normale mictie
2.1. Definities
Een afwijking van het normale plaspatroon kan als disfunctionele mictie omschreven worden. Dit wordt op
verschillende manieren gedefinieerd.
De Nederlandse vereniging voor urologie definieert disfunctionele mictie bij kinderen als: “een
gefractioneerde (onderbroken) of staccato uroflow door onvrijwillige activiteit van de peri urethrale gladde of
dwarsgestreepte spieren zonder een aantoonbare neurologische aandoening” [5].
ICCS definieert disfunctionele mictie als volgt: “ herhaaldelijke, intermittente contracties van de urethrale
sfincter of de bekkenbodemspieren tijdens mictie bij neurologisch intacte personen. Meervoudige EMG
uroflowmetrie metingen of video-urodynamica tonen een staccato patroon met of zonder onderbroken
flow”[5]. De recentste toevoegingen aan deze definitie zijn de bijdragen van de levator ani spieren aan de
disfunctionele mictie en implementering van een niet onderbroken patroon [4].

17
De beide definities verwijzen steeds naar een onderbroken en/of fluctuerende flow veroorzaakt door
onvrijwillige intermitterende contracties en dus verhoogde EMG activiteit van de peri urethrale en levator ani
spieren tijdens plassen bij neurologisch normale personen [2-4, 7, 9].
Er wordt dus een duidelijk onderscheid gemaakt met detrusor-sfincter dyssynergie (DSD). Dit wordt enkel
vastgesteld in aanwezigheid van een neurologische aandoening en beschreven als een contractie van de
urethrale sfincter tegelijk met de detrusor.
Er is geen sprake van dyssynergie wanneer het gaat om bewust, actief ophouden tijdens urineverlies
(ongewilde mictie) of tijdens (gewilde) mictie.
Wanneer we enkel bovenstaande definities van disfunctionele mictie in rekening nemen, valt een zwakke of
trage, continue straal hier buiten; zoals Sinha ook aanhaalde in zijn onderzoek [18]. Dit plas patroon is
nochtans ook afwijkend van het normale.
Een “abnormaal trage of onvolledige mictie, gebaseerd op symptomen en urodynamisch onderzoek” wordt
door de ICS en de International Urogynaecological Society (IUGA) als ‘voiding dysfunction’ (mictie
disfunctie) gedefinieerd [1].
Beide definities beschrijven een afwijking in het normale plaspatroon, gediagnosticeerd op basis van technisch
onderzoek, maar komen niet overeen op vlak van afwijkende parameters. Dit is een eerste reden voor
verwarring binnen het onderzoeksdomein.
Een tweede reden hiervoor is dat, ondanks de aanwezigheid van duidelijke definities, de beide termen in de
literatuur vaak foutief gebruikt worden als overkoepelende term voor zowel vullings- als lediging stoornissen,
voornamelijk bij kinderen [4, 19]. Zowel disfunctionele mictie als mictie disfunctie zijn problemen van de
ledigingsfase van de blaas. Het gebruiken van deze term voor vulling stoornissen is dan ook foutief. Dit
inconsistent gebruik bemoeilijkt literatuuronderzoek en vergelijking van data uit verschillende studies.
In deze paper zullen wij enkel de focus leggen op problemen van de ledigingsfase en hierbij een duidelijk
onderscheid trachten te maken tussen disfunctionele mictie en mictie disfunctie.
2.2. Oorzaken
2.2.1. Disfunctionele mictie
Over de oorzaak van disfunctionele mictie bestaan verschillende theorieën, maar voorlopig is hierover nog
geen sluitende evidentie [20]. Zo is er bijvoorbeeld sprake van disfunctionele mictie als geleerd gedrag na een
inflammatie, infectie, trauma of irritatie in de kindertijd of het volwassen leven, of door gebrek aan aanleren
van juist toiletgedrag, nl. ontspanning van de bekkenbodemspieren tijdens mictie [18].
In het geval van een infectie, maar ook bij detrusoroveractiviteit, zal het sterke drang gevoel kunnen leiden tot
overreactie van de externe urethrale sfincter om de detrusorcontractie te inhiberen.
Ook de invloed van emotionele en gedragsfactoren op het ontstaan van disfunctionele mictie wordt
beschreven.

18
Perioden van stress en zindelijkheidstraining zouden een oorzaak kunnen zijn voor het ontstaan van een
disfunctioneel plaspatroon bij kinderen [19]. Te vroege (<24 maanden) of te late (>36 maanden)
zindelijkheidstraining zou gelinkt zijn met disfunctionele mictie, al wordt er hierbij enkel rekening gehouden
met de aanwezigheid van urgentie, frequentie en incontinentie [21]. De methode van zindelijkheidstraining,
ouder gericht of kind gericht, heeft echter geen significante invloed op het ontstaan van disfunctionele mictie
tijdens deze periode [2, 22].
Enkele onderzoekers verwijzen naar het onvoldoende uitrijpen van de bewuste controle over mictie als
oorzaak van disfunctionele mictie. Hierdoor blijft de mictie onder controle van het PMC, wat onvoldoende
relaxatie van de urethrale sfincter kan verklaren [18]. Hierbij kan de vraag gesteld worden of er dan gesproken
kan worden over een niet neurologisch probleem.
Erfelijke en omgevingsfactoren, evenals constipatie problematiek, zouden de disfunctionele mictie ook
beïnvloeden en triggeren [18].
2.2.2. Mictie disfunctie
2.2.2.1. Persmictie door verminderde detrusoractiviteit
Mictie disfunctie kan ontstaan als resultaat van abdominaal persen als compensatie voor een acontractiele
detrusor of detrusor onderactiviteit [23]. Verminderde detrusor contractiliteit kan ontstaan door medicatie,
overdistensie schade, chronische urinaire retentie, veroudering, postoperatief, postpartum, ...[7, 16]. Deze
oorzaken van disfunctie kunnen zowel tijdelijk als permanent zijn.
2.2.2.2. Persmictie door obstructie
Mictiedisfunctie kan ook ontstaan als resultaat van abdominaal persen ter compensatie van een obstructie [23].
Soorten obstructies worden als volgt ingedeeld: anatomisch (urogenitale prolaps, urethrastrictuur, urethraal
trauma, meatale afwijking, tumor, blaasdivertikel, prostaathypertrofie…), iatrogeen (anti-incontinentie
chirurgie en mesh) of functioneel (hypertonie van de bekkenbodemmusculatuur, blaashalsdisfunctie) [4, 24].
Wat de iatrogene obstructie betreft, worden plasmoeilijkheden na anti-incontinentie chirurgie en mesh-operatie
in 2,8-39 % van de gevallen gerapporteerd [4]. De meeste studies beoordelen echter het plassen in de vroege
postoperatieve fase en baseren zich hier enkel op het PMR en de onmogelijkheid om te plassen [4, 24]. In een
studie van Chung et al. werden plasmoeilijkheden opgevolgd tot één maand postoperatief. Bij de
proefpersonen met plasmoeilijkheden verdwenen de klachten binnen de tien dagen postoperatief spontaan of
mits conservatieve behandeling [25]. Sweeney et al. stellen dat, indien de klachten echter na vier weken
blijven bestaan, de kans op spontaan herstel minimaal is [26].

19
2.2.2.3. Andere
Als andere mogelijke oorzaken voor mictie disfunctie worden nog genoemd: Fowler syndroom, idiopathische
detrusor onderactiviteit, pseudo-chronische darmobstructie, blaaspijnsyndroom, hypercalciurie, constipatie…
[2, 18, 21].
2.2.2.4. Objectiveren van de oorzaak
De oorzaak van mictie disfunctie kan niet zuiver door een UDO vastgesteld worden. [2] Tijdens een UDO
wordt in verschillende gevallen een Qmax gemeten < 15 ml/sec. Een EMG meting is noodzakelijk om verder
onderscheid te maken tussen de verschillende oorzaken. [4]. Een UDO wordt echter in de meeste zittingen
reeds gecombineerd met een EMG meting. Bij vrouwen met mictie disfunctie zou een obstructie vaker
voorkomen dan een onderactiviteit [2].
2.2.3. Conclusie
Het lijkt aannemelijk om te stellen dat het ontstaan van afwijkend plassen multifactorieel is en aldus ook zo
benaderd moet worden tijdens de behandeling.
2.3. Klinisch
Disfunctionele mictie en mictie disfunctie kunnen op elke leeftijd voorkomen en kennen een zeer uiteenlopend
klachtenpatroon. Klachten kunnen subtiel tot zeer ernstig zijn en een impact hebben op de kwaliteit van leven.
Kinderen presenteren zich vaak met klachten van de vullingsfase (urinaire incontinentie, zowel overdag als ‘s
nachts) [18, 27].
Bij volwassenen geldt een grote overlap in zowel vullings- als ledigingsklachten. Volwassenen vrouwen
zouden zich volgens enkele studies meer met vullingsfase stoornissen presenteren, terwijl bij mannen over het
algemeen meer stoornissen van de ledigingsfase voorkomen [9, 16, 18].
2.3.1. Vulling stoornissen
Vulling stoornissen komen vaak voor bij patiënten met disfunctionele mictie en kunnen het enige symptoom
zijn [28]. Afhankelijk van de onderliggende oorzaak en de reactie van de blaas hierop, kunnen zowel
incontinentie (enuresis, urge-incontinentie en overloopincontinentie) als urgentie en frequentie voorkomen
[18]. Percentages voor frequentie en urgentie kunnen oplopen tot 94 % en tot 43 % voor urge-incontinentie bij
vrouwen met mictie disfunctie [28]. Volgens het onderzoek van Groutz et al. was de gemiddelde
plasfrequentie per dag bij volwassen mannen en vrouwen twaalf en de nachtelijke frequentie 3 tot 3,5 keer.
2.3.2. Lediging stoornissen [4, 16, 29-31]
2.3.2.1. Objectief te meten
Via uroflowmetrie kunnen verschillende patronen onderscheiden worden, die elk suggestief zijn voor
problemen. Een normale uroflow toont een klokvorm. Een torenvormige curve is suggestief voor OAB - een
vulling stoornis - en zal hier dus niet verder besproken worden.

20
In onderstaande tabel worden verschillende afwijkende patronen, de subjectieve klacht en de mogelijke
oorzaak op een rij gezet.
Klacht Beschrijving Figuur Suggestief voor
Startproblemen Verlengde tijd (lag
time) tussen signaal
tot starten en
effectieve start van de
flow (> 6 sec).
Blaashals disfunctie of dys
-synergie urethrale sfincter.
Staccatomictie Fluctuerend patroon
met mogelijks
verlengde mictie duur.
Intermittente overactiviteit
bekkenbodemspieren.
Intermittente mictie Volledig onderbroken
mictie met her -
haaldelijke start en
stop-spurts, verlengde
mictie duur.
Onderactieve detrusor en
abdominaal persen
intermittente overactiviteit
bekkenbodemspieren.
Zwakke straal Afgenomen
flowsnelheid,
plateauvormige curve
met verlengde mictie
duur.
Obstructie aan de
blaasuitgang.
Eindfase druppelen Verlengd einde van de
mictie met een
druppelende straal.
Afname contractiliteit
detrusor in de eindfase van
de mictie, obstructie.
Fig. 9: Afwijkende plaspatronen [4, 30, 31]
2.3.2.2. Subjectieve klachten
● Gevoel van incomplete lediging: de blaas voelt niet leeg aan na het plassen.
● Onmiddellijke nood om opnieuw te plassen: verdere mictie is noodzakelijk, snel na het lozen van urine.
● Persmictie: nood aan intensieve inspanning (buikpers, valsalva of suprapubische druk) om het plassen te
initiëren, onderhouden of de straal te verbeteren.
● Retentie: onmogelijkheid om te plassen, ondanks aanhoudende inspanning.

21
● Positie afhankelijke mictie: nood om een specifieke positie aan te nemen om te kunnen plassen (vb:
voorwaarts leunen, achterwaarts leunen of squat positie aannemen).
● Dysurie: brandend of oncomfortabel gevoel tijdens plassen. Dit kan optreden bij de start van de mictie of
aan het einde.
● Nadruppelen: ongewild urineverlies meteen na of binnen enkele minuten na het beëindigen van de
mictie. Dit kan geassocieerd zijn met vaginale reflux bij meisjes of syringocele bij jongens, of met een
zwakte van de m. Bulbocavernosus.
● Sproeistraal: sproeiende of gesplitste straal in plaats van een enkele, doorlopende straal.
● Plasangst of “shy bladder syndrome”: psychogene inhibitie van plassen, een extreme vorm van
startproblemen voornamelijk bij plassen op publieke plaatsen, in artificiële omstandigheden of in bijzijn
van andere personen [1, 32].
2.4. Risico’s
Zowel tijdens disfunctionele mictie als bij mictie disfunctie verhoogt de intravesicale druk en verhoogt aldus
het risico op vesico-urethrale reflux (VUR) [18, 19, 33, 34]. Disfunctionele mictie wordt vaker gezien bij
kinderen ouder dan vijf jaar met bilaterale, ernstige VUR. [34].
Patiënten met een afwijkend plaspatroon hebben daarnaast ook meer kans op het ontwikkelen van
urineweginfecties (UWI), voornamelijk deze die buikpers gebruiken tijdens het plassen.[27, 35]. De UWI
kunnen zowel het gevolg zijn van het plaspatroon als van het hieraan geassocieerde PMR. Door de contractie
van de sfincter tijdens het plassen kan een deel van de urine terugvloeien naar de blaas. Door dit
‘terugpompen’ komen bacteriën van buiten in de blaas terecht en bestaat een grotere kans op de ontwikkeling
van UWI. Hierbij is de UWI dus het gevolg van het plaspatroon zelf. Als er sprake is van residu, kan dit verder
leiden tot ontwikkeling van UWI [33].
Of een PMR steeds aanwezig is bij mensen met disfunctionele mictie heerst onduidelijkheid in de literatuur.
[3-5, 7]. Toch wijst onderzoek van Choi et al. bij vrouwen met disfunctionele mictie uit dat het gevoel van
incomplete lediging de meest voorkomende klacht is.[36].
Hoewel de oorzaak-gevolgrelatie niet helemaal duidelijk is, wordt gesteld dat blaasdisfunctie, VUR en UWI
belangrijke risicofactoren zijn in de ontwikkeling van nierschade en nierfalen op lange termijn. Hoewel ook
een overactieve blaas (OAB) in de afwezigheid van disfunctionele mictie kan leiden tot VUR en aldus
nierschade, is disfunctioneel plassen in combinatie met VUR sterker gerelateerd aan nierschade dan OAB
alleen.[33].
Persisterende disfunctionele mictie kan leiden tot de ontwikkeling van een luie, onderactieve blaas of zelfs
detrusor falen. Deze situatie wordt gekenmerkt door een verminderde mictiefrequentie, grote maximale
capaciteit, grote residuele volumes, overloopincontinentie en herhaaldelijke UWI.[19]. Anderzijds kan de
reactie op verhoogde weerstand ook een sterkere detrusorcontractie en verdikking van de blaaswand in de
hand werken, hetgeen zich uit in klachten van een OAB met frequentie, urgentie en urge-incontinentie[16].

22
Er zijn heel wat factoren die een invloed kunnen hebben op het mictie proces. We trachten hiervan een
opsomming te maken. We zijn ons ervan bewust dat dit niet volledig zal zijn.
2.5. Beïnvloedende factoren
2.5.1. Gedragsproblemen en psychiatrische stoornissen
Er is reeds heel wat onderzoek verricht naar de relatie tussen mictieklachten en neuro psychiatrische
stoornissen. Gedragsproblemen en psychiatrische stoornissen vormen een risicofactor voor het ontwikkelen
van blaasdisfuncties, omwille van onderstaande redenen:
● De mentale toestand van de patiënt vormt een determinerende factor of de patiënt al dan niet op tijd bij
de wc geraakt.
● Medicijnen, zoals bijvoorbeeld duloxetine, ®Cymbalta, ® Irenka die gebruikt worden om angst,
depressieve klachten of obsessieve dwangstoornissen (OCD) te behandelen, kunnen de blaas en darm
direct beïnvloeden, waardoor de persoon minder bewust wordt van de drang voor mictie en/ of
stoelgang. Bovendien hebben deze patiënten meestal minder gunstige behandelresultaten, vooral door
het feit dat ze de therapie niet volhouden. Vroege diagnose en behandeling van de mictie disfuncties zijn
cruciaal om secundaire comorbiditeiten te vermijden die de nier- en blaasfunctie kunnen beïnvloeden en
daaropvolgend impact kunnen hebben op hun psychosociaal welzijn.
2.5.2. Intellectuele functies
Intellectuele factoren zijn belangrijk bij de behandeling van mictie disfuncties. De personen moeten voldoende
mogelijkheden hebben om te begrijpen welke stappen ondernomen moeten worden. [37, 38].
Anderzijds hebben Yang P. et al in 2010 aangetoond dat mictie disfuncties vaker voorkomen bij kinderen met
een mentale retardatie in vergelijking met normaal ontwikkelende kinderen.[39].
2.5.3. Constipatie
Constipatie is een belangrijke oorzaak van plasproblemen.
Functionele constipatie is een klacht die zeer vaak samen gaat met disfunctionele mictie [40]. De
onderliggende pathofysiologie voor dit verband is nog niet volledig duidelijk. Een overactiviteit van de
urinaire sfincter om urinaire incontinentie te voorkomen zou een mogelijke oorzaak zijn [41].
Contractie en relaxatie van de bekkenbodemspieren zijn normaal gezien afgestemd op reflex contracties van
de blaas en het rectum [42].
Bovendien hebben mensen die persen bij stoelgang maken, een groter risico op het ontwikkelen van
stressincontinentie en urgentie [43]. Verder veroorzaakt constipatie een aangehouden intra-abdominale druk,
maar weliswaar niet zo hoog als bij hoesten. Toch heeft het wel een effect op de integriteit van de
ondersteunende structuren [44].

23
2.5.4. Toilethouding
Disfunctionele mictie kan het gevolg zijn van een onjuiste toilethouding. We gaan hier dieper op in bij het
hoofdstuk management.
2.5.5. Prolaps
Blaas- en continentieproblemen kunnen samengaan met een prolaps, vooral een anterieure verzakking. De
relatie tussen deze twee factoren is nog onduidelijk. Personen met een prolaps hebben meer klachten die
duiden op een overactieve blaas (urgentie, frequentie en urge incontinentie). Personen met een grotere graad
van verzakking hebben minder last van incontinentie dan personen met een kleine graad van verzakking. Een
prolaps kan een blaashalsobstructie veroorzaken.
Andere intrinsieke urethrale factoren liggen meer aan de basis van het ontstaan van incontinentie dan de
prolaps op zich. [71] Er is echter geen bewijs geleverd dat de blaasklachten bij prolaps veroorzaakt worden
door disfunctionele mictie of mictie disfunctie.
2.5.6. Stress
Stress kan mictieproblemen in de hand werken. Wood et al. heeft bij ratten aangetoond dat sociale stress
invloed heeft op de structuur en werking van de blaas, meer nog, dat hierdoor urinaire retentie kan optreden
[45]. Stress zorgt voor een verhoging van de bekkenbodem tonus en kan disfunctionele mictie in de hand
werken, maar ook hiervoor is geen bewijs.
2.6. Prevalentie
De prevalentie van plasproblemen is moeilijk in te schatten. Het gebrek aan consistent gebruik van een
duidelijke definitie en methodologie in studies bemoeilijkt het vergelijken van data. De variatie binnen cijfers
is dan ook groot. Daarnaast blijft het probleem vaak onopgemerkt door ouders of zorgverleners, wat een onder
rapportering van de problematiek met zich mee kan brengen [27].
2.6.1. Kinderen
Feldman et al stelden dat 40 % van de consultaties op pediatrische urologie voor klachten van disfunctionele
mictie waren [19]. Studies op basis van vragenlijsten bij kinderen met incontinentie rapporteren een
prevalentie van plasklachten van 4.2% tot 32% [27].
2.6.2. Volwassenen
In tegenstelling tot een hoog percentage op kinderleeftijd, zouden plasproblemen bij volwassenen voor 0,5 tot
2 % van de doorverwijzingen voor een UDO instaan [18].

24
Choi et al. spreekt echter van hogere percentages. Zo zou 7.2% van alle vrouwen met plasproblemen en 12.8%
van vrouwen met LUTS, die doorverwezen worden naar een specialist, disfunctioneel plassen [36]. Jeoung et
al. rapporteren hogere percentages bij mannen tussen 18 en 50 jaar met LUTS, nl 19,8- 30,2% [46].
Groutz et al spreken van een gelijke verdeling tussen mannen en vrouwen met LUTS, met een gemiddelde
leeftijd van 44,9 jaar bij mannen en 51,5 jaar bij vrouwen [18].
2.6.3. Ouderen (>65j)
Gezien het hoog aantal comorbiditeiten in deze populatie, is de prevalentie van zuivere disfunctionele mictie
of mictie disfunctie erg moeilijk in te schatten. Specifieke studies naar disfunctionele mictie, op basis van een
UDO of een flow EMG zijn op dit moment niet voorhanden.
Wel bestaat meer onderzoek naar detrusoroveractiviteit met verminderde contractiliteit als oorzaak van
urinaire klachten bij deze populatie. Jeong et al. stelt dat deze problematiek voor 38,6% bij mannen en 35,6%
bij vrouwen boven 65 jaar voorkomt [47].
Gezien bij veroudering zowel de detrusor kracht als de urethrale weerstand verminderd, zou vooraf bestaande
disfunctionele mictie zowel positief als negatief beïnvloed kunnen worden.
2.7. Diagnose
Mictie disfuncties en disfunctionele mictie kunnen gerelateerd zijn aan een uitgebreid spectrum van
klinische tekens en uitkomsten, gaande van relatief onschuldige klachten en, in het ergste geval, tot de
levensbedreigende complicatie van nierfalen. Bovendien is er tot op heden, zoals reeds hierboven
beschreven staat, geen eenduidige definitie over wat de term ‘disfunctionele mictie’ precies inhoudt en
wordt deze term vaak verward met mictie disfunctie. Dit heeft tot gevolg dat de diagnosestelling, tot
op heden, niet gebaseerd is op één duidelijk protocol [18]. Een nauwkeurige diagnose is essentieel
voor het opstellen van een correct behandelplan. Een video-urodynamisch onderzoek (VUDO) zal
ongetwijfeld de meest accurate onderzoeksmethode zijn. Maar er zijn een aantal nadelen aan
verbonden: hoge kosten, het is een invasief onderzoek, het vereist specifiek materiaal en getraind
personeel en bijkomend is er nog de blootstelling aan straling [48].

25
2.7.1. Anamnese
Zoals steeds moet er gestart worden met een grondige anamnese. De hulpverlener tracht een duidelijk beeld te
krijgen van het soort en de ernst van de klachten die de patiënt ervaart. Hoewel een zeer nauwkeurige
anamnese het hoofdprobleem kan aanwijzen, zijn het vaak de secundaire complicaties, zoals urine-
incontinentie en urineweginfecties, die klachten geven. Moeilijkheden met plassen op openbare plaatsen,
vertraagde initiatie van de mictie, een lage mictiefrequentie en de nood aan auditieve (bv. het geluid van
stromend water), visuele of fysieke (plassen in bad) hulpmiddelen om de initiatie van de mictie te kunnen
bevorderen, zijn vaak typische tekens die kunnen wijzen op moeilijkheden om de bekkenbodem te ontspannen,
noodzakelijk voor de mictie [2, 48, 49].
2.7.1.1. Plasdagboek
Een plasdagboek vormt een essentiële factor bij het stellen van de correcte diagnose en gaat in de regel vooraf
aan een urodynamisch onderzoek. De patiënt wordt gevraagd om de plasfrequentie, drang, plasvolume,
urineverlies en drankinname minimaal drie dagen (en nachten) bij te houden [48, 50]. Hieruit krijgt de
zorgverlener nauwkeurige en objectieve informatie over de vochtinname, de plasfrequentie, het totale
mictievolume, de maximale blaascapaciteit en de incontinentie episodes van de patiënt en krijgt zo eventueel
al wat meer inzicht in de symptomen die de patiënt ervaart. (Figuur 10 in bijlage).
2.7.1.2. Stoelgang dagboek
Bijkomend is een evaluatie van de darmfunctie, a.d.h.v. een stoelgang dagboek, aangewezen. (Figuur 11 in
bijlage).
2.7.1.3. Vragenlijsten
De “dysfunctional voiding symptom score” - vragenlijst kan gebruikt worden om een objectieve
evaluatie van de mictieproblemen te krijgen. Andere vragenlijsten, zoals bijvoorbeeld de ICIQ-
Male/female Lower Urinary Tract Symptoms (MLUTS/FLUTS), kan helpen bij de evaluatie van de
plasklachten en de impact op de levenskwaliteit. (Voor voorbeelden zie bijlagen).

26
2.7.2. Klinisch onderzoek
Basis neurologisch onderzoek: omvat voornamelijk een inspectie van de rug. De neuromotorische
functie van de onderste ledematen wordt hierbij nagegaan.
Bekkenbodem functie: een evaluatie van de bekkenbodemfunctie is eveneens op zijn plaats in de
diagnostische fase. Tijdens dit onderzoek wordt de tonus, de kracht, de uithouding en de
vermoeidheid van de bekkenbodemspieren nagegaan. Dit onderzoek gebeurt d.m.v. digitale
palpatie en de kracht van de bekkenbodem wordt gescoord volgens de Oxford Scale (zie bijlage).
Evaluatie mentale capaciteit: gezien het belang van de hogere mentale capaciteit bij het
voorkomen en bij de behandeling van disfunctionele mictie én mictie disfuncties, is een evaluatie
van de mentale capaciteiten onontbeerlijk tijdens het diagnostisch proces.
Urineonderzoek: dit kan uitgevoerd worden voor screening naar urineweginfecties en/of
nieraandoeningen.
US: De integriteit van de urinaire tractus dient nagegaan te worden d.m.v. ultrasound voor en na
de mictie [51]. Dit wordt vooral toegepast om eventuele schade aan de hogere urinewegen, VUR,
afwijkingen van de blaas (zoals een verdikte blaaswand, divertikels, sediment, abnormale
blaashals) en de rectale diameter (> 3 cm vormt een indicatie voor constipatie) na te gaan [49, 52].
2.7.3. Niet-invasief urodynamisch onderzoek: uroflowmetrie en EMG van de bekkenbodem
Dit onderzoek vormt de gouden standaard, en is dus ook een absolute noodzaak bij het opsporen van
disfunctionele mictie. Toch wordt het bij kinderen niet aangeraden om dit onderzoek meteen uit te voeren,
maar om ze eerst drie maanden door middel van urotherapie te behandelen [53]. Het is een relatief goedkoop,
gemakkelijk en pijnloos onderzoek, waardoor het ook geschikt is om toe te passen bij kinderen. De geplaste
volumes worden bepaald en moeten minimaal 50 % van de verwachte maximale blaascapaciteit bedragen
((leeftijd + 1) x 30 ml bij kinderen of 500 ml bij volwassenen). Maar anderzijds dient overdistensie van de
blaas ten allen tijde vermeden te worden. Het PMR wordt bepaald met behulp van een blaasscan. Hierbij
worden herhaalde post-mictie residu’s (>20 ml bij kinderen van vier tot zes jaar en >10 ml bij patiënten vanaf
zeven jaar) gezien als abnormaal. Verder wordt de urinestroom geanalyseerd. Tenslotte gaat men de maximale
stroomsnelheid (Qmax) na, met een minimaal toelaatbare waarde van 11.5 ml/s voor kinderen tot zes jaar en
15 ml/s vanaf zeven jaar [10]. Figuur 10 geeft een overzicht van de verwachte waarden voor mannen, vrouwen
en kinderen.

27
Fig. 12: Maximale stroomsnelheid voor mannen, vrouwen en kinderen [4]
Zoals hierboven vernoemd werd, is een staccato flow veroorzaakt door een dynamische urethrale obstructie
tijdens de mictie, indicatief voor disfunctionele mictie. Echter, in de studie van Wenske et al. was het
voorkomen van een staccato-curve bij uroflowmetrie maar bij 1/3 van de kinderen te wijten aan activiteit van
de bekkenbodem [31]. Een jaar later toonde dezelfde onderzoeksgroep aan dat 58% van de kinderen,
gediagnosticeerd met disfunctionele mictie, een staccato patroon vertoonden bij uroflowmetrie en de overige
42% andere curves, namelijk: onderbroken, gemixt en klokvormig [54]. Hieruit kunnen we besluiten dat
diagnose stellen enkel op basis van uroflowmetrie kan leiden tot over-diagnostisering van disfunctionele
mictie en detrusor overactiviteit en wordt het belang van simultane EMG van de bekkenbodem duidelijk.
Een volgend gegeven van enig belang is de lag-time. Hiermee wordt het tijdsinterval tussen het ontspannen
van de bekkenbodemspieren op EMG en de start van de urineflow bedoeld. Normaal relaxeren de
bekkenbodemspieren 1 tot 4 sec voor de start van de vrijwillige detrusorcontractie en dus de start van de flow
[14]. Hoewel, de resultaten beïnvloed kunnen worden door een vochtige huid en/of aanwezigheid van haar op
de plaats waar de elektrodes kleven. En bovendien meten, de oppervlakkige huid elektrodes niet rechtstreeks
de activiteit van de externe urethrale sfincter, maar vooral de activiteit van de levator ani. Het is in de klinische
praktijk voldoende om oppervlakkige huid elektrodes te gebruiken. Bijkomende EMG van de abdominale
spieren kan extra relevante informatie opleveren.
Uroflowmetrie inclusief residubepaling dient minimaal één keer herhaald te worden, in dezelfde omgeving.
Wanneer twee metingen erg verschillend zijn is een derde meting nodig [1, 9, 11].
Qmax(vrouw) 25-30ml/s
Qmax(man) 20-25ml/s

28
2.7.4. Verdere onderzoeken
Indien aangewezen, kunnen er nog een aantal bijkomende onderzoeken uitgevoerd worden.
MRI ruggenmerg: bij een verdacht neurologisch basisonderzoek kan een MRI van het ruggenmerg
uitsluitsel bieden over eventuele neurologische oorzaken.
Cystoscopie: dit kan eventuele anatomische afwijkingen van de urethra, de blaas of het
prostaatgebied opsporen.
VUDO: tenslotte kan een video-urodynamisch onderzoek (VUDO) meer duidelijkheid brengen
over de compliantie van de blaas, de functie van de blaashals en de eventuele aanwezigheid van
detrusoroveractiviteit of van VUR.
2.8. Management
Zie schema in de praktische handleiding
De behandeling van plasproblemen die hier verder besproken wordt, vraagt een individuele multidisciplinaire
aanpak. De behandeling die hier verder wordt toegelicht, betreft volgende plasproblemen: een discoördinatie
tussen blaas en bekkenbodemspieren (disfunctionele mictie) of plassen met een slechte straal (mictie
disfunctie) [55]. Deze plasproblematiek kan leiden tot de aanwezigheid van een postmictioneel residu.
Tijdens het eerste consult worden de kinderen, ouders of familieleden ingelicht over het verloop van een
normale mictie en over hoe een disfunctionele mictie verschilt van een normaal plaspatroon. Daarnaast wordt
het verloop van de behandeling, welk voor ieder individu verschillend is, verder toegelicht. Hierbij wordt de
nadruk gelegd op levensstijl interventies en het aanpassen van plasgewoonten.
Een standaard behandeling bestaat meestal uit urotherapie, aangevuld met andere behandelingstechnieken.
Urotherapie betekent dat er aan blaastraining gedaan wordt, zonder chirurgie of gebruik van medicatie.
Urotherapie bestaat uit, educatie, plas- en drankschema en een goede toilethouding. Echter, wanneer er
onderlinge fysiologische afwijkingen zijn, moet er toch gesproken worden over medicatie en chirurgie.
Bekkenbodemreëducatie, biofeedback, elektrostimulatie en sacrale neuromodulatie zijn mogelijke aanvullende
therapie onderdelen. Elk onderdeel wordt hieronder verder toegelicht.
2.8.1. Educatie
Wanneer de problematiek gekaderd is, start de educatie in functie van de urotherapie.
De patiënten en, indien mogelijk, hun omgeving, worden geïnformeerd over de normale functie van de blaas
en de bekkenbodem. Hierna wordt de wisselwerking tussen deze componenten verder uitgelicht. Net als het
belang van de juiste coördinatie tussen deze anatomische structuren voor het bekomen van een optimaal
plaspatroon.

29
De uitleg van de therapeut aan de patiënt moet zeker de volgende
elementen bevatten om te kunnen uitleggen hoe hun plassen afwijkt
van het normale patroon:
● Normale fysiologie vulling en lediging blaas
● Functie bekkenbodem
● Invloed bekkenbodem op mictie
● Invloed buikspieren op mictie en stoelgang
Fig. 13: Voorbeelden ophoudmanoeuvers bij kinderen [67]
Ophoud manoeuvres zijn strategieën om het symptoom incontinentie en urgentie tegen te gaan. Hierbij gaan
de patiënten met bepaalde houdingen de bekkenbodem aanspannen en zo de urethrale opening sluiten. De
benen kruisen, met de handen de genitale regio ondersteunen, op de hielen zitten, zijn enkele van deze
mogelijke posturen die voorkomen bij kinderen [55].
Het is belangrijk dat de therapeut de uitleg individueel aanpast, zodat de patiënt zijn specifieke problematiek
begrijpt, dit om te verzekeren dat de patiënt zijn problematiek kan kaderen.
Om de normale functie van de blaas te kunnen verzekeren, is het belangrijk dat er voldoende gerdronken
wordt en dat er regelmatig naar het toilet gegaan wordt.
Genitale hygiëne en de afwezigheid van constipatie zijn ook van primordiaal belang.
De therapeut kan aan de patiënt tips meegeven om de hygiëne van de genitale regio te waarborgen, gezien
irritatie van de huid in deze regio disfunctioneel plassen in de hand kan werken. Zo is het belangrijk dat natte
kledij tijdig verschoond wordt. Deze regio moet op een correcte wijze afgeveegd worden. Na het urineren
wordt de genitale regio best van voor naar achter gereinigd. De beweging van achter naar voor verhoogt de
kans op urineweginfecties, dit omdat de rectale bacteriën zo samenkomen in de vagina en zich dan kunnen
verplaatsen naar de blaas toe. Een andere manier is deze regio afdoppen. De genitale regio wordt best
gereinigd met producten zonder pH om zo de natuurlijke flora te behouden [27].
Om functionele constipatie te voorkomen, kan de therapeut de patiënt adviseren om vijf tot vijftien minuten na
elke maaltijd naar het toilet te gaan, dit om gebruik te maken van de gastrocolische reflex. De spieren van de
maag en darmwanden trekken samen na de maaltijd en zorgen ervoor dat de voeding doorheen de darm
vervoerd wordt door peristaltische bewegingen om zo plaats te maken voor nieuwe voeding [56].
De patiënt moet ook bewust worden van de juiste toilethouding tijdens defecatie. Deze verschilt met de
toilethouding voor mictie die verder besproken wordt. Het verschil ligt bij het feit dat bij stoelgang meer naar
achter wordt geleund en bij mictie meer naar voren. Stoelgang die zich lang in de darmen bevindt, wordt van
water onttrokken. Hierdoor wordt het belang van voldoende vochtinname nog eens benadrukt [55]. Naast
drinken is het eten van vezelrijke voeding aangeraden, doordat deze water absorbeert. Hierdoor verbetert de
consistentie van stoelgang, welk kan geobjectiveerd worden met de Bristol Stool Scale (Figuur 14 in bijlage).
Voldoende beweging heeft ook een positieve invloed op de gastro-intestinale transititietijd [38, 57].

30
Wanneer deze maatregelen niet genoeg zijn, kan de arts gecontacteerd worden om eventueel medicatie, zoals
laxativa op te starten.
2.8.2. Plasdisfunctie
Behandeling in geval van detrusor onderactiviteit of acontractiliteit
2.8.2.1. Urotherapie
2.8.2.1.1. Levensstijlverandering
Wanneer de ledigingsfase moet verbeteren, wordt in de behandeling de nadruk gelegd op het veranderen van
gewoonten. Deze veranderingen moeten geïntegreerd worden in het dagelijkse leven van de patiënt, zodat de
oorzaak van het probleem wordt aangepakt. Hierdoor worden betere resultaten behaald en wordt heval
voorkomen. De succesratio en de duur van de behandeling, waarover geen consensus bestaat, wordt mede
beïnvloed door mentale, psychologische en omgevingsfactoren.
Bij patiënten met een onderactieve detrusor kunnen deze veranderingen in levensstijl heel nuttig zijn. Het
vermijden van overrekking van de blaas is hierbij van groot belang.
Het beperken van vochtinname en een reductie in de inname van thee, koffie en alcohol kan het urine volume
doen dalen en kunnen bijgevolg helpen. Cafeïne, theïne en melkproducten zorgen ervoor dat de nieren meer
urine produceren om zo afvalstoffen uit te scheiden (zie figuur 15 in bijlagen) [38.] De aanbevolen
hoeveelheid vochtinname voor volwassenen is 1,5 liter per 24 uur, wat overeenkomt met zes tot acht glazen
van 1800-2400 ml. Deze richtlijn is wel afhankelijk van bijkomende factoren, zoals de gezondheid van de
patiënt, temperatuur en sport. Er moet echter wel voldoende vocht geconsumeerd worden, zodat de urine
zuiver, geurloos en licht geel kleurig is. [58].
2.8.2.1.2. Klokplassen
Bovenstaande levensstijl veranderingen moeten gecombineerd worden met klokplassen elke twee à drie uur.
Patiënten moeten de instructie krijgen om te plassen volgens de klok en niet te wachten op een drang om te
plassen. Veel van deze patiënten hebben een verminderd blaasgevoel, waardoor hun drang om te plassen
verlaat kan zijn. Het wachten op een drang om te plassen kan leiden tot een progressieve overrekking van de
blaas en detrusor schade. Aangezien de blaas het best contraheert bij een vulling van 300-350 ml, kan het
limiteren van het blaasvolume tot dit niveau een hulp zijn [37].
Bij kinderen kan gebruik gemaakt worden van een trilhorloge om hen eraan te herinneren regelmatig naar
toilet te gaan. Tevens kan een attest meegegeven worden aan de school om onbeperkte toegang tot het toilet
toe te laten [59].

31
2.8.2.1.3. Ledigingsmanoeuvers
● Dubbel- en driedubbel plassen: (dit wil zeggen twee- of drie keer na elkaar gaan plassen om de blaas
volledig te ledigen) 20 minuten na de initiële toiletgang kan eveneens helpen om het residu te
minimaliseren [37].
● Bekkenbodemreëducatie: De focus ligt hier op relaxatie van de bekkenbodemspieren om blaaslediging te
bevorderen [60].
● Psychologische- en omgevingsfactoren: Bepaalde symptomen, zoals incontinentie (zowel overdag als ‘s
nachts), herhaaldelijke urineweginfecties kunnen een grote psychologische impact hebben. Bijgevolg
moet de therapeut hier bedacht op zijn en, indien nodig, doorverwijzen naar een psycholoog [61].
● Intermittente katheterisatie: Bij patiënten met een ernstige onderactiviteit of acontractiliteit, is
intermittente zelf-katheterisatie aangewezen. Aan de patiënt wordt de instructie gegeven om hun blaas
vijf keer per dag te ledigen met een smalle katheter die ze zelf moeten inbrengen [37].
● Behandeling in geval van obstructie met goede coördinatie van de sfincters: Mictiedisfunctie als gevolg
van een obstructie (waarbij er een goede coördinatie van de sfincters is) kan niet conservatief behandeld
worden. De behandeling is hier medicamenteus, chirurgisch of via urethrale dilatatie. Aangezien hier
geen kinesitherapeutische behandeling voorhanden is, wordt dit niet verder besproken [37].
2.8.3. Disfunctionele mictie
2.8.3.1. Urotherapie
2.8.3.1.1. Informatie en educatie over de normale functie van urinewegen
Zie ‘educatie’
2.8.3.1.2. Gedragsverandering
Toilethouding: Disfunctionele mictie kan het gevolg zijn van een onjuiste toilethouding. Deze verkeerde
houding wordt doorgaans ontwikkeld vanaf de schoolleeftijd [17]. Door afgunst van de toiletten op
school (moeilijke bereikbaarheid, gebrek aan privacy, gebrek aan hygiëne), plassen jongens in staande
positie. Meisjes, echter, hurken boven de wc. Dit heeft tot gevolg dat ze leren plassen met een continue
contractie van de bekkenbodem, wat dan blaasdisfuncties in de hand kan werken. Bovendien plast 85 %
van de volwassen vrouwen op openbare wc’s in diezelfde half staande positie. Wanneer ze hier een
gewoonte van maken en op meerdere plaatsen boven de wc gaan hangen, gaat dit blaasdisfuncties in
stand houden [17].

32
Richtlijnen die we als therapeut kunnen meegeven met
de patiënt in verband met de toilethouding;
De patiënten moeten de tijd nemen om naar het toilet
te gaan. Het duurt enige tijd vooraleer de blaas
volledig geledigd is.
De patiënt moet een ontspannen houding aannemen.
Indien het achterwerk te klein is, kan er best gebruik
gemaakt worden van een kinderbril.
Patiënten moeten zitten op het toilet met volledige
steun van de dijen om zo een ontspannen houding te
bekomen.
Onderste kledingstukken tot aan de enkels brengen.
Staartbeen op de achterste rand van de bril laten rusten.
Niet persen. (zie verder)
Bekken wordt door de patiënt licht naar voor gekanteld.
De bekkenbodem moet bewust ontspannen worden door de patiënt, dit, omdat de mictie dan start
onder controle van de ‘wil’ van de patiënt. [68]
De urinestraal mag door de patiënt niet onderbroken worden tijdens de mictie, dit om postmictioneel
residu te voorkomen.
Na de mictie wordt door de patiënt zelf gecontroleerd of zijn/ haar blaas volledig leeg is. Dit doet
mendoor het bekken enkele malen te kantelen in voor- achterwaartse richting. Wanneer er nog urine in
de blaas zou zitten, wordt de blaas omwille van intra-abdominale verplaatsing verder geledigd.
Timed voiding: Zie ‘voiding dysfunction’
Genitale hygiëne: Zie ‘educatie’
Vermijden van ophoud manoeuvres: Zie ‘educatie.
Water laten stromen: Een kraan open zetten om plassen te kunnen initiëren, wordt regelmatig als
facilitatie gebruikt. Horen stromen van water kan langs de andere kant ook klachten van urgentie
uitlokken. De oorzaak hiervan wordt door onderzoekers verklaard door drie mechanismen. Ten eerste
kan het stromen van water een verhoging van parasympatische activiteit uitlokken, hetgeen
blaascontractie stimuleert. Daarnaast kan het geluid een kalmerend effect hebben, waardoor fysieke en
emotionele stress verminderen en het plassen zo gefaciliteerd wordt. Ten derde kan er sprake zijn van
een Pavlov-effect of conditionering, omdat het geluid van stromend water overeenkomt met het geluid of
zelfs het gevoel van plassen [62, 63].
Beperkt onderzoek toont aan dat het horen van stromend water een significante stijging van de
piekflowrate kan veroorzaken. Het heeft echter geen effect op PMR of plasduur [63].
Fig. 16: Correcte toilethouding

33
2.8.3.1.3. Levensstijladvies
● Type en volume van vochtinname: Hier gelden dezelfde richtlijnen als vochtinname bij plasdisfunctie
(zie hierboven).
● Preventie van constipatie: Zie ‘educatie’
2.8.3.1.4. Plasschema
Disfunctionele mictie kan samengaan met detrusor overactiviteit of detrusor onderactiviteit [59]. Hierin dient
dan ook een onderscheid gemaakt te worden in het plasschema dat voorgeschreven wordt.
2.8.3.1.4.1. Onderactieve blaas
Na het bekijken van het plasdagboek, samen met de patiënt, wordt er een plas interval bepaald op basis van het
langste interval tussen twee micties dat nog comfortabel is voor de patiënt. Aan de patiënt wordt de instructie
gegeven om te plassen bij het opstaan, elke keer op het afgesproken tijdsinterval en voor het slapengaan. In de
loop van de tijd wordt het tijdsinterval tussen twee plassen gradueel afgebouwd. Het doel is om te komen tot
een tijdsinterval van drie tot vier uur.
2.8.3.1.4.2. Overactieve blaas
Uitgesteld plassen is een andere manier om de patiënt te leren de blaas te controleren. De patiënt wordt hierbij
aangemoedigd om elke keer wanneer hij de drang voelt om te plassen, vijf minuten uit te stellen alvorens naar
toilet te gaan. Wanneer het goed lukt om vijf minuten uit te stellen kan de tijdsduur van het uitstellen verhoogd
worden, tot er uiteindelijk een normaal interval aanwezig is tussen twee plassen. Het kan helpen om de
aandacht van de patiënt af te leiden van de blaas door een taak te doen die concentratie vergt (bv. lezen, een
vriend bellen, to-do lijstje maken, …) [38].
2.8.3.2. Bekkenbodemreëducatie
Om disfunctionele mictie te behandelen moeten de patiënten hun bekkenbodem leren controleren. Bij deze
problematiek is er sprake van een discoördinatie tussen de bekkenbodem, de buikspieren en de blaas. Om een
goede coördinatie tussen deze elementen te bekomen, is bewuswording van elke anatomische eenheid
afzonderlijk belangrijk.
De bewustwording van de blaas wordt vooral bekomen door de urotherapie, die al eerder besproken is.
Als bij mictie de buikspieren te veel worden aangespannen tijdens het plassen, kan dit tegengegaan worden
door de kinderen een diafragmatische ademhaling aan te leren. Deze oefening wordt zowel uitgevoerd in
zittende, als in liggende positie (zowel rug als zijlig). In liggende positie worden de knieën geplooid en de
benen worden ondersteund door een kussen. De handen van de patiënt worden om de buikspieren neergelegd.
De therapeut vraagt aan de patiënt om in te ademen door de neus, terwijl de buik een bolle vorm aanneemt en
dus naar buiten gaat. Vervolgens moet de patiënt de adem enkele seconden inhouden om dan te eindigen met
rustig uitademen langs de mond met getuite lippen.

34
Hierbij moet de nadruk gelegd worden op de ontspanning van de buikmusculatuur. Het is belangrijk dat de
therapeut de patiënt leert de m. transversus abdominis te controleren en te palperen. Een spiegel kan gerust
gebruikt worden als hulpmiddel [55].
In het kader van deze problematiek moet de bekkenbodem vooral kunnen ontspannen. Bij deze patiënten
vertoont de bekkenbodem een contractie tijdens het plassen. Om ontspanning te bekomen moeten er enkele
stappen in de behandeling doorlopen worden.
2.8.3.2.1. Bewustwording
Als eerste stap moet de bekkenbodem kinesitherapeut de patiënt bewust maken van de bekkenbodem. Dit
wordt gedaan door de nodige uitleg te geven over de bekkenbodem, aangepast aan de patiënt. Tijdens de
educatie is dit al aangehaald, maar overloop het nog even kort met de patiënt, zodat deze zeker bewust is van
het doel van de oefeningen. Hiernaast laat de therapeut de patiënt kennis maken met de bekkenbodem a.d.h.v.
tactiele of visuele feedback strategieën. Hierbij kan de therapeut gebruik maken van de palpatie van het
centrum tendineum. Eveneens dient een inwendig onderzoek uitgevoerd te worden.
Als thuisoefening kan de patiënt de bekkenbodem zelf manueel palperen op het centrum tendineum.
Hierbij krijgt de patiënt sensorische feedback door de inwaartse liftbeweging van de levator plaat [55]. Deze
palpatie kan ondersteund worden door een spiegel.
2.8.3.2.2. Coördinatie
Een volgende stap in de behandeling is het ‘bewust’ leren op- en ontspannen van de bekkenbodem. Het
relaxeren van de bekkenbodem moet vooral benadrukt worden in de behandeling van disfunctionele mictie.
Volgende parameters worden best als uitgangspunt genomen. Drie of vier seconden submaximale contractie,
gevolgd door dertig seconden relaxatie [27, 55]. Deze waarden kunnen aangepast worden aan de behoeften
van de patiënt.
2.8.3.2.3. Functionele toepassing
Voor de mictie gestart wordt, moet de patiënt zich ervan bewust zijn dat de bekkenbodem ontspannen is.
Tijdens het plassen moet deze ontspanning kunnen aangehouden worden. Vaak lukt het om de bekkenbodem
te ontspannen voor de mictie, maar niet tijdens. Deze spieractiviteit kan gecontroleerd worden met behulp van
een biofeedback toestel [55].

35
De blaas, buik- en bekkenbodemspieren moeten nu gecoördineerd kunnen samenwerken, wanneer de patiënt
zich op het toilet bevindt. Voor de mictie start, moet de patiënt zich bewust zijn van de bekkenbodem die
ontspannen is en de diafragmatische ademhaling, zodat de buikspieren niet mee opspannen. Ook tijdens de
mictie moeten al deze spieren ontspannen blijven.
2.8.3.3. Biofeedback
Dit kan een aanvullende, goed voor de hand liggende, therapie zijn, naast urotherapie bij de behandeling van
disfunctionele mictie [27]. In het algemeen wordt biofeedback geopteerd, wanneer de bekkenbodem
onvoldoende kracht en uithouding heeft, maar ook coördinatie en spierrelaxatie van de bekkenbodem en
kenmerken van disfunctionele mictie, kunnen verbeterd worden door het gebruik van dit toestel [64].
Dit laat de patiënten toe om de output van de spiercontractie onmiddellijk te zien tijdens de oefening en kan
voornamelijk nuttig zijn bij patiënten die moeilijkheden hebben om te begrijpen hoe ze de spieren moeten
aanspannen of in dit geval ontspannen [65]. Hierdoor geeft het terug een motivatie aan de patiënten, indien de
standaard urotherapie niet voldoende bleek te zijn [59].
Er kan gebruik gemaakt worden van drie soorten biofeedback:
- Auditieve biofeedback (bv. door therapeut)
- Sensitieve biofeedback (bv. conussen)
- Visuele biofeedback (bv. via biofeedbacktoestel)
2.8.3.4. Elektrostimulatie
Parasacrale transcutane elektrische zenuwstimulatie (TENS) en percutane nervus tibialis stimulatie (PTNS)
kunnen toegepast worden, indien de patiënt, bijkomstig aan de disfunctionele mictie, symptomen heeft van een
overactieve blaas [59].
2.8.3.5. Sacrale neurostimulatie
Sacrale neurostimulatie (SNS) kan effectief zijn in de behandeling van disfunctionele mictie, indien er
symptomen aanwezig zijn van urinaire retentie en overactieve blaas. Sacrale neuromodulatie kan de
hersenrespons normaliseren, de blaas sensatie verbeteren en de ledigingsfunctie verbeteren bij niet-
obstructieve urinaire retentie [66].
2.8.3.6. Psychologische- en omgevingsfactoren
Zie voiding dysfunction
2.8.3.7. Intermittente zelf-katheterisatie
Zie voiding dysfunction

3.Bronnen
1. Koski, R.a., Rapid and practical interpretation of urodynamics. New York Springer, 2015.
2. Artibani, W. and M.A. Cerruto, Dysfunctional voiding. Curr Opin Urol, 2014. 24(4): p. 330-5.
3. Lukacz, E.S., et al., A healthy bladder: a consensus statement. Int J Clin Pract, 2011. 65(10):
p. 1026-36.
4. Austin, P.F., et al., The standardization of terminology of lower urinary tract function in
children and adolescents: update report from the Standardization Committee of the
International Children's Continence Society. J Urol, 2014. 191(6): p. 1863-1865 e13.
5. Utomo, E., J. Groen, and B.F. Blok, Surgical management of functional bladder outlet
obstruction in adults with neurogenic bladder dysfunction. Cochrane Database Syst Rev,
2014(5): p. CD004927.
6. Legger, Sequence of events in voiding the bladder, Dreamstime.com
7. Kampen, M.V., urine-incontinentie en andere klachten in de bekkenregio. Acco, 2001.
8. Fotter, Pediatric Uroradiology. Springer, 2008.
9. Nederlandse Vereniging voor Urologie, d.N.V.v.K.e.d.V.v.N.I.V. richtlijn: urine-
inctontinentie (UI) bij kinderen. 2016; Available from:
https://richtlijnendatabase.nl/richtlijn/urine-incontinentie_bij_kinderen/urine-
incontinentie_kinderen_-_korte_beschrijving.html#verantwoording.
10. Goldman, H.B. and S.P. Vasavada, Female urology : a practical clinical guide. Current
clinical urology. 2007, Totowa, N.J.: Humana Press. xvii, 433 p.
11. Austin, P.F., et al., The standardization of terminology of lower urinary tract function in
children and adolescents: Update report from the standardization committee of the
International Children's Continence Society. Neurourol Urodyn, 2016. 35(4): p. 471-81.
12. Van Kerrebroeck, P., et al., The standardization of terminology in nocturia: report from the
standardization subcommittee of the International Continence Society. BJU Int, 2002. 90
Suppl 3: p. 11-5.
13. Tse, V., et al., Conjoint Urological Society of Australia and New Zealand (USANZ) and
Urogynaecological Society of Australasia (UGSA) Guidelines on the management of adult
non-neurogenic overactive bladder. BJU Int, 2016. 117(1): p. 34-47.
14. Padoa, The overactive pelvic floor, ed. Springer. 2016.
15. Fowler, C.J., D. Griffiths, and W.C. de Groat, The neural control of micturition. Nat Rev
Neurosci, 2008. 9(6): p. 453-66.
16. Vella, M., D. Robinson, and D. Staskin, A reappraisal of storage and voiding dysfunction.
Curr Urol Rep, 2012. 13(6): p. 482-7.
17. Bauer, R.M. and W. Huebner, Gender differences in bladder control: from babies to elderly.
World J Urol, 2013. 31(5): p. 1081-5.

18. Sinha, S., Dysfunctional voiding: A review of the terminology, presentation, evaluation and
management in children and adults. Indian J Urol, 2011. 27(4): p. 437-47.
19. Feldman, A.S. and S.B. Bauer, Diagnosis and management of dysfunctional voiding. Curr
Opin Pediatr, 2006. 18(2): p. 139-47.
20. de Jong, T.P., et al., Effect of biofeedback training on paradoxical pelvic floor movement in
children with dysfunctional voiding. Urology, 2007. 70(4): p. 790-3.
21. Hodges, S.J., et al., The association of age of toilet training and dysfunctional voiding. Res
Rep Urol, 2014. 6: p. 127-30.
22. Abdel Raheem, A. and H. Madersbacher, Voiding dysfunction in women: How to manage it
correctly. Arab J Urol, 2013. 11(4): p. 319-30.
23. Hickling, D., M. Aponte, and V. Nitti, Evaluation and Management of Outlet Obstruction in
Women Without Anatomical Abnormalities on Physical Exam or Cystoscopy. Current Urology
Reports, 2012. 13(5): p. 356-362.
24. Robinson, D., et al., Defining female voiding dysfunction: ICI-RS 2011. Neurourology and
Urodynamics, 2012. 31(3): p. 313-316.
25. Chung, S.M., et al., Risk factors associated with voiding dysfunction after anti-incontinence
surgery. Int Urogynecol J, 2010. 21(12): p. 1505-9.
26. Sweeney, D.D. and W.W. Leng, Treatment of postoperative voiding dysfunction following
incontinence surgery. Curr Urol Rep, 2005. 6(5): p. 365-70.
27. Chase, J., et al., The management of dysfunctional voiding in children: a report from the
Standardisation Committee of the International Children's Continence Society. J Urol, 2010.
183(4): p. 1296-302.
28. Kuo, H.C., Videourodynamic characteristics and lower urinary tract symptoms of female
bladder outlet obstruction. Urology, 2005. 66(5): p. 1005-9.
29. Haylen, B.T., et al., An International Urogynecological Association (IUGA)/International
Continence Society (ICS) joint report on the terminology for female pelvic floor dysfunction.
Int Urogynecol J, 2010. 21(1): p. 5-26.
30. Kim, J.H., et al., Terminal dribbling in male patients with lower urinary tract symptoms:
relationship with International Prostate Symptom Score and with intravesical prostatic
protrusion. BMC Urol, 2015. 15: p. 89.
31. Wenske, S., et al., Can Staccato and Interrupted/Fractionated Uroflow Patterns Alone
Correctly Identify the Underlying Lower Urinary Tract Condition? Journal of Urology, 2012.
187(6): p. 2188-2193.
32. Franco, I., Functional Bladder Problems in Children Pathophysiology, Diagnosis, and
Treatment. Pediatric Clinics of North America, 2012. 59(4): p. 783-+.
33. Lee, H., et al., Vesicoureteral reflux and bladder dysfunction. Transl Androl Urol, 2012. 1(3):
p. 153-9.

34. Batinic, D., et al., Vesicoureteral reflux and urodynamic dysfunction. Urol Int, 2013. 90(4): p.
480-3.
35. Salinas, J., et al., Abdominal strength in voiding cystometry: a risk factor for recurrent urinary
tract infections in women. Int Urogynecol J, 2015. 26(12): p. 1861-5.
36. Choi, Y.S., et al., Analysis of female voiding dysfunction: a prospective, multi-center study. Int
Urol Nephrol, 2013. 45(4): p. 989-94.
37. Heesakkers, F.F., Practical Functional Urology. 2016: Springer.
38. Haslam, J. and J. Laycock, Therapeutic management of incontinence and pelvic pain : pelvic
organ disorders. 2nd ed. 2008, London: Springer. xxiii, 301 p.
39. Hoebeke, P., et al., Diagnostic evaluation of children with daytime incontinence. J Urol, 2010.
183(2): p. 699-703.
40. De Paepe, H., et al., Pelvic-floor therapy and toilet training in young children with
dysfunctional voiding and obstipation. BJU Int, 2000. 85(7): p. 889-93.
41. De Paepe, H., et al., Pelvic-floor therapy in girls with recurrent urinary tract infections and
dysfunctional voiding. Br J Urol, 1998. 81 Suppl 3: p. 109-13.
42. Hellerstein, S., Antibiotic treatment for urinary tract infections in pediatric patients. Minerva
Pediatr, 2003. 55(5): p. 395-406.
43. Byles, J., et al., Living with urinary incontinence: a longitudinal study of older women. Age
Ageing, 2009. 38(3): p. 333-8; discussion 251.
44. Duffy, D.L., K.A. Kruger, and J.A. Serpell, Evaluation of a behavioral assessment tool for
dogs relinquished to shelters. Prev Vet Med, 2014. 117(3-4): p. 601-9.
45. Wood, S.K., et al., Social stress-induced bladder dysfunction: potential role of corticotropin-
releasing factor. Am J Physiol Regul Integr Comp Physiol, 2009. 296(5): p. R1671-8.
46. Jeong, S.J., et al., Chronic lower urinary tract symptoms in young men without symptoms of
chronic prostatitis: urodynamic analyses in 308 men aged 50 years or younger. Korean J
Urol, 2014. 55(5): p. 341-8.
47. Jeong, W.S., et al., Men With Severe Lower Urinary Tract Symptoms Are at Increased Risk of
Depression. Int Neurourol J, 2015. 19(4): p. 286-92.
48. Ku, J.H., Voiding diary for the evaluation of urinary incontinence and lower urinary tract
symptoms: prospective assessment of patient compliance and burden. neurourol Urodyn,
2004. 23(4): p. 331-334.
49. Clothier, J.C. and A.J. Wright, Dysfunctional voiding: the importance of non-invasive
urodynamics in diagnosis and treatment. Pediatr Nephrol, 2017.
50. Schick, E., et al., Frequency-volume chart: the minimum number of days required to obtain
reliable results. Neurourol Urodyn, 2003. 22(2): p. 92-6.
51. Tangal, S., et al., Evaluation of a new ultrasound measurement tool for the diagnosis of
dysfunctional voiding in pediatric population: full/empty bladder wall thickness ratio.
Urology, 2014. 83(6): p. 1369-72.

52. Roupret, M., et al., [Use in daily urological practice of an ultrasound device for measuring
bladder volume]. Presse Med, 2003. 32(17): p. 776-80.
53. Fernandez, N., et al., Neurostimulation Therapy for Non-neurogenic Overactive Bladder in
Children: A Meta-analysis. Urology, 2017.
54. Wenske, S., et al., Analysis of uroflow patterns in children with dysfunctional voiding. J
Pediatr Urol, 2014. 10(2): p. 250-4.
55. Zivkovic, V., et al., Diaphragmatic breathing exercises and pelvic floor retraining in children
with dysfunctional voiding. Eur J Phys Rehabil Med, 2012. 48(3): p. 413-21.
56. Lynch, A., et al., Clinical inquiries. What are the most effective nonpharmacologic therapies
for irritable bowel syndrome? J Fam Pract, 2008. 57(1): p. 57-8.
57. McKay, S.L., M. Fravel, and C. Scanlon, Management of constipation. J Gerontol Nurs, 2012.
38(7): p. 9-15.
58. Laycock, J. and J. Haslam, Therapeutic management of incontinence and pelvic pain : pelvic
organ disorders. 2002, London ; New York: Springer. xxi, 265 p.
59. Arlen, A.M., Dysfunctional Voiders-Medication Versus Urotherapy? Curr Urol Rep, 2017.
18(2): p. 14.
60. Chapple, C., Female urology. Curr Opin Urol, 2011. 21(4): p. 267.
61. Hoebeke, P., et al., Assessment of lower urinary tract dysfunction in children with non-
neuropathic bladder sphincter dysfunction. Eur Urol, 1999. 35(1): p. 57-69.
62. Kim, G.S., et al., Combined pelvic muscle exercise and yoga program for urinary
incontinence in middle-aged women. Jpn J Nurs Sci, 2015. 12(4): p. 330-9.
63. Cho, K.J., et al., Evaluation of female overactive bladder using urodynamics: relationship
with female voiding dysfunction. Int Braz J Urol, 2015. 41(4): p. 722-8.
64. Hay-Smith, E.J., et al., Comparisons of approaches to pelvic floor muscle training for urinary
incontinence in women. Cochrane Database Syst Rev, 2011(12): p. CD009508.
65. Ghaderi, F. and A.E. Oskouei, Physiotherapy for women with stress urinary incontinence: a
review article. J Phys Ther Sci, 2014. 26(9): p. 1493-9.
66. Young, Detrusor Overactivity with Impaired Contractility (DOIC) in the Elderly: Challenges
in Management. springer, 2015. 10(3): p. 278-287.
67. Franco, I., Overactive bladder in children., Nature Reviews Urology, 2016 (13), 520-532
68. Osteonieuws (2016), Houden we het droog?, Osteonieuws.com, Retrieved august 8, 2017,
https://osteonieuws.com/2016/06/
69. MediPedia (2015), Overactieve blaas, Retrieved september 16 2017,
https://nl.medipedia.be/overactieve-blaas/begrijpen/anatomie-van-de-urinewegen-blaas-
urinebuis-en-sluitspier
70. The Well Woman Centre (2014) Adult Urinary Incontinence, Retrieved july 26, 2017
http://wellwomancentre.ie/sub-topics/adult-urinary-incontinence/

71. Montserrat, A., Pelvic floor symptoms and severity of pelvic organ prolapse in women seeking care
for pelvic floor problems., Elog, 2014(177), 141-145
72. Harinath, K., et al. (2005). "Autonomic nervous system and adrenal response to cold in man at
Antarctica." Wilderness Environ Med 16(2): 81-91

4. Afkortingen
DSD: Detrusor sfincter dyssynergie
EMG: ElektroMyoGrafie
ICS: International Continence Society
ICCS: International Children’s Continence Society
IPG: Interne pulsgenerator
IUGA: International Urogynaecological Society
OAB: Overactieve blaas
OCD: Obsessive Compulsive Disorders (obesessive dwangstoornissen)
PMC: Pontien mictiecentrum
PMR: Post mictioneel residu
PTNS: Percutane nervus tibialis stimulatie
SANS: Sacrale neurostimulatie
TENS: Transcutane elektro neurostimulatie
UDO: Urodynamisch onderzoek
US: Ultrasound
UWI: Urineweg infectie
VUDO: Video urodynamisch onderzoek
VUR: Vesico-urethrale reflux

5. Bijlagen
5.1. Figuren
Fig 1: Een normale mictie
Fig 2: Een anatomische voorstelling van het urinewegstelsel
Fig 3: De blaas
Fig 4: Anatomische structuren van het perineum
Fig 5: De musculaire ondersteuning van het bekken
Fig 6: De invloed van de hersenen op de blaas
Fig 7: De invloed van de hersenen op de blaas
Fig 8: De Plascurve
Fig 9: Afwijkende plaspatronen
Fig 10: Plasdagboek
Fig 11: Stoelgangsdagboek
Fig 12: Maximale stroomsnelheid voor mannen, vrouwen en kinderen
Fig 13: Voorbeelden van ophoudmanoeuvers bij kinderen
Fig 14: Bristol Stool Form
Fig 15: Dranken voor een gezonde blaas
Fig. 16: Correcte toilethouding

Fig 2: Een anatomische voorstelling van het urinewegstelsel [3]
Fig 3: De blaas [69]

Fig 10: Plasdagboek

Fig 11: Stoelgangsdagboek

Fig 12: Maximale stroomsnelheid voor mannen, vrouwen en kinderen
Qmax(man) 20-25ml/s
Qmax(vrouw) 25-30ml/s

Fig 14: Bristol Stool Form

Fig 15: Dranken voor een gezonde blaas

5.2. Documenten
5.2.1. Varia Tips
Koude omgeving en plassen
Verandering van warme naar koude omgeving zorgt voor een graduele afname van sympathische
activiteit en een shift richting meer parasympatische activiteit. Dit kan verklaren waarom gezonde
individuen last kunnen krijgen van urgentie en frequentie bij verandering van omgevingstemperatuur
of indien handen of voeten koud hebben. Indien er reeds klachten van overactieve blaas bestaan, kan
koude de klachten sterk doen toenemen. [73]
Intravaginaal plassen (vaginal voiding/ vaginal reflux)
Klacht van ongevoeld urineverlies binnen 10 minuten na het beëindigen van de mictie in afwezigheid
van anatomische afwijkingen of afwijkende mictie, bij personen met normale sfinctercontrole. Dit
urineverlies treedt op als een deel van de urine in de introïtus terecht komt tijdens het plassen en er
nadien terug uit druppelt. Dit kan vaginale irritatie en roodheid veroorzaken en zou gelinkt zijn met
meer vulvovaginitis of zelfs schimmelinfecties. Vaginale reflux treedt vaak op wanneer de benen in
adductie zijn of er niet voldoende plaats tussen de benen is (vb. bij obese kinderen).
Behandeling bestaat dan ook voornamelijk uit het aanleren van een correcte, ontspannen plashouding.
[74,4]
Anteverse mictiestraal : Anterior Deflection Urinary Stream (ADUS)
Anteverse mictiestraal treedt op bij meisjes met een meatusafwijking. Omdat de straal naar voor
afwijkt, hebben deze meisjes moeite met plassen, willen ze de straal remmen en ontstaat er mogelijks
disfunctionele mictie met gevolgen als UWI, PMR etc. Chirurgische correctie blijkt hier de meest
aangewezen behandeling.

5.2.2. Praktische handleiding
5.2.2.1. Definities
Normale mictie
Normale mictie is een vrijwillig geïnitieerde continue detrusorcontractie die leidt tot een complete
blaaslediging in een normale tijdspanne met de afwezigheid van obstructie.
Disfunctionele mictie
Een onderbroken en/of fluctuerende flow veroorzaakt door onvrijwillige intermitterende contracties
en dus verhoogde EMG activiteit van de peri urethrale en levator ani spieren tijdens plassen bij
neurologisch normale personen.
Mictiedisfunctie
Abnormaal trage of onvolledige mictie gebaseerd op symptomen en urodynamisch onderzoek
5.2.2.2. Diagnose
Anamnese
Plasdagboek
Stoelgangsdagboek
Vragenlijsten
Subjectieve klachten:
Gevoel van incomplete lediging
Onmiddellijke nood om opnieuw te plassen
Persmictie
Retentie
Positie afhankelijke mictie
Dysurie
Nadruppelen
Sproeistraal
Plasangst of shy bladder syndrome

Klinisch onderzoek
Basis neurologisch onderzoek
Bekkenbodemfunctie
Evaluatie mentale capaciteit
Objectieve onderzoeken
Urine onderzoek
Ultrasound
UDO+EMG
Uroflow+ EMG
Indien onvoldoende informatie doorverwijzen voor:
MRI
Cystoscopie
...

Plasdisfunctie
Urotherapie
Levensstijl- verandering
Klokplassen
Ledigings-
manoeuvers
Bekkenbodemreëducatie
Psychologische- en
omgevingsfactoren
Intermittente katheterisatie
5.2.2.3 Behandeling



5.2.3.Meetinstrumenten
5.2.2.3. Vragenlijsten
Dysfuctional Voiding Symptom Score
Questions predictive of Dysfunctional Voiding in both males and females: 1, 4, 6, 7
Threshold Score for Dysfunctional Voiding: Females = 6 Males = 9

ICIQ – LUTS
ICIQ-MLUTS – plasklachten vragenlijst mannen
Let op: Deze vragen hebben betrekking op de afgelopen 4 weken! Vink of omcirkel telkens één
antwoord aan per vraag.
1a. Duurt het even vooraleer u kunt beginnen met plassen?
Nooit
Zelden
Soms
Meestal
Altijd
1b. Hoeveel last hebt u hiervan?
0 1 2 3 4 5 6 7 8 9 10
helemaal geen last heel veel last
2a. Moet u moeite doen om te blijven plassen?
Nooit
Zelden
Soms
Meestal
Altijd
2b. Hoeveel last hebt u hiervan?
0 1 2 3 4 5 6 7 8 9 10
helemaal geen last heel veel last
3a. Hoe zou u de kracht van uw urinestraal omschrijven?
Nooit
Zelden
Soms
Meestal
Altijd
3b. Hoeveel last hebt u hiervan?
0 1 2 3 4 5 6 7 8 9 10
helemaal geen last heel veel last

4a. Stopt u meer dan eens tijdens het plassen en gaat u daarna weer door?
Nooit
Zelden
Soms
Meestal
Altijd
4b. Hoeveel last hebt u hiervan?
0 1 2 3 4 5 6 7 8 9 10
helemaal geen last heel veel last
5a. Hoe vaak hebt u na het plassen het gevoel dat uw blaas niet goed geleegd is.
Nooit
Zelden
Soms
Meestal
Altijd
5b. Hoeveel last hebt u hiervan?
0 1 2 3 4 5 6 7 8 9 10
helemaal geen last heel veel last
6a. Moet u zich plotseling naar het toilet haasten om te plassen?
Nooit
Zelden
Soms
Meestal
Altijd
6b. Hoeveel last heb u hiervan?
0 1 2 3 4 5 6 7 8 9 10
helemaal geen last heel veel last

7a.Verliest u urine vooraleer u het toilet kunt bereiken?
Nooit
Zelden
Soms
Meestal
Altijd
7b. Hoeveel last hebt u hiervan?
0 1 2 3 4 5 6 7 8 9 10
helemaal geen last heel veel last
8a. Verliest u urine wanneer u hoest of niets?
Nooit
Zelden
Soms
Meestal
Altijd
8b. Hoeveel last hebt u hiervan?
0 1 2 3 4 5 6 7 8 9 10
helemaal geen last heel veel last
9a. Verliest u wel een urine zonder duidelijke reden en zonder dat u het gevoel hebt dat u moet
plassen?
Nooit
Zelden
Soms
Meestal
Altijd
9b. Hoeveel last hebt u hiervan?
0 1 2 3 4 5 6 7 8 9 10
helemaal geen last heel veel last

10a. Verliest u urine als u slaapt?
Nooit
Zelden
Soms
Meestal
Altijd
10b. Hoeveel last hebt u hiervan?
0 1 2 3 4 5 6 7 8 9 10
helemaal geen last heel veel last
11a. Hoe vaak gebeurt het dat enkele minuten nadat u geplast hebt en u uw kleding weer hebt
aangetrokken, uw onderbroek een beetje nat wordt?
Nooit
Zelden
Soms
Meestal
Altijd
11b. Hoeveel last hebt u hiervan?
0 1 2 3 4 5 6 7 8 9 10
helemaal geen last heel veel last
12a. Hoeveel keer plast u gemiddeld overdag?
1-6 keer
7-8 keer
9-10 keer
11-12 keer
13 keer of meer
12b. Hoeveel last hebt u hiervan?
0 1 2 3 4 5 6 7 8 9 10
helemaal geen last heel veel last

13a. Hoeveel keer moet u ’s nachts gemiddeld opstaan om te plassen?
Nooit
Zelden
Soms
Meestal
Altijd
13b. Hoeveel last hebt u hiervan?
0 1 2 3 4 5 6 7 8 9 10
helemaal geen last heel veel last

ICIQ-FLUTS – plasklachten vragenlijst vrouwen
Let op: Deze vragen hebben betrekking op de afgelopen 4 weken! Vink of omcirkel telkens één
antwoord aan per vraag.
1a. Hoeveel keer moet u gemiddeld ’s nachts opstaan om te plassen?
Geen keer
1 keer
2 keer
3 keer
4 of meer keer
1b. Hoeveel last hebt u hiervan?
0 1 2 3 4 5 6 7 8 9 10
helemaal geen last heel veel last
2a. Moet u zich naar het toilet haasten om te plassen?
Nooit
Af en toe
Soms
Meestal
Altijd

2b. Hoeveel last hebt u hiervan?
0 1 2 3 4 5 6 7 8 9 10
helemaal geen last heel veel last
3a. Heeft u pijn in uw blaas?
Nooit
Af en toe
Soms
Meestal
Altijd
3b. Hoeveel last hebt u hiervan?
0 1 2 3 4 5 6 7 8 9 10
helemaal geen last heel veel last
4a. Hoeveel keer plast u overdag gemiddeld?
1-6 keer
7-8 keer
9-10 keer
11-12 keer
13 of meer keer
4b. Hoeveel last hebt u hiervan?
0 1 2 3 4 5 6 7 8 9 10
helemaal geen last heel veel last
5a. Moet u even wachten voordat u kunt beginnen met plassen?
Nooit
Af en toe
Soms
Meestal
Altijd

5b. Hoeveel last hebt u hiervan?
0 1 2 3 4 5 6 7 8 9 10
helemaal geen last heel veel last
6a. Moet u drukken of persen om te plassen?
Nooit
Af en toe
Soms
Meestal
Altijd
6b. Hoeveel last hebt u hiervan?
0 1 2 3 4 5 6 7 8 9 10
helemaal geen last heel veel last
7a. Wordt het plassen meer dan eens onderbroken zonder dat u dat wilt.
Nooit
Af en toe
Soms
Meestal
Altijd
7b. Hoeveel last hebt u hiervan?
0 1 2 3 4 5 6 7 8 9 10
helemaal geen last heel veel last
8a. Verliest u urine voor u het toilet kunt bereiken?
Nooit
Af en toe
Soms
Meestal
Altijd

8b. Hoeveel last hebt u hiervan?
0 1 2 3 4 5 6 7 8 9 10
helemaal geen last heel veel last
9a. Hoe vaak verliest u urine?
Nooit
Eén keer per week of minder
2-3 keer per week
Één keer per dag
Verscheidene keren per dag
9b. Hoeveel last hebt u hiervan?
0 1 2 3 4 5 6 7 8 9 10
helemaal geen last heel veel last
10a. Verliest u urine wanneer u lichamelijk actief bent, zich inspant, hoest of niest?
Nooit
Af en toe
Soms
Meestal
Altijd
10b. Hoeveel last hebt u hiervan?
0 1 2 3 4 5 6 7 8 9 10
helemaal geen last heel veel last
11a. Verliest u ooit urine zonder duidelijk oorzaak en zonder dat u voelt dat u moet plassen?
Nooit
Af en toe
Soms
Meestal
Altijd

11b. Hoeveel last hebt u hiervan?
0 1 2 3 4 5 6 7 8 9 10
helemaal geen last heel veel last
5.2.2.4. Objectieve meetmethoden
Oxford Scale
Score 0: geen zichtbare of voelbare contractie
Score 1: twijfelachtige tot zeer zwakke contractie
Score 2: zwakke contractie, maar zonder twijfel waarneembaar, zonder verplaatsing
Score 3: goed voelbare contractie, die weerstand kan overwinnen met verplaatsing
Score 4: krachtige contractie tegen matige weerstand
Score 5: maximale contractie tegen sterke weerstand