水素,一酸化炭素,二酸化炭素及びメタンの **, -mitstm, …
Transcript of 水素,一酸化炭素,二酸化炭素及びメタンの **, -mitstm, …

JAER1-M—93-029
JP9306174
J A E R I - M 93029
**, -mitstm, rmwsmA&* *>® m>mm%>*v*r-v
1 9 9 3 ^ 3 ft
mm -m
Japan Atomic Energy Research Institute
~AERI ・ M
93・029
JAERI-N-93-029
JP9306174
水素,一酸化炭素,二酸化炭素及びメタンの
熱物性値推算パッケージ
1 993年 3月
羽田一彦
日本原子力研究所Japan Atomic Energy Re掠archInstitute
ー

JAERI-M V ,-K- h li, B ^ft?.?^W^ESrA^SXBCaflJL-Cv^W^*^*-^, A*«ora&*>«u;, B*B|f *w?EBftt*flMR«tti!*R«»a (T3i9-ii3a*«*srffl5*:
(T3i9-ii sjt ajjireBiRfswB if. ftfif^EWrt) -t-»¥u<j:sts***£i;~$.--?-c fc1) a t .
JAERI-M reports are issued irregularly. Inquiries about availability of the reports should be addressed to Information Division,
Department of Technical Information, Japan Atomic Energy Research Institute, Tokai-mura, Naka-gun, Ibaraki-ken 319-11, Japan.
Japan Atomic Energy Research Institute, 1993
9 M ww?****-*—**
圃t
JAERI-Mレポートは.日本原子力研究所が不定期に公刊している研究報告書て寸。
入手の間合わせは,日本原子力研究所技術情報部情報資料課(〒319・11茨織県那珂郡東
海村)あて.お申しこし〈ださい。なお.このほかに財団法人原子力弘済会資料センター
(〒319-11茨城県都珂郡東海村日本原子力研究所内)で複写による実費頒布をおこなって
必ります。
JAERI-M reports are issucd irresu1ar1y_ Inquirics ab叩 tavailability of thc開 po出品叫ldbe add暗闇dto Information Di'吋sion,
Dcpartment of Tcchnica1 Information, Japan Atomic EncllY Rcscarch Institute, Tokai-mura, Naka宮un,lbar富悩"kcn319-11, Jap.n.
。JapaaAt咽 icEncrl)" Research lnstitllte, 1993
編集議姥行 日本原子力碕究所
印 刷 側様子力資将サービス

H
JAERI-M 93-029
mm -m
U993*Flfl26B£&)
(1) ^ g < C o l > T ( i . Peng-Robinson-Redlich-Kwong CDttlfi^g^;.
(2) «£EJtffe(C-5i»r«. van der Waals © t t f f i * e ^ t r » * ^ f t f e H # ^ * a f f l L T * » f c
**W3£i9r : T311-I3 3?*!*!K3IS!*?G*zfeBrJ£ffl*r:£*f«3607
ー
JAERI-M 93-029
水素.一酸化炭素,二酸化炭素及びメタンの
書生物性値f陸算パッケーツ
日本原子力研究所大洗研究所高温工学試験研究炉開発認
羽田一彦
【1993年UJ26日受理}
水素.一酸化炭素,二酸化炭素及びメタンの熱物性値推算パッケージを,公開文般に提案され
ている理論式や実験式を検討し選定することにより構築した。熱物性値としては,密度,定圧
比熱.粘性係数及び熱伝導率を対象とした。
選定した縫算式は次のとおりである。
(!) 密度については.Peng-Robinson-Redlich-Kwongの状態方程式.
(2) 定圧比熱については. van der Waal sの状態方程式に熱力学的な関係式を適用して求めた
式.並びに.
(3) 粘性係数及び熱伝導率については.Thodosらが開発した次元解析法を適用した一般化関係
王t。
これらの選定推算式を試験データや選定値集の値と比較した結果,比熱以外の密度,給性係数
及び熱伝導率の推算式の精度は,工学的に十分許容される範囲内にあることが明らかになった。
大洗研究所:干311-13 茨被県東茨減郡大洗町成田町字新纏3607

JAERI-M 93-029
Thermal Property Correlation Package of Hydrogen, Carbon Monoxide, Carbon Dioxide and Methane
Kazuhiko HADA
Department of HTTR Project Oarai Research Establishment
Japan Atomic Energy Research Institute Oarai-machi, Higashiibaraki-gun, Ibaraki-ken
(Received January 26, 1993)
A thermophysical property correlation package of hydrogen, carbon monoxide, carbon dioxide and methane has been constructed from a critical evaluation of theoretical or empirical correlations available in the literature. The properties include density, isobaric specific heat, viscosity and thermal conductivity.
Selected package correlations are summarized below: (1) For density, Peng-Robinson-Redlich-Kwong equation of state, (2) for specific heat, an expression from thermodynamic theory with the
van der Waals equation of state and (3) for viscosity and thermal conductivity, generalized relationships
by the use of dimensional analysis that were developed by G. Thodos group. From a comparative evaluation of the package correlations with
measurements and selected values available, it has been concluded that except for specific heat these correlations are predictable with an acceptable accuracy.
Keywords: Thermal Property, Hydrogen, Carbon Monoxide, Carbon Dioxide, Methane, Density, Specific Heat, Viscosity, Thermal Conductivity
II
JAERI-M 93-029
Thermal Property Correlation Package
of Hydrogen. Carbon Monoxide. Carbon Dioxide and Methane
Kazuhiko HADA
Department of HTTR Project
Oarai Researcb Establisbment
Japan Atomic Energy Research lnstitute
Oarai-machi. Higashiibaraki-gun. lbaraki-ken
(Received January 26. 1993)
A thermophysical property correlation package of hydrogen. carbon
monoxide, carbon dioxide and methane bas been constructed from a criti-
cal evaluation of theoretical or empirical correlations available in the
literature. The properties include density. isobaric specific heat.
viscosity and thermal conductivity.
Selected package correlations are summarized below:
(1) For density. Peng-Robinson-Redlich-Kwong equation of state.
(2) for specific heat. an expression from thermodynamic tbeory with the
van der Waals equation of state and
(3) for viscosity and thermal conductivity. generalized relationships
by the use of dimensional analysis that were developed by G. Thodos
group.
From a comparative evaluation of the package correlations witb
measurements and selected values available, it has been concluded that
except for specific heat these correlations are predictable with an
acceptable accuracy.
Keywords: Thermal Property. Hydrogen. Carbon Monoxide. Carbon Dioxide,
Methane, Density, Specific Heat, Viscosity. Thermal
Conductivity
11

• IAKHI M 9;< 029
@ ik
1. **.## 1 2. !&&14ffift»i$©il£ 2
2. 1 $ a 3 2.1. 1 «£3¥it©«g 3 2. 1. 2 « * ; * © » £ 5
2. 2 5gEit& 8 2.2. 1 ff£SL5$©«lg 8 2.2.2 mn^.<omm u
2.3 temm 14 2.3. i mn^conm 14 2.3.2 mw^<omm is
2.4 &£*$ 20 2.4.1 mu^owim 20 2. 4. 2 flCWst©^ 23
3. mw-i$,<z>m%.m±:®it®mm 28 3. 1 «^ffi*©l»Wtifc«el¥ffiffl©*^ 28 3. 2 i tSi f f f l 30
4. mrnrnuB ei 5. t t & 74 m 1% 79 ##£lft 80 m 1 s £ uzmmmm&onnm 83 nmz mMM&Rvmji 92 #§§3 onifyf-y?<Dmnz*'bt:itz, MMm»3:®m%.mk<z>itmtm 94 ttlJU Jt&Jt/c©*#«;:ot,>T 98
ii!
.IAI-:I¥I ¥1 9;{ 029
日 次
1. まえがき
2. 熱物性値推算式の選定 一一一一一一一一一一一一一…-.-._._.ー…一一一一………ー……ー 2
2. 1 密 度……一一………………………………一一一一一ー…---_.....一一…一一一 3
2. 1. 1 推算式の慨要-一一一一一…………ー・…一……一一一一一一一一一……一一一… 3
乙1.2 推算式の選定一一一一一・…一一一一一一…一一一一ー一一一一一……一一一一一 5
2.2 定圧比熱 _._.". 一一一 一一一 ー一一一ーー・・‘...、ー・ーーーーーー_......-.-..._----_.ーー令・ーーーーーーー.......ーーーーー.. 8
2.2. 1 推算式の慨要一一一一一一一…ー………一一一一一……………………………….. 8
2.2.2 推算式の選定一一一一-一一一一一一一一…一一一一……ー…………一一一一 11
2.3 粘性係数………..-..一一…,ー・一一一…一一…………一一一一一一…………… 14
2.3.1 推算式の概要一一一一一一一一一一一一一,ー………………一一一一一一一一一 14
2.3.2 推算式の選定 0'__"'-'-一….._--ーー…一一一一一一一一一一一一一一一一一一・ 18
2.4 熱伝導率 一一一一一一一一一一一…・一一一一一一一一一一一一一一一一一一一…一一一……--..20
2.4. 1 推算式の概要一一........._--一一…"'-.-………一一………一一…ー……一一… 20
2.4.2 推算式の選定一一一一一…一一一一一一一._----_...…一一一一一一一一一一一一一……...23
3. 推算式の選定値との比較評価………ー一一一一一……一一----_....……一一一一一一 28
3. J 選定値集の概要と比較評価用の選定一一一一一一一一一一一一一一一一…一一一一一…・一一一 28
3.2 比較評価 一一…………・……ー一一一一ー一一…・一一一一一…………...30
4. 熱物性値線図 ー-.--.一一一一・・…一一-……ー……一……一一ー…ー…--...__.._-…… 61
5. まとめーー一一一ー…ー一一一一……ー一一一ー…………ーー・一一一一一一一一一一一・ーー 74
謝 辞 …ー一一一一一一一-ーー一一一一一一"'-_.-.…...・- 一一一一一一-一一一一…一一 79
参考文献 ーー…………一一……………………‘一一一一一一…………一一……一一…...80
付録 l 選定した熱物性値推算式の計算例………....._---…………一一一一一一一一一一..83
付録2 飽和温度及び圧力 一一一一一 一一一一一一一一一一一一一一一一一…._----一一一..92
付録3 ワ J~ ガフチックの便覧を中心とした,選定縫算式の選定値との比較評価……一一 94
付録4 比熱比κの推算について……………………………一一"._------………....__...……--98
II!

.IAHHI M 93 -029
Contents
1. Introduction j 2. Selection of Thermal Property Correlations 2 2.1 Density 3 2.1.1 Review of Correlations 3 2.1.2 Selection 5
2.2 Isobaric Specific Heat g 2.2.1 Review of Correlations g 2.2.2 Selection JJ
2.3 Viscosity 14 2.3.1 Review of Correlations ]4 2.3.2 Selection jg
2.4 Thermal Conductivity 20 2.4.1 Review of Correlations 20 2.4.2 Selection . 23
3. Comparative Evaluation of Selected Correlations with Selected Values 28
3.1 Review of Selected Value Handbooks and Their Selection for the Evaluation 28
3.2 Comparative Evaluation 30 4. Thermal Property Diagram , gj 5. Summary 74 Acknowledgement 70 References on Appendix 1 Calculation of Thermal Property Values by Use of
Selected Correlations g3 Appendix 2 Saturated Temperature and Pressure 92 Appendix 3 Comparative Evaluation of Selected Correlations with
Selected Values with Focusing on Vargaftik's Handbook .. 94 Appendix 4 Estimation of Specific Heat Ratio K gg
IV
.l..¥EHI ¥1 93 (J~9
Contents
1. Introduction ・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・ 1
2. Selection of Thermal Property Correlations ・・・・・・・・・・・・・・・・・・・・・ 2
2.1 Density ..••••••••••••••••••••••••••••••••••••••••••••••••••• 3
2.1.1 Review of Correlations ......・・・・・・・・・・・・・・・・・・・・・・・・・・・・ 3
2.1.2 Selection.. • .. • • • • • • .. • • • • • .・・・・・・・・・・・・・・・・・・・・・・・・・・・・ 5
2.2 Isobaric Specific Heat ・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・ 8
2.2.1 Revlew of Correlations ......・・・・・・・・・・・・・・・・・・・・・・・・・・・・ 8
2.2.2 Selection ...................・・・・・・・・・・・・・・・・・・・・・・・・・・・・ 11
2.3 Viscosity ・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・ 14
2.3.1 Review of Correlations ・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・ 14
2.3.2 Selection ..................・・・・・・・・・・・・・・・・・・・・・・・・・・・・・ 18
2.4 Thermal Conductivity ........................................ 20
2.4.1 Review of Correlations ・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・ 20
2.4.2 Selection ・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・ 23
3. Comparative Evaluation of Selected Correlations with
Selected Values ・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・ 28
3.1 Review of Selected Value Handbooks and Their Selection
for the Evaluation •••.••..•••.•••••••.••..••.•.••••••••••••• 28
3.2 Comparative Evaluation ・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・ 30
4. Thermal Property Diagram ,...................................... 61 5. Summary ・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・ 74
Acknowledgement ・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・ 79
References .......................................................・・ 80
Appendix 1 Calculation of Thermal Property Values by Use of
Selected Correlations ・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・ 83
Appendix 2 Saturated Temperature and Pressure ・・・・・・・・・・・・・・・・・・・・・ 92
Appendix 3 Comparative Evaluation of Selected Correlations with
Selected Values with Focusing on Vargaftik・sHandbook ・・ 94
Appendix 4 Estimation of Specific Heat Ratio K ・・・・・・・・・・・・・・・・・・・・ 98
IV

JAKHI M 93-029
m m §a ^
c. : £ E J t &
<? : mm.%#-tfMxo%&.$m M • fr?m P EE ± P, ES??EA P, *f6gf?E^J ( f f i E ^ E ^ j t f c l ^ ) ( = P / P . ) P . P mns. R -i&m#£ts( T & s T„ £ ¥ * £ i £ K Tc esfm/g T r *Jt£JM® ( = T / T . ) V t A f t i Vc B**Afl£» v, *W$#t t ( = V/V.) z : E « « *
/c Jt&Jt I »e»* X' •gETCDgife*^
V ttttfRtt u' urE-eotttttttt p ffi S P o B*I*K P r #ag&s (=P, to fltoH?-
V
.L¥EHl -~1 9:l-029
使 用 記t=t 亨7
c. 定圧比熱
q 理想気体状態での定圧比熱
M 分子量
P 圧力
p, 臨界圧力
p, 対臨界圧力〔擬臨界圧力ともいう) (=P/P,)
P .• 蒸気圧
R 一般気体定数
T 温度
Tb 標準沸点温度
T, 臨界温度
T, 対臨界温度 (=T/T,)
V モル体積
V, 臨界モ J~体積
V, 対臨界体積 (=V/Vc)
z 圧縮係数
ギリシャ文字
K 比熱比
λ : 熱伝導率
A' 常庄での熱伝導率
μ 粘性係数
μ・ 常庄での粘性係数
ρ 密度
ρc 臨界密度
ρ, 対臨界密度 (=ρ/ρc)
丘J 偏心因子
V

-IAHKI M * i «»
I. £ x. ft
m$,miz¥&§;frf£timm£titzx&v&Tmm<Mt;M&3L¥Wi&®%.p CHTTR) a.
0,^ifxjplzX'). cJt£ff l&##x£mti-f-5C£:4-<£j 950°C11>nigjgffl&x*.>l^—£ ft 0 Hi I . c©aiB©iBix*>i.4 : r-£ffc£X!g. &Sg^©»&iLTfiJff lLJ:-5£-f3raiWfc t£ffi"cfc-3o
-So c t i l i . S«S* 'x^©$l l i^ { t7K^gJSi*-5^( i5^£**xf fcLT4f iK^t i -5^^>c*m §L£»R. i a f i R « H : i 0 a » 5 l E * t l ; 5 - & r * * t - « f t K * . xBKLMJ?f££j£L, ef t
* a W 8 $ © B * t t * « ± « £ LT l *«11 v i S ,
^ § m ^ < f P I I * ^ ' < - o ^ J ¥ A ^ ± * ^ T i 7 t o -&©-5*.©—-its * ^ t l « K c J : 5 * * / y
^Mffl4-7i^*^m©f»i^i4«niasii. mmmzmi6>btiTi^iimmzmiLLTi^,3,„ L^L , ^ > . * ^ K - o i > T I 2 , S*©fft!att1|[{i»i**^5g$ftT<il'-5t>©©ffllSWc B t t t r f i S K t i i o T i ^ i v , *fc. fk?X*^H-C*«Siac*3g-r :7>N©|j|!lfKtfflJ:-5tt
T<&'30
•e-T. £#(£, *^X^Affl-D«g|5t4-->-Cl^7K^SiScW?l©i6fFffif*T*5**. - »
« U »« t t£ f fMLfc „
1.¥1-:1¥1 ¥1 ~.\ I)~!j
1.まえがき
鹿島趨に望む豊かな白然に固まれた大洗の地で建設か進む高温工学試験研究炉 (HTTR)は.
f!本カ、世界の先陣に立勺て開発を進めている高温骸熱利用を実証することをメインテーマのひと
つとする試験研究用の高温ガス炉である。現住.全地球的な規僕てI寮刻な問題となっている地球
温暖化や酸性i~:î~与の環境問題は,熱エネルギーを作り出すため化石燃料を燃焼させたときに.多
量の炭質量ガス,続黄酸化物等の公害ガスか排出されるのが主たる原因である。高温筏熱帯HDは.
高温ガス炉により,これらの公害ガスを併出することなく約 950・Cという高温の熱エネルギーを
作りHlしこの高温の熱エネルギーを化学工業,発電等の熱源として利用しようとする画期的な
技術である。
高温核熱利m として最も有望復されているのが.水蒸気改質による水素ノメタノ-,~製造であ
る。これは.天然ガス等の軽質炭化水素資源あるいは石炭をガス化して生成されるメタンに水蒸
気を加え.高温t~熱により改質反応を生じさせて水素と一酸化炭素.二酸化炭素を生成しこれ
から二次エネルギー源あるいは化学品等の製造原料として重要な水素及びメタノー,(,を製造する。
この製造プロセス自体は.化石燃料を熱源として化学工業分野で十分実績があり.従って,水蒸
気改質器等の要素技術は擁立しているといえる。
しかし高温ガス炉にこの水素ノメタノール製造システムを緩続するとなると.新たに解決す
べき重要な課題かいくつか浮かび上が「てきた。そのうちの一つが.水蒸気改質による水素/メ
タノー,(,製造システムを高温ガス炉に接続した全体システムが事故時あるいは起動・停止時にど
のような挙動を示すかを正確に表現できる過渡挙動解析手法を開発することでーある。そこで.著
者らは.著者が既に開発したHTTR本体の過渡挙動解析手法 tド・山に基づいて.全体システ
ムの過渡挙動解析手法の開発を進めている。
過渡挙動を正篠に解析するためには,そのシステムの動作流体の密度,比熱.熱伝導率等の熱
物性値を正確に縫算できることが大前提であることは論をまたなL、。水蒸気改質による水素/メ
タノ-)~製造システムでは.その動作流体は.原料であるメタンと水蒸気.並びに.改質により
生成する水素.一酸化炭素及び二酸化炭素,更にはメタノ -J(,が複雑に混合している。これらの
物質のなかで水蒸気の熱物性値推算法は.国際的に認められている方法が既に確立している山。
しかし メタン,水素等については.積今の熱物性値推算法か提案されてはいるものの国際的に
認められるには至っていない。また.化学工業分野で水蒸気改質器プラン kの設計にどのような
権算式を用いているかは企業のknol'l-hol'lに属するため,この推算式を公に知ることは非常に困難
である。
そこで.著者は,本システムの心臓部とな「ている水蒸気改質器の動作流体である水素,一酸
化炭素.二酸化炭素及びメタンについて,設計上並びに過渡解析上重要な熱物性である密度,定
圧比熱.粘性係数及び熱伝導$の推算式を文献調査に基ついて選定し.これを実測データ等と比
較し信頼性を評価した。

.JAKKI M i« (G9
2. MfJHMM©iI£
S i : « b ' i i * - L f c i 6 a i t B « » J W * l < 8 « * i T i f c , c W i . ftcffiE. ^ST®iH!I
<fc'3$llfrt*£< tefi-^fztztb. mm'r-70>t£l-to'8^<»ifc&&bgLtztzit>£&t>tlZo -2f.
dynamic properties) t$feJH#Slt(Transport properties)©£T©f*EJ14tei::*f L"Cli&jt;MS8
ig/g • E^7®iiffl*<iKl^#t)*-5o S I ® : t W 6 , Jgig«l^^*i/:f»i!E!i1±«HSS^®S-A^«ft*i<J;»;i§<. cj- i t .©JitM;
* « f f l t 5 ® A ^ i L l ^ s ^T®a^f4IS(:-o^TMIS[Jf;T-4x.' i t lT^.sti l tTl i ' , j : i>Ct. ttc/ir, zrcDwa. £X0&®i±®tz^i>x%H?timfA%mmj££m^zki±&£tm*<D mmmmmzmtz^xmi&mizt. z<btat. Ajjix<Dm$y><m<Kztzitr'ts:<AJ]
f ^ i O ? ( t ' 5 c i i : 1 o f f l T , c c t i i S f f l L < c i « c t t L f c . f t b O C ^ - S ^ r i f i
$*i-Tl^o«l»it*-Sl»(iS^fi(Selected values) £«m'ft3BII£*ft iJteU *(Digffi£&
L, ±ifi®~@®*#cflgt.LritSS;«-S^-r5o * L T . * * T , «£fgj?5$:coi >t. jg
n£o-r i^^*Wt.^ i r - r§fc* !>, f r » f f l £ f t # l K*Lfc„
- 2 -
J孔ヒHI ¥1 ~I;l O~~
2. 熱物性値推算式の選定
ブ弓シトの過渡挙動解析コー Fに組込む熱物性値推算式は.最低限次の条件を満たすことが要
:1とされる。
j f往算f直の信頼性か高い。
2 計算時間カ、短L、。
,:3, 推算に必要な入力データ量が少なく,計算後上で占める記億領峻か少ない。
これまで,推算式は,上記①を第 1目標に開発か進められてきており.この目標を達成するた
めに推算式の項数を多くしたり.膨大な数表や線図から係数値を求めるように工夫されたものが
多か「た。これら推算式の開発の流れを展望してみると, 1950年代頃までは理論に基き係数を実
測ヂ-7に合うように補正したり.あるいは,対応状態原理や次元解析とい「た方法を用いて物
質に依らない統ーした熱物性値推算式か数多く提案されてきた。これは.特に高圧,高温での測
定Ji法かなかったり.あったとしても測定結度が悪いことなどから.信頼性の高い実測データの
ある物質カ、多くなか勺たため.実測データのない物質への拡張をめざしたためと思われる。一方.
近年は,実測データか増え熱物性データベースが充実してきたため,物質ごとに縫算式が
提案されている場合か多い。近年提案されている推算式を調査してみると.水蒸気改質システム
で対象としている水素.一酸化炭素,二酸化炭素及びメタンに限勺ても.熱力学物性値(Then::J一
小・namicproperties)と銭送係数CTransporlproperties)の全ての熱物性値に対して推算式が関
数形で与えられているわけではない。数表あるいは線図として与えられている場合もある。また,
温度・圧力の適用が狭い場合もある。
当然のことなカ、ら,最近提案された熱物性値錐算式の方か信頼性がより高<.これらの推算式
を採用するのカ、~ましいが.全ての熱物性値について関数形で与えられているわけではないこと.
並びに,全ての物質.全ての熱物性値についてそれぞれ異なる推算式を用いることは混合気体の
熱物性値推算に当た「て混乱を沼くこと.さらには.入力ミスの確率が高くなるだけでなく入力
領岐をより多くとることになるので.ここでは採用しないこととした。代わりに,統一型式で記
述され.上述(D~③を満たす推算式を選定することを基本方針とし.選定した推算式を最近提案
されている推算式あるいは選定値CSelectedvalues)と呼ばれる推薦値と比較し.その信頼性を
評価することとした。本章では,まず,これまでどのような形式の熱物性値推算式が提案されて
きたかを簡単にレビューし,文献等山・山 (6,.山で検討されている信頼性の評価結果を参考に
し上記①~③の条件に照らして推算式を選定する。そして.次章で.選定推算式について.最
近提案されている推算式あるいは選定値と比較し信頼性を評価する。
なお.これらの選定した熱物性値推算式中の各パラメータ.定数か具体的にどの様な数値に
なっているかを明らかにするため.計算例を付録 1に示した。
qru

.IAKKI M tfi IK!!»
2.1 £ JS
2.1.1 i t s ^ © « s
P = ^ r (2.1.1)
: : t , M( i . # i^ [g /g-mol ]T<fc£ 0
affimftoiEA-^-'t^a-jgg C P - V - T ) Mim£<,mt>tix\l>5&vizika.rm-?c
PV = RT (2.1.2) : c t , R : -A$mft;£fSt = 82.056S[ciif • atm/g-mol - K]Q
(i) p - v - rmme>®m ( t t swgiO » £ < © « « # * « . * £ & » © « « * # « L T a S » » © B s H l * « i E U . * » H f t 4 P - V -
TBi f f . j t ^ f f i *L-Cl»5o C O + T ^ f e W ^ T f e O . fr->e©&©BF3E©ga£i:fc-,-0'5© frvan der Waals jHt^LfcUSflJi t ( t t & ^ g i t ) "Cfe-So -e©&. RedlichtKicong-£-teJ6. H A k r o B F f t ^ C © van der Waals i t©&&5t&St*U * t > f c 3 * & 5 ^ £ / r t l * ; * * l - 5
van der Waals^^jgjg t " T § CfflJ: -? fci£*» <tSS-tt->fc«¥tfrft5fc:fi-&A<. BWR (Benedict-Webb-Rubin) ^ K f t S ^ t t o ^ i S i E i a K i S A i f c - C & S o
C * i 6©r t£Wt t t t» ; f re i t *0CKJF-ro (D van der Waalsst
van der Waals It. m( *©E;M** l£K{ i#^ f f l 3 l : J j©# fc ' t f 8^UT§WI !3* l3©-C 'a SHc i f * i t©P£P+a ' V 2 (C^iEL. £ ^ K . ^ © t t B K i a ^ B g - O i a & S f c a a f c ' t t
' > t t t ' © T ' V £ V - b £ g i E U & © i t £ $ . I 8 7 3 ^ « r ^ $ L f c , , , o
fp + ^ ? ] ( V - b ) = RT (2.1.3)
IP*,.
V 2
P = ^ T " " ^ ( 2 L 4 )
27 R2T*. 64 P, «•»•«
- 3 -
.1,¥Ekl ¥1 ~:l Il~~f
2. 1 密度
2.1.1 推算式の概要
密度 ρ[gl.:rrlJ は,モ J~体積{分子容積) V [crr!/g-mol Jと次の関係にある。
M ρ 二 子 、‘,,
咽岡且• ・・且• ?“ ,,、
• • • • • • • • • • • • • • • • ・•
ここで. t¥tは.分子量[g,'g-mollであそ。
理想気体の圧力一モル体積一温度 tP-V-T)関係はよく知られているように次式で表すこ
とができるか.一般の実在気体l;t.この関係からずれるため.補正が必要である。
PV =RT 、,9u
--A 9u
,a・、
• • • • • •
ここで. R ー般気体定数=82.056S[crrl. atm/g-mo卜則。
繍正の方法としては.分子間引力等を考慮.して上式を修正したP-V-T関係を得る方法と.
上式に圧縮係数と呼ばれる補正係数を導入する 2方法がある。
(J) P-V-T関係の修正(状態方程式)
数多くの研究者か.実在気体の特質を考慮して理想気体の法則を修正し,解析的なP-V-
T関係式を提案している。この中で最も有名であり.かっその後の研究の源流となっているの
がvander ¥¥'aalsか提案した関係式(状態方程式)である。その後.RedIichとE削 ngを始め.
何人もの研究者がこの vander Waals式の改良式を提案し,さらなる改良弐かまた提案される
とい「た具合に改良につぐ改良が加えられてきた。
van der Waals式を起源とするこのような流れと異なった解析的な方法が.BWR CBer.edict-
¥¥'ehb-Rubin)式に代表される多項式近似によるん誌である。
これらの代表的な状態方程式を次に示す。
cD van der Waals式
van der ¥¥'aalsは,気体の圧力は実際には分子間引力の分だけ減少して計測されるので理
想気f本式のPをP+a ~ノ V' に修正し.さらに.気体の体積は分子自身の占める体積分だけ
少ないのでVをV-bと修正し,次の式を得. 1873年に発表した..>。
[P +手](V -b) = R T 、,a,
qd
'E・‘9-,,‘、
• • • • • • • • • • • •
即ち.
P=R T a ------V -b V'
...・H ・..(2.1.4)
ここで.
、,,,PD • --a -
q4
re・、
• • • • • • • • • • • • • • • • • ・
。、u

-IAKKI M »3 (>:>»
b = - ~ f (2-1-6)
Tc^CfPeli&^ES^SJS&C/ES^tEAT&^o c © van der laalsiUi. fiH'Ti »£& f l ' ^ / - ? A n \ # t f P c O 2 o , Ell*,. 2 ' < 7 y - j ? S © « f f i * l i i t (tuo paraaeler equation of s ta te)TA5 0 lttirfiSf£(A-e©f£ffi*5*n:i »«»?«fit.(CH:'<*i{±*5A>. *"
•' Redlich Kwong i t £-£©&& van der Waals^©fi©fiiffi-&|fiJ_h$-lt5fcA. tfTISHIAdiS&kiE^i&^-r a V ©
191'J^C Redlichi K*ong fr&%ltzm^-fVM1j&&T$>?, " 0
(V - b) = RT (2.1.7) I 1 ' T 0 5 V ( V + b)
T\
£2, • R ! « T I S
Pc
b = Q , , - R « T c b = P .
Q . = 1
Q . = 9 ( 2 , / 3 - l )
Q> = 2 , y j - 1
3
•• (2.1.8)
• (2.1.9)
(2.1.10)
(2.1.11)
**l £©#?£li, £|[aMbIC^fStfc#-tt*fiF/;-fr^ 11 fe(C&frH?<u£#A-<}-.52f &
Redlich-Kwong i t C i S P . V, T©16A>t>f£iirt32t (2.1.15) (' J: 03c£ § z © t t £ ZRKtfc< t
Z = Z R K + A Z
t S f t U c©Az£*f6SP5ljgJgT, ( = 1 - T c ) &<31ci®%.I£l]PA = p . - ' P c ) , £t> K<ia>©B§tfciLT»*rfo croW&^&lifcfc*. C©#j£liJIHiWTttt,\,
fil'kHitw&SJA-rs^fetLTfcgte©**. PengtRobinsonCJ:Offl*Snfca<itTfe 0 '"" . C*i£ Peng-Robinson-Redlich-Kwcngitt^Ln^c
[ P + V ( V + b ) (
+
T b ( V - - b ) ] <V - b) = RT (2.1-12)
.J..¥EH! :¥1 ~l;;υ~~
b RT, ----8P,
、.Pau
l
ヲ包〆・、• • • • • •
T,及びP,Ii各骨臨界温度及び臨界圧力である。この町ander Waals式は.mいている物
f主パニー ~-7 カ、T,及び p ,の 2 つ. I!/Jち. 2パラ 1ータ型の状態、方程式(t圃oparameler
equation of state)である。推算結度はその後提案されている解街式に比べれば劣るか.尖-
(f気体の挙動を評析的に表現する方法として簡潔であることから. しばしはIfH、られる。
~, RedJich Kwong式とその改良
¥an der ¥¥"aaJs式の縫察病院を向上させるため.分子間引力による袖Aを表わすa V'v")
Jftに改良ぞ加えた状態方程式かその後極キ提案されてきている。この,"で長も釘名なstか.19.1911に RedJic/】と KJ{ollgが提案した次に示す状態方程式である S940
[P +門ふb)J (V -b) = R T 、J守
g-qF-,,、
• • • •
- -司
~ ~ 1...
Q •• RZ .T~5
a p, …・ (2.1.8)
b = ~ b ・R・T,p, )
凸31
内正(
• • • •
Q. 一一」一一9 (2'/'ー 1). (2.1.10)
Qh 二 2'/3.-1 一 -3
.,.・H ・H ・H ・..(2.1.11)
この Redlich-Kwong式の綜lJlをさらに向上させるための改良式か数多く提案されている。
それらの方法は,定数a及びbに温度依存性を持たせるとともに信心因子ωを導入する方法
と,圧縮係数Zを用いてこの値を補正する方法とに大別される。圧縮係数を補正する方法は.
Redlich-Kwong式による P. V, Tの値から後述する弐(乙 1.15)により求まる zの値を
Z RKとおくと
Z=ZR'+~Z
と表わしこのム Zを対臨界温度T,(=1 〆 L)及び対臨界圧力P,(=p /P,), さら
にはωの関数として表わす。この関数か複雑なため,この方法は実用的でなL、。
偏心因子ωを導入する方法として有名なのが. PengとRobinsollにより提案された次式であ
り[I 0 j これを Peng-Robinson-Redlich伽ong式と紘している。
lam l 、I(V -b) = R T V (V + b) + b (V -b) J
H ・H ・..(2.Ll2)
-4 -

.IAKKI M iW 02S»
P = _ R I *<I> (2.1.13) V - b V(V + b) + b(V + b)
a (T)&t f b 0>«l©i?*B(i^(C^-ro 3 BWRit
Benedict. Webb t Rubin {21940ipC. ikl~&tP-o (5HN££> - T I H f i J ^ i g S U f c " " .
P = R T p + [ B , R T + A o - ^ f 1 p ! + 0 , R T - a ) p ' + a a o '
+ ^ ( 1 + r - o 2 ) e x p ( - r P 2 ) (2.1.14)
CcDjUi a . Ao. b . B„. c . C 0 . a & t f 7 © 8 3£&£#«!l1f r t C ^ a 6 5 * H * ' i * 0. ^ I f lWT ' i l ' o Ea*IC ;< ;?>©*§&, 0~350*CT'li, CoopertGoldfrank K < k 3 t c t l £ 8 J&KJi&OHir t tSo
a = 4 . 3 5 2 0 x i o 2 [ U g - m o l ) • atm] A 0 = 1.79894 [ U / g - m o l ) -aim] b =2.52033-<10-3 {{£ /g-mol) 2 ] B o = 4.54625 xiO" 2 [£/g-rool] c =3.58780.x io 3 [ ( i / g - n o l ) 3 • K2 • atm]
C o = 3.18382X10' [ U / g - m o l ) 2 - K 2 - a t m ] a =3.3000xi0" 4 [ U / g - m o l ) 3 ] 7 =1.05000xl0" 2 [ (£ /g -mol ) 2 ]
(2) £Stt*8<r<k.5fifiE
!Et*iStz£igJt. E*^©BStt<tL-C^^-5o
P V = z R T (2.1.15)
SPEAK J: 0S«- rn j f«KCH«t t < - t t f t T S §o tfEIPgg&tmElWAJCJ: 0^*) L/cz£--liS;ft:ESgi*&i»ftf, - E r © t t l 4 « a * 5 l W ± » a t L T 4 ^ ^ n r i » S o
2.1.2 1t*3t<Z>££
5 -
JλElil ~I !I:! り:!!I
J!(Iち.
P-R T a (T) 一一一
V -b V (V + b) + b (V + b) …...・H ・..........… (2.1.13)
a (1')及びbの値の詳細は後に示す。
.~', BWR.rt:
Bened i c 1. WebbとRubinは1940年tこ.次に示すp-ρ(分子密度)-T関係式を提案
した 111)。
P=R町+[Bo R T + Ao-争|ρ'+川 T一山'+aaρ6
十字 (!+rρつ州-rρワ ………… (2.1.14)
この式は a. A o. b. B Q. C. C Q.α及び7の8定殺を各物質ごとに定める必要があ
り.実問的でなt、。因みに. ;1.タンの場合. O~350"Cでは. CooperとGoldfrankによると
これら 8定数は次の値となる。
a =4.3520X ¥0-2 [U' /g-叩J). atm]
A 0 = 1. 79894 [ u' / g-叩J). atm]
b =2.52033:' ¥0-3 [U'〆 g-mol)2)
B 0 = 4.54625 X ¥0-2 [ P. / g-moIl
c = 3. 58780 X W [U: / g-蜘 ))3.K' • atm)
C 0 =3. 18382 x ¥0' ((p. / g-mol)2 . K2 • atm)
α= 3. 3000 X ¥0-' [(p. / g-moJ) 3 )
r = 1. 05000;, ¥0-2 [(p. / g-moJ) 2)
(2) 圧縮係数による補正
実在気体に対しては.理想、気体のP-V-T関係式を次のように舗正し.圧縮係数と呼ぶ補
正係数zを温度,圧力等の関数として与える。
PV = zRT 、‘,,Fa l
--EA
• n4
r、• • • • • • • • • • • • • • • • •
・
zの値は物質の種類によって変わるが.後述する対応状態原理を用いて対臨界温度及び対臨
界圧力により表現すれば物質に関係なく一般化できる。対臨界温度及び対臨界圧力により表わ
したzを一般化圧縮係数と呼び,その値は線図あるいは数表として与えられている。
乙1.2 錐算式の選定
一般化圧縮係数は線図あるいは数表として与えられているため,計算機への入力領岐をかなり
必要とする。さらには, , ~WR式は,密度か温度とともに独立変数となっており,指数関数を含
む複雑な関数で表されているため.この方程式の恨を求めるのは容易でなt、。これに対し.実在
-5ー

JAEHI M 93-029
nfcOikBfi'&jZlt. Peng-Robinson-Redlich-Kmong ©M:*"C-C&*lK. «iL#f£iV«5lif;t£
« i M ^ i : l f » L . mmu. * ^ . H f t f t t t * . ZJMfcttS. y ^ > H { r * i i L r . KIT T^-TPeng Robinson-Redlich-Kwong ©*t£HH'-5o
RT a(T) V - b V (V + b) + b (V - b)
: T ,
P *e*fE*Eatmj P[atml=P[Pa]/l. 013x10s
V ft-ftftlcm -g-mol] T tt#fiff[K] R -«m*^S=82.0568[tnf • atm/g-mol • R] a, b £ S
(2.1.16)
* S P [g/W](i. ± S t © V * ^ T J t K i 0 * * 5 o
p = M/V (2.1.17)
: : t M:5HFS[g/g-mol] a ( T ) . b ( i « T < f c 0 * » 5 o
a(T) = a(T)«a'(Tc) (2.1.18)
[ a(T)]" J = 1 + (0.37464 + 1.54226 w - 0.26992w') x (1 -T'/2) (2.1.19)
a*(T.) = 0.45724 R ' T ; (2.1.20)
b = 0.07780 - ^ - (2.1.21)
P.. T c : f>M&M&tm]RcmnBBZlK]Tmz 1 S c * t i . Tr = T/Tc : *fES^i&K (reduced temperature)
ft&H^wli. # t t * f l a T , = 0 . 7 © i # © * t B * * f t B E P „ . , = P , , / P , 4 ^ * * C
w = - logioP.... - 1.0 (2.1.22)
P.p. ,12, ftlCTjrT Riedel © ^ " 2 , ^ t > * a 6 5 o
£n P . P . , = A" - - ™ - + C"£n T, + D* T.« (2.1.23)
- 6 -
圃・
.J:¥EIiI :¥1 93 -029
気体の状態方程式は.Peng-Robinson守 Redlirh-K.ongの式までであれば.モJ!.体書面Vあるいは密
度ρを独立変殺としているものの3次方程式であり.簡単に健を求めることができる。
以上を総合的に評価し.密度は.水素.一段化炭素,二酸化炭素.Jタン等に共通して.以下
て表すPe目g-Robinson-Redlich-Kwongの式を悶いる。
P-R T a (T) 一一一
V -b V (V + b) + b (V -b) 、.JPO
--a • ・2a• 2
,a
、• • • • • • • • • • • • • • • • •
・
ここで.
P 絶対圧力[atmJ
P [at刷J= P [Pa]/l. 013:<.10'
V モル体積[aIl〆g-回)j
T 絶対温度[Kl
R 一般気体定数=82.0568[cm'.atm!g-moI • KJ
a. b:定 数
密度ρ[g/l1ll'lIま.上式のVから下式により求まる。
ρ= M/V 、.,勾,-EA
--A qι ,e・、• • • • • • • • • • • • • • • • •
・
ここで M:分子量[g!g.moll
a (T). bは以下より求める。
a (T) = a(T)・a・(T.) . (2.1.18)
[ a(T)]円=J -4-(0.37464 + 1.54226ω-0.26992ωつx(l-Tγつ…… (2.1.19)
R2 T~ aO(Tc) = 0.45724 "p:'
RT. b = 0.077田下ア
......・H ・.(2.1.20)
、,J'・AqL ---A
• 9'-r、• • • • • • • • • • • • • • • • •
・
P.. T. 臨界圧力[atml及び臨界温度[K)で第之 l表に示す値。
T,=T/T. :対臨界温度 Creducedtemperalure)
ω=偏心因子
偏心因子ωは.対臨界温度T,=O.7のときの対臨界蒸気圧P...,=P../'P.から次式に
より求まる。
ω=一loglOP..., -1.0 、.Jq4
q4
2且
q4
,,E、• • • • • • • • • • • • • • • •
・
Pv...1ま,次に示す Riedelの式 Z山から求める。
ilnPv..,= A・一芸+C' fl n T, + D' T " 、.,,n
唱
Eaq'u
rz‘、
-6 -

.IAKHI M 93 029
z-c.
A' = -35Q. B" = -36Q. C = 42Q + ««, D- = -Q . Q = 0.0838(3.758- a«) (2.1.24)
ac ©ffifi, &5W>t>;fctf>30 CffliUi. SfUEP.. = 1 [atra] fc/£££K#ff¥*.& i&g (nornal boiling temperature) TrC&wC iA>£. i t (2.1.23) i r T . t L T S t S SSHS**.ST„. ,= T„ T c . c ® t i © P „ . ,= \/ Pc£ftAL-aS6tt7c&<Z>-e*
_ 0.315 T . + f n P . tfc " 0.0838 V , - i n T , , U 1 Z 5 )
T . = -35 + -^- + 42inT b . f - TV,' (2.1.26) 1 b. '
tztzL, *^tK*fLTIi, w=0.0 t-TSo ±.3.izi.zmi£-0.22£te(). g©«Kitfl>
im-?%k, &m-t5mmm%mtzMLTii. w=o.o t i / ; m ^-*>h^M*<« *a*#JyTitt.5©-C, c©f6£fiU8L>t„
Peng-Rob i nson-Red 1 i ch-K*ong©5t(i#;© X 0IC L TU¥ < „
= a ( T ) - P . = _bvP_ , , . , 7 v
i f c § ,
V = x — - (2.1.28)
£ L t x ^ i t S t , Peng-Robinson-Redlich-Kwong©^;(i£(T©3ftitTat>^tl5<,
x s - ( l - /9 2 )x J +( /S , -3 /S 2
2 -2 /8 J )x - ( j3 , . /S J - /8 J
2 - iS J
s ) = 0 (2.1.29)
Cfflx£T[K]. Ptatm], R=82.0568[cnf • atm/g-mol • K] <fc»). ^A^SfVtcBf/g-mon^' *£<;. «Kp[g/crf]*»cS;jr<ko*J6Sct*<r-§5o
p = M/V (2.1.30)
ttfc. 5$ (2.1.29) ^ t . ( i « * 3 o © ^ « * < f f ^ * i S o C©rtt©ffi^iElB-r !*'5A^tfL/c
7 -
• .1:¥1-:1¥1 .:'¥1 93 O~9
ここで.
A' = -35Q. B' = -36Q. C' = 42Q + a ..
D' = -Q. Q = 0.0回8(3.758 -a.) ...・H ・H ・H ・..… (2.1.24)
αcの値は.次式から求める。この式は.蒸気lEP..= 1 [atm1となる温度が標準梯点
温度 (normalboil ing temperature) T bであることから.式(2.1.23)にT,として対臨
界標準沸点T.. T...T c • このときの P..ー I/P.を代入して得られにものであ
る。
a. 、,,z
・・且q'u r、
36 肌 -35+干ご+42ln Tb., -Tb.,' ...・H ・H ・H ・..(2.1.26)
ただし水素に対しては, ω==0.0とする。上式による値は-0.22となり.真の値に近い
といわれているが.古典的な文献山に示されているω=0.0とω=-6.22とした場合を
比較すると,後述する基準選定値に対しては, ω=0.0とした方か.パーセント誤差が概
ね半分以下となるので.この値を採用した。
Peng-Robinson-Redlich-蜘ongの式は次のようにして解く。
β =三笠ヒP s.;:主こ主J ~ R' T. 1"" - R T 、J樗,
q'u • --a
• qL
,s、• • • • • • • • • • • • • • • • •
・
とおき,
…… (2.1.28)
として xを定義すると. Peng-Robinson-Redlich-蜘ongの式は以下のき次式で表わされる。
ピー(1-s.)x. +(β,-3β;-2β,)xー(乱・ムー βi-βn= 0 ・…・・ (2.1.却)
このxとT[K]. P [atm]. R =82. 0568[cof • atm/g-mol・Klより.モJ[.,体積V[cul/g-嗣1]が
求まり,密度ρ[g/coflを次式により求めることができる。
ρ= M/V …...・H ・..…・ (2.1.30)
なお.式 (2.1.29)からは最大3つの実根が得られる。この内どの恨か正解であるか検討した
結果,最大正値の根であることがわか勺たので.この板から密度を推算した。一例を付録 1の
ケース 3に示す。
-7 -

JAEH1 M 93 0>$
2.2 SEifcfc
2.2. 1 Jt f tJtoAS J t » t ( i . i|M±M *©<ai?fflSlg-£ 1 K (=1"C) ±ff£-t*-5©J-.&£fc?**-C;&-->T. ftf*
c*ui. ^E*frTTJD*-rstmm&<D-mmm<Bm-rztzMz&WA.n^<!)ik#tL
r<Dtt&£7£IEIt#kC, <tl'l>. £gT-C©Jt&£££.fcf*C. t l ^ o
dQ = dU + APdV (2.2.1)
: : t , U : rtSPJc*;i^-A : <±*©&Sft
°--(&].-l-s f l4£ z a).-(-&!. «*» : ; T , I : x > ^ ; t t ° i C ^ T . i>?;lhfS©£iK#«;Hfc©<J;?(::j£.5o
d H H h d T + ( - f f l / p (22-3)
dS = dQ/T = dl/T - AVdP/T fr <b,
AS I CP S T ] , T ( 2 - 2 - 4 )
*fc. a * x > * * e G = I - T S 0 £ » f l ' t t « © < * - 5 i c f t S o
dG = dl-d(TS) = AVdP-SdT (2.2.5)
CCT, ttMX, Y, Z©®ICZ = Z (X. Y) 4«Hf f * * * *»J . £&#<!: LT
dZ = MdX + NdY (2.2.6)
U~9 93 五1.J:¥EHl
定圧比無
乙乙 1 推算式の概要
比熱とは,単位質量の物質の温度を 1K (== 1 .C)上昇させるのに必要な熱量であって.気体
の場合には,圧力一定の条件で加熱する場合と容積一定の条件で加熱する場合でその値が異なる。
これは.定圧条件下で加熱すると加熱量の一部は気体が膨張するために必要な外部への仕事とし
て貨やされるのに対し.定容条件下で加熱すると全て温度上昇に費やされるからである。定圧下
での比熱を定圧比熱C.といい,定容下での比熱を定容比熱C.とも、う。
c.を求める方法には.要事力学的にP-V-T関係式から得た式を用いる方法と,実測データ
を統計処理して得た式を悶いる方法がある。 P-V-T関係式としては.実在気体の状態方程式
を飼いる方法と圧縮係数zによる補正式を用いる方法とがある。
(1) 実在気体の状態方程式を用いる方法
気体が吸収した熱量をQとし.気体の仕事は収縮膨張によるものだけとすると.費生カ学の第
一法則から次式カ、成立する。
2.2
、,a'‘
•• ‘
• ?“ -
q4
r・、• • • • • • • • • • • • • • • • •
・dQ = dU + APdV
U:内部エネルギ-
A:仕事の熱当量
こ」で一.
ι=[~手if i o(tJUPV)lp=!?tj,
故に.
、,向
4q,4 “
均
4,,、• • • • • •
‘
• • • ・
ここで. 1:エンタルピ
ところで.エンタJLピSの全微分は次のようになる。
dS = [詳LdT+ [努LdP 、.,,qd
?M
9u
,置、• • • • • • • •
dS == dQ;T == dI;T -AVdPjTから,
(若L=守 、‘,,凋“,qL
9u
,z‘、• •
また.自由エンタルピG=I-TSの全微分は次6むようになる。
、.,,Fhd
qL
q4
r、• • • • • • • • • • • • • • • dG = dI -d (TS) = A V dP -S dT
Zの間にz=z(X. Y)なる関係式があり.全微分としてY. ここで,状態量X.
、.a'戸。勾
49u
,z、• • • • • •
-8 -
dZ = MdX+NdY
と表わすとき.

IAKHI M y;f 029
dU dY
1 = g ' Z
= f dN ] J. dXdY [ dX J, (2.2.7)
&&&*%„ z.oMW.£8&x.s?)l¥(D£1&#a.(ZAti&i:. #CC:*-r*yj^©-)l8:Baff.5t£ I f So
av 5T
as dP
Vt^X, *•>?>lk°S<D£&ftimT<»£Hz:£t>Zti%B
—'^K*l-&].» it (2.2.7) ®mm^.
(2.2.8)
(2.2.9)
3C, = - A T d 2 V
0 P J T " " I dT (2.2.10)
3c 9T
<?'V 5 T 2
(2.2.11)
fflUt L . T * © J ; 9 l c S ^ ^ n - 5 o
(c„-c»T = - T j ; ( ^ dP (2.2.12)
5 T 2 J P
Cg = a + bT + cT 2 + dT s
Cg = a + bT + cT 2
(2.2.13)
(2.2.14)
® Berthelot © t t ! R * S i C « - « ^ 5 * & Berthelot < i f t©t t« l ; f rg5S£l t* LTV >3 " 3 >
0
- 9 -
• !λEhl ¥1 ¥1:1 02!l
[ :手1.=五三子[:~ L 、,守
S?"
qL
,,‘、
か成立する。この関係を自由エンタ J~ ピの全微分式に入れると.次に示す熱力学の一般関係式を
得る。
A [ :~ L ,= -[ :~ L . (2.2.8)
従って,エンタルピSの全微分は以下のように表わされる。
dS = [平JdT -A [ :~ L dP 、.a'ng
q4
9u
,,‘、• •
式 (2.2.7)の関係から.
[ o (号)/叶=寸(~手L
(告L= -AT [ :~~ L • (2.2.10)
仕事の単位が熱の単位として表わされていれば仕事の熱当量Aは不要となり,次式を得る。
|告L叶tizjp 、.J--a 'EA -
q4
• 9&
r、• • • • • • • • • • • • • • • • •
・
従可て,任意の圧力における定圧比熱c.は. P= 0 (理想気体状態〉におけるc.の値弓と
の差として次のように表わされる。
(c. -c仏=ーTJ: [ :引 dP 、J司
41
• 内,
u• 内
'u,g
、• • • • • • • • • • • • • • • • •
・
[問4刊lを肌こ示す問よれうな欄実難在気緋駒体伽の状憾附態肘方程式村求州θT' J p
とができる。
qは,一般に.次に示すように温度Tの3次式あるいは 2次式で表わしている。
C~ a + bT + cT' + dT'
C~ = a + bT + cT'
. (2.2.13)
. (2.2.14)
① Berthelotの状態方程式を用いる方法
Berthelotは次の状態方程式を提案している (13)。
-9 -

I -TV)
• IAKKI - M 93 - 029
(V - b) = R T (2.2.15)
P V = R T + B P (2.2.16)
: : t ,
9RT, _ 54 RTI 128P< 128PcT 2 « ." . i 'v
l o t ,
d>V] _ 81R . TI_ ( 2 _ 2 _ 1 8 )
5 T J j 32 PcT*
tfcO. CP ( i»c^:<}:0^«>Sct*<r '#5o
CP = « + - ^ - ^ f (2.2.19)
c©i t ( i . c£ ^ ^ > E ^ 1 [atm] t © C , £*&«£#« : : , * CfcfcttSas fci&ififg
D van der Waalsit£ffll.>§2ji£ van der Waals ^SSgrs^fcMftroft l&fre^ti&arC'SfrStlS, ,
P + ^ T ( V - b ) = R T (2.2.20)
:r. 97 R 2 T 2 Q
a = " ^ - J 1 p 7 £ - = 3PcVi = -f-T.Vc (2.2.21) , 1 RTc J ^ D 8 Pc 3
±it*E:fi-£fflfcfrTrfiST-C«fl--f**. ft**ff««i
( W ) , = p a* 2ab <2.2.22) P V 2 """ V
S£->T. E*-«©*#TT'© ; e;l /f t :«V©g|gT«rM-r5-Bfi{a»{i»t©J:-5C<C5o
- 10-
' IAEHI -:¥1 93 -029
(P +赤](V -b) = 、.,pb
,
••. • nL
• ?u
,.、• • • • • • • • • • • • • • • • •
・
この式は次のように書き換えることができる。
PV = RT+BP 、.jeu
--且9u
q'u ,e・、
• • • • • •
ここで.
B-9RTc54RTi -ー-一128Pc 128Pc T' 、.J守,--a
向
dq4
,『、• • • • • • • • • • • • •
・
従「て.
I2:エト一旦旦 T~ 。T'I 32 PC T・ H ・H ・(2.2.18)
となり. c.は次弐により求めることができる。
81R P, c. Cg +一一一一一て32 T~
. (2.2.19)
この式は.q!から圧力 1[atmlて‘のc.を求めるときによく使われるが,もともと精度
の良い状態方程式ではないので高圧でのc.を求めるときには注意を要する。
② van der Waals式を用いる方法
van der Waalsが提案する実在気体の状態方程式は次式で表わされる。
[P +剥 (V-b) = RT . (2.2.20)
ここで.
27 R'中za 一一一一ーニ 3PcV~ 一一 TcVc64 PC 、‘,,ー
町
4n4
n4
r、• • • • • • • • •
b -1-R..Tc ~c -----ー8 PC 3
上式を圧力一定の条件下で温度Tで微分すると.次式を得る。
l主 トァ」θT J p a . 2 ab 一 一-V' ・ V'
…・ (2.2.22)
従って.圧力一定の条件下でのモル体積Vの温度Tに関する二階偏微分は次のようになる。
-10-

» • IAKHI M !« UliH
[ 2a 6ab ] f gV ] '
V 2 V 5
[ 2a 6ab 1 f 8V } L v 3 v J 1 a t J,
± iS£ i t (2.2.12) i;ftAL-CE^jP*T!i[5>-r*lli'Cp £f?3o (2) E*«»z*ff l l»fcttB2rBstKJ:*2F8!
* f t a # 0 P - V - THffs&i. EftfEK z &Rjl >T&0<J: -5 I C g ^ S o
V = ^ - z T (2.2.25)
g o t , ( 3 ! V / 3 T ! ) f (i^xCtnc-So
l - T - [ T ( ^ ) P
+ 2 ( w ) J «- 2 " 2 6 > d2 V <3TJ
iSST&D :EE;ftP£[S^rglgT\ RC/ IS^E^Pc T ^ L T S S t f c (itftTcffcLfc) JtEgS £ K T . S c f f l E E ^ E ^ P , T g § * x . ^ ( i ' . C, (±T t S t f P , © r a t f c i L T f c f f l J ^ t c S
(CP-C?)T = -T.J;-g-[T, (-f^-] p i + 2 [ - $ r ] J d P . -(2.2.27) s ACP
/ . CP = C°P + ACP (2.2.28)
ACp ©ttf i*fB§il&ST, t * f f i g ^ E * P t ©Hgt tLT f taT-4^ . t .< lT l ^o (3) *«x -^©«EIHf f iac« t«SHiC* f f l l ' *# t t
latm ^ ' JsET^EJ t f iCp 4-^fflJ-f § c i J i f c f r f c f rgU ' , , C©fca6, £iftPl£Lfc KfflTii. mir-9itm&f&mm&ziMilium) i~m<btir&i), mmroc, <omit
TnfflLtzWlit&i, # j fc¥x- :?Kl fc^ l 'T fh*Lfc i©#*5J: -pT'&.5o
CP (T) = a + b T + c T ! + d T 3 + e T ' ! + f T 3 (2.2.29)
2.2.2 « tg f t© i l£
- 1 1 -
1..¥1-:1¥1 ¥1 ¥1:1 II~~
[h-i生](:i ]: V'v・ loT J
P _ .~, + 2.~~ -y, + -y; 防芸].=
'
…・ (2.2.23)
、.,,au' nL
9-
qL
,.、• n [与一判(評1.
-.. [Pーや+与吋
上式を式(乙乙12)に代入して圧力Pまで積分すればG.を得る。
圧縮係数Zを用いた状態方程式による方法
実在気体のP-V-T関係式は,圧縮係数zを用いて次のように表現する。
(2)
、sa'おnru
内
L,e・、V 号zT
(θ'V/θT')Pは次式となる。
同エ).=手[T [恭子1.+ 2 (長1.J
従って,
、.JFo n4
• q,u
• q,u
rg
‘、• • • • • • • • • • • • • • • •
・•
温度T及び圧力Pを臨界温度Tc 及び臨界圧力Pcで除して還元した(無次元化した}対臨界
温度T,及び対臨界圧力p,で置き換えれば. G. はT,及びp,の関数として次のように表
わされる。
(C. -C仏 -T,J:吾[T,陥与し+2 [表7lp,hpz…(2.2.27)
三LlC.
ムC.の値は対臨界混度T,と対臨界圧力p,の関数として数表で与えられている。
実測データの統計処理による相関式を用いる方法
1 atmより高圧で定圧比熱C.を実測することはなかなか量産しい。このため,文献調査した
範闘では.実測データは理想、気体状態あるいは 1[atmlに限られており.高圧でのC.の値は
見つけることができなかった。さらに,実測データと称主れているものの中には,直接熱量計
で実測したのではなく,分光学データに基づいて計算したものがあるようでーある。
近年.広い温度範囲に渡って.精度良く実測データを相関できるように,次に示す多項式を
適用する場合が多いけれ。
H ・H ・(2.2.28)cg + LlC. C.
(3)
、,,,nv n4
• ?“ • n4
fE
、• • • • • • • • • • • • • • • • •
・C. (T) = a + b T + c T' + d T' + e T・, + fT-'
乙2.2 推算法の選定
圧縮係数zを用いた状態方程式による方法では.膨大な数表データを入力する必要がある。ー
1
・E且

JAKR1-M 93-029
Tlivan dar Waals jt^-ffll'-So Sffimf*tt&!T©q! li. TPRC Data Series' 3 0 ' t r4x." i t lTl >-5S)S©3*it^ffll>5o
C*l£3&^*miIT'§5^»l7 r - ;?a^#fcfe©TNfc.5o C©C*JC^-^§. &EET©C,£3c
® * at H* 100[K] STS400[K]
CS/4.1840 = 1.46910 + 1.60057 X 10"2 X T - 4.44048 x 10" x T 2
+ 4.21220 x 10" x T 3 (2.2 30) 400[K] <TS1500[KJ
CS/4.1840 = 3.56903 - 4.89590 X 10* x T + 6.22549 x 10" x V - 1.19686 X lO"'" X T 3 (2.2.31)
zzr, T : t&tt&miK] © -SSfkK* CO
250[K] STS615[K] CS/4.1840 = 0.256859 - 6.46329 x 10" x T + 1.31865 x 10"7 x T2
- 2.65440 X 10" x T 3 (2.2.32) 615[K] <TS1500[K]
CS/4.1840 = 0.210345 + 9.44224 x 10" X T - 1.94071 x 10" x T2
- 2.35385 x 10 1 2 x T 3 (2.2.33) : : f , T :|ft*fHK[K]
® rjsntmm co 2
200[K] ST^590[K] CJ/4.1840 = 0.105914 + 4.03552 x 10" X T - 3.03235 X 10" X T2
+ 8.29431 X 10" x T 3 (2.2.34) 590[K] <TS1500[K]
CS/4.1840 = 0.135069 + 2.89483 x 10" X T - 1.64998 x 10" x T2
+ 3.53157 x 10" x T 3 (2.2.35) ZZV, T :*6*figJK[K]
@ *?> CH, 270[K]ST^790[K]
CS/4.1840 = 0.458066 - 2.61341 x 10"' x T + 2.07904 x 10" x T 2
-1.25017 x 10" x T 5 (2.2.36)
- 12-
,JAEHI-:"I 9:~ -029
方.実在気体の状態方程式を用いる方法は,積分する必要があり.かっ.モ)~体衝を温度に関し
て二階微分しているため精度が懸念される。また.実測データによる相関式は.高圧について提
案されていない。
以上の状況を考慮し精度について不確かなところがあるが正確なP-V-T関係式を導入す
れは精度が上かることに期待して実在気体の状態方程式による方法を採用する。状懸方程式とし
てはvandar WaaIs式を用いる。
理想気体状態での匂は.TPRC Dala S削 es'30,に与えられている温度の3次式を用いる。
これら 3 次式は信頼できる実測データから得たものである。この~に基づき.高圧での c.を求v
める。
(J)理想気体状態での定容比熱q [J,/g -14]
①水素 H2
100[1¥]壬T孟400[K]
Cg/4.1840 = 1.46910 + 1.60057 X 10-' X T -4.44伺8X 10' X T'
+ 4.21220 X 10・XT' …...・H ・..…… (2.230)
400[1¥] < T 孟1500lKJ
Cg/4.1加o= 3.56卯3-4.89590 X 10・XT+6沼田9X 10-1 X T'
-1.19686 X 10-10 X T'
ここで. T:絶対温度[KJ
② 一酸化炭素 CO
250[1¥]豆T壬615[K]
Cg/4.1840 = 0.256859 -6.46329 X 10-5 X T + 1.31865 X 10-7 X T'
、.,,曾
EA
qd
qL
内
Lr・、• • • • •
-2.65440 X 10-11 X T' . (2.2.32)
615[1¥ ]く T壬1500[1¥)
Cg/4.1840 = 0.210345 + 9.44224 X 10→XT一1.倒071X 10-8 X T'
-2.35お5X 10-12 X T'
ここで. T;絶対温度[K)
③ 二酸化炭素 C02
200[K] 孟T壬590[KJ
Cg/4.1840 = 0.105914 + 4.03552 X 10-4 X T -3.03235 X 10-7 X T'
+ 8.29431 X 10-11 X T' ……・....・H ・..(2.2.34)
、aノqd
。d内
4qL
,s‘、
• • • • • • • •
590[KJ <T孟1500[K J
Cg/4.1倒o= 0.135069 + 2.8拠出 X10-・XT -1.64998 X 10・7 X T'
+ 3.53157 X 10-11 X T' -・… (2.2.35)
ここで. T;絶対温度[1¥J
④ メタン CH4
270[1¥)壬T亘790[K]
CV4.1840 = 0.458侃6-2訓 341X 10-‘XT+2β7卯4XIO-.xT'
-1.25017 X 10-9 X T' ・H ・.....・H ・..(2.2.36)
12

.IAKK1 \ ! !« 029
790iKl<T&1500[K]
CJ/4.1840 = 0.0258866 + 1.60802 x 10 > x T - 6.67069 X 10 7 x T' + 1.06432 x 10'° x T 3 (2.2.37)
: : t , T : « * f f i g [ K ]
cai urn Y.S. TouloukianI and T. Makita. "Thermophysical Properties of Matter vol.6 Specific Heat. Nonmetallic Liquids and Gases." IFI/Plenum. 1970.
(2) SE-CCD/EEEit&C, [ J , g • K]
P - V - T r a ^ t L T . van der Waals * ' H ^ - r - 5 t t S ^ g i C * f f l l \ ftK/rhHE^jPKM
CP = CS + ( A C P ) T x 4.1840
( A C ) T = ( ACp.no : ) T /M/41.3187
(Ac_.)T = -TJ;(4^) pdP.
(2.2.38)
(2.2.39)
d' V 3 T 2 R 2
2a _ 6a»h 1 V s V j
P _ _ § _ + _2ab » 3
r v V s
(2.2.40)
: T . A C . : /5TEEJt&ffl*i& [cal,„/g-K]
A C . . . . , : ^ E E ^ S * © * ^ [on • atm/g-mol • K] M : # - ? i t [g/g-tnolj
a = 3PcV !
' - *
(2.2.41)
(2.2.42)
±^ii*©*f£*rs*3-ro R P
P , V V, T
-&%#•"£%.=82.0568 [en? • atm/gmol • K ]
ELJ] [atm] . fcfc. 1 [atm] =1.013xl0 5 [Pa]
ffi#E* [atm]
t A # l ( # * * » > [cmVg-mol]
B f ^ ^ A f t a i [cm'/g-mol]
[ K ]
1 3 -
¥1 ~j;\ tl:!~1 .1.¥1-:1¥1
、.,,今,qa qL
qL
,,‘、
790['" ]く T;;, 1500[K]
CV4.1制o= 0.02回船6+ 1.6関02x 10 • X T -6.61069 X 10 T X T'
+ 1.06432 X 10-10 X T'
T:絶対温度[K]ここで.
上記(I'~J.'の出典は次の通り。これ以降.参考の便を考え.各推算式の出典をそれぞれの式
の直後に示す。
典〕
Y.S. Touloukianl and T. Makita. “Thermophysical Properties of Matter vol. 6
Specific Heat. Nonmetallic Liquids and Gases." IFIIPlenum. 1970.
出
高圧での定圧比熱C.[J〆 g • KJ
P-V ← T関係として. van der協加Isか提案する状態方程式を用い.次に示す圧力 PIこ関
する績分から求める。
12)
…・ (2.2.38)C. Cg+(~C')TX4.l840
(~C.h = (~Cp_~o h/M/41.3181
(ム C..~o.)T 一T I~ [長円 dP・ …(2.2.39)
…...・H ・..…… (2.2.40)2 (寺子-与手jiぅ1斗 R [Pーや+や),
ムC. 定圧比熱の剰余 [cal t b/g • KJ
ムCP. ..01 定圧分子熱の剰余 [cm• atm/g-mol • KJ
.分子量 [g/g-molJ
ここで,
M
-…… (2.2.41) 3 P<V~ a
上式は次の単位系で表わす。
:一般気体定数=82.0568
:圧力 [atmJ.なお,
:臨界圧力 [atm]
:モA体積(分子容積) [cDI/g-moI]
:臨界モJL体積 [cni/gー即日
温度 [K]
. (2.2.42) b =与
[cul • atnνg-mol • K J
1 [alm] == 1. 013 X lO" [Pa]
R
qo
P
p畠
V
V<
T

JAKH1 M M 029
•5©T. 1 [gmoI j !§£0©&Sfi£W9;£E#?&C, . . . . ©U&AC. .„, Tfc«o caf • aim, g • Ktcal,„/g • K<t©ftgl*&li. «T©t fcOT*-5o
1 Ecal.a/g • K]=41.3187 [cm • atm/g • K ] » < L ^ * n ' J - c a l , h i J £©£»{£&(;*. JKT©£fc0T*5o
1 [cal,„]=4.18-10 [ J ]
1 leal, r] =-1.18680 [ J ]
2.3 ttttffia
2. 3. 1 ffi#*C©ff£
s«a#«t*iJitt-frsJKE-e©fl«tt&5t**£. c t icE*a**so i5* f t * t - .T i^ . in a §& i t
i ) ^•fET'oaait; miE^^^M^O-ffl-EtcfcitSttl l t f^. i i f c # * ^ © « ! i i « i a ( i Enskog-Chapnian ©S
IftjtfCioTtJIi^^dJRto-s.C t ^ T ' § « 0 Enskogt Chapmpan (£. ^ © ( ^ © T T ^ (8I**^l f . LTf i f t f l - T-aii l*»W L.
•5>^(i. f&f9r '^a-FK©»^©** s fc- -S.
• ^T©»^«^( i^ t t« / -e*5o
tttt«»Kit L « l ^ f i C * » f c (1 5>
5 16
Mjrmkryq ( 2 3 1 }
Boltzmann ^ t i k T
fcJ&©«5J-*T, HJftJ^^KSf-f-SQ (=1 ) t©JtTa*3Lfct>©o ) f„ :&IS&»B?- (c©aift©jSK«»JS*»t)-rH-F-e. i.o<cis^ie^t§0 >
- 1 4 -
.J..¥EHI ~[ 9;1 lI:!H
なお.ムc.ι.I は.モ I~体積Vが 1 [g-moIl当たりの体積,即ち分子容衝で定義されてい
るので. 1 [g-moll当たりの熱容量を言う定圧分子熱C......の剰余~C.. ...である。
cui • alm/g • Kとcal..!g • Kとの換算係数は,以下のとおりである。
I [callh/g'Kl=4J.3187 [cm'atm/g'K]
熟化学カロリー cal'bとJとの換算係数は.以下のとおりである。
1 [cal.
なお,国際カロリ -cal.τとJとの換算係数は.以 Fのとおりである。
1 lcal" 1 =4.18680 [J]
2.3 粘性係数
2.3. I 推算式の概要
粘性係数の推算式は.分子運動論に基づき理論的に導いたものと.経験的に得られた知見に基
づき実測データから導いた経験式とに大別される。いずれの方法も.圧力に対する考慮.は,まず
理組気体状態と見倣せる低圧での温度依存式を導き.これに圧力効果を加える方法をとっている。
())理論式
i )常圧での理論式
単原子分子気体の常圧における粘性係数,熱伝導率等の鎗送係数は Enskog-Chap目白日の理
論式によ-,てほほ完全に求めることができる。 Enskogと Chapmpanは.次の仮定の下で分子
問カを考曜、して気体分子運動を解析し
・分子は,希薄で二分子聞の衝突のみがおこる.
.分子間の衝突は古典力学によ司て記述できる,
.全ての分子衝突は弾性的である。
-分子聞の力は分子の中心問で作用し.従って分子間力の場は対称的な球形である.
粘性係数に対し次に示す式を得た<lS}。
μ・_ 5 r (1imkT)川 1一一目 一目
16 IπoQ μ| 、.,,1
9d
?-r・、
• • • • ・
μ・:常圧での粘性係数
k : Boltz岡叩定数
T 温度
a 分子間カ定数
九 -還元衝突積分(分子関カが存在する場合の衝突断面積をzσ2Qとして表わす
ための積分量で,剛体球分子に対する Q (= 1 )との比で表わしたもの。)
fμ :無限級数因子(この理論の無限級数項を表わす因子で. J. 0に近い値をとる。)
多原子分子気体等にこの理論式を拡張するため.種今の分子問ポテンシ十 J~模型が提案され,
分子悶力定数σ,還元衝突積分Quおよび無限級数因子 ιが与えられている。
-14

• IAKK1 M W3 IK!H
ii) Art (A^ft) TOilMi^
£ftOi£l. -#^8i3&©^£%(i .Lt : Boltzmann©iIi!lia£it5$lg#!gKol>TIBl.><tg
n/ V bp [ ( 1 / b P z ) + 4 /5 + 0.7614 • bp*]
i, I 5T, J„, b p * = - ^ | -~~- | - 1 (2.3.2)
: : t , p :
b : '/i-?®£§*SK*hr-SfitiEH?
ZCDiXX'l*. b&Vbp x£;Jca&Tfc<#gA*<&5o £ S* *
i ) -srETOS^st &;SII¥#f^*f£".#£lfS (theorem of corresponding states)**:£«c£-3££ffc©*lSfc$
t<mm^tiXi^i><. Si&W«8l«-fc*>SSffl^^iCittT. Thodos^^»C7t;)g#CS-^^
0) Thodos'ifflftSfStfrSc Thodos<i(i. ill!ii&fr<=>. f&E (moderate pressure) T©mf*©tt14$tfoW£;'j <-<£->
pc vc(c0t^-r5tJtfflaLfc„ ; ; •? , T.. P.. VC ii&*ti#sj£, ES^E^J, es
^ . = a T . T * M c P d v « R ( (2.3.3)
^7L«. fC^m, § £ £ , I ^ H r S ^ f i R t T ' i S ^ t A M i . t<T£?#5=,
.-. a = f - b , b = b, c = 1 - (d + f) = - y , d = -~ - f,
e = - - y ( l + 2 f - d ) = - -g- - f. f = f. (2.3.4)
•!©*££. tett^^wlii^SKjCfi^CfflMstCiOS^-rct^Ti^o
<tr*f = y5z? T? (2.2.5)
• 1.¥1-:1¥1 ¥1 Y;l O~リ
u)高fE(高密度}での理論式
圧力の効果を表現する式としては. Enskogが分子模型として分子問力をもたない剛体球
を仮定し二分子衝突のみを考flして B日ltz回目日の運動論を高密度状態について解いた理
論式か唯一実用化されたものである。粕性係数に対しでは次式で表わす 115)。
μ/μ・=bρ[ O/bρx) + 4/5 + 0.7614・bρxJ
bρx ム r~~, 1 ん ρ,l oT, J 、J9白q
d
内
4,,.、• •
ここで. ρ:密度
b:分子の実容積に対する補正図子
X:分子衝突の修司区因子
この式では. b及びbρXを求めておく必要カ、ある。
12) 経験式
i )常圧での経験式
次元解析や対応状態原理 (theoremof corresponding states)などに基づき多数の経験式
か提案されているが.理論的根拠をもち精度の良い式として.Thodosらが次元解析に基づい
て提案している相関式が有名である。
① Thodosらの次元解析法
Thodosらは,運動論から低[王Cmoderatepressure)での気体の粘性係数か圧力によっ
ては変化せず温度T と分子量MIこ依存することが明らかであり,さ hには臨界定数 T c •
p" V clこ依存すると錐測した。ここで. T c. P c. V cは各者臨界温度.臨界圧力,臨
界モ)~体積である。レーリーの次元解析法をこの関係に適用すると.次式を得る。
μ・ aT8T~ M< p~ V~ R' 、E
,,qU
40
ヮ“,,‘、• • • •
・
次元は,質量m.長さ R.時間r及び温度 tであることから.以下を得る。
ほ汁=仰
a = f-b・b=b. c=l一仙 0=十 d =す-f.
e = -1-( 1 + 2f -d) ==ーす-f. f =え ……H ・H ・..… (2.3.4)
この結果,粘性係数μは次元的には次の相関式により表わすことができる。
μ. f =βz~ Ti
、Jea
今
'u
勾
4J'、
• • • •
ここで.
司、1/.
f =ポ示v3 、‘,,C0
• qu -
n4
rE
、• • • • • • • • • • • • • • • • •
・
FD

I
JAEH1-M 93-029
Z c = W7 : « # £ * « * (2.3.7)
T, = T / T , : * fEP?£g (2.3.8)
A ^ f c O . Thodos^fi. £ t * « K t e l ± # i i £ & © < J : •?«::$*>?-;: t ^ T # 5 1 L f c " 7 > „
* ' f = J8TT (2.3.9)
• * x
-teic iKo^©!»Kffli:-o«±ffl«moKfflfflra*af5F^wca*>tfct#fiffiiit
«t?©<fi* 1 . 0 i - r ^ ! a ^ L T ^ * « l x . a c i : ^ l 4 \ £ fgT l i . reduce) , * fS£ - f5
Thodos'ifi, ^ © ^ f L i ^ ^ I i a ^ S f f l L T ^ f S l l ^ f t f ^ L - C ^ I - ^ ^ j u V w * (T.)
T, S1.0 T'l i
tf* = T
0 9 " (2.3.10)
T, S3.5 T'li
- ^ r y = 1.276 T, 0 M 5 (2.3.11)
1.0<T r<3.5 T © K l i l S g i r * ^ n - C l ^ 0 * M i ^ * « J o T * 4 6 - 5 c t t U T ^ 5 o C ©#arC'f±, tttt&»©i£**a&3©j::-e©&K©T. (cfcij-^^ff^ro^i^tt^S-r
i i ) i i i E T © S ^ i t ® Thodos t> ©&xPff i#CN::* f tSttiBSTIlKg-^ < &!£*£
Thodos'ifi, fifSJS${C*f-T-5 Abas-Zade©fig#""(cS^§, igEr-<i«,4st t tS^» (residual viscosity)** - (t* A<&Ki$H i S#t fK !&Kf f l 6S f?£8©K8£Tg:b ;S ; f t
16-
.JAEHI-:<'I 93-029
Z, P,Vc RTc 臨界圧縮係数 . (2.3.1)
T, = T/T. 対臨界温度 -・・・ (2.3.8)
粘性係数データを検討した結果,無極性気体に対してはμOflまz.1こ依存しないことが明ら
かとなり.Thodosらは.最終的に枯性係数を次のように表わすことができるとした川町。
μ • E βT~ H ・H ・.....・H ・-・ (2.3.9)
そして,化学的性質.極性の有無や分子の形状に基づき,物質を以下のようにグルーピング
し各グループごとに精度良い相関式を求めている。
・無極性気体グループ〔量子効果を考慮する必要かあるヘリウムと水素を除く。)
・ヘリウム
・水 素
・飽和,不飽和及び環状炭化水素化合物
.極性気体
② 対応状態原理
一般に.いくつかの物質の二つ以上の物性の間の相聞を幾何学的に表わしたとき相似性
があるならば.それらの物性を各物質に特有な基準値で還元すれば(還元するとは,基準
値での値を1.0とする物指しで読み換えることをいい,英語では.reduce) .対象とする
物質に共通した一つの関係式を求めることができる。この還元値が等しい状態を対応状態
といい.その状態での従属還元量は物質によらず等しくなる。これを対応状態原理とL、ぅ。
Thodosらは,この対応状態原理を適用して不活性気体に対して次に示すμ・/μ・(T,)
とT,との関係式を得たけ 830
T,三1.0では
一一ι二一=中間17μ・(T,)軍
. (2.3.10)
T,孟3.5では
_-1!二一=1.276T,。制5
μ・(T,) )
--且'・AqJv qL
fE
、• • • • • • •
1.0<T,<3.5での値は原著に示されている図から読み取って求めることとしている。こ
の方法では,粘性係数の値を求めるのにその物質のT,における信頼性の高い粘性係数デ
ータヵ、必、要となる。
証)高圧での経験式
① Thodosらの次元解析並びに対応状態原理に基づく経験式
Thodosらは,熱伝導率に対する Abas-Zadeの関係て 19)に基づき,高圧では剰余枯性係数
(residual viscosity)μ 一μ・か密度と分子量並びに物質の臨界定数の関数とて表わされ
ー16-

.1AKK! M !tt IC\>
(pt-fi") f = fc'p," (2.3.12)
P , = p P c : *fES§^g
Thodost.(i, tfc. *fl£^SI)iillc£^ia*©It*JCfc^S/«,tT,tfflfflBa^atL
(2.3.10) St/ (Z3.ll) !5>t.*J6, T;U^>tco^r*a6fc«'!r(D£E*. gJgtCfcttStt
•5c cfifcT^^KftoaSfKanHL. :iIJi!?fl-^Si#i:T'(i4~5%©ttS-CM3g-C'§
5 : i * i W : . LfrL. =« :F£ :P»*Ktt.5fc. A>L(trJMUtt«a>«^. TORSI* io°D^e ( m»^tL-ciiaeiT''A-i»0
@ Reichenberg irJ:3SEifc5t Thodos-iO^^li. S S - T - ^ ^ ^ ^ t - r S f c M ) . -&©iS*att(iffiffiKlff©«lffiJC
i - ^ T ^ K S S ^ S o Ctilc*fU Reichenberg<il975*p. *f BSf?EE:fi P, t*fEg^g
S T , ©*©H»tLr«*>u #«ttft*»cF«ta#ffli»rftKt>aw"c**»st*»
f. = 1 + (1 - 0.45q) B . P r +
A
( i y 5
c . p ? ) - (2.3.13)
c zv.
A = - ^ - exp(a 2 T; a ) (2.3.14)
B = A(/3,T, - j80 (2.3.15)
C = - | ^ - exp( rt T7r ) (2.3.16)
D = - | j - expU sT— ) (2.3.17)
CCT-PctTc©*fe€-#*[atm] . [K] i-f-Si. *»(*&©£ 9 (Cft So a, = 1.9824 x 10" * a 2 = 5.2682 a 3 = 0.5767 /S, = 1.6552 0, = 1.2760 r , = 0.1319 72 = 3.7035 7, = 79.8678 5 , = 2.9496
17-
.1.¥ト:liI ¥1 リ:1 lI~~
ると仮定し. レーリーの次元解析法を適悶して次の関係式を得た t2 0 ~。
(μ 一μ・)ε=βzfρ …… (2.3.12)
ρ,二 ρ 〆 ρε:対臨界密度
Thodosらは,また.対応状態原理に基づき種キの圧力におけるμ冒とT,との相聞を固とし
て与えているけれ。この図は.上述の剰余粘性係数の栂関式ム基づき.常圧での値は式
(乙 3.10)及び(乙 3.11)から求め.アルゴンについて求めた種身の圧力.温度における鈷
性係数推算値μをμ/μcとして対臨界密度μzに還元しμ,とT,との相関を求めたものであ
る。これをアルゴン以外の物質に適用し,二原子分子気体までは4-596の精度で拡張でき
ることを示した。しかし三原子分子気体になると.例えは二酸化炭素の場合,平均誤差は
1000を超え,推算式としては適切でない。
② Reichenbergによる経験式
Thodosらの方法は,密度データを必要とするため.その縫算精度は密度推算の精度に
よって大きく左右される。これに対し. Reichenbergは1975年.対臨界圧力p,と対臨界温
度T.のみの関数として表わし非極性気体及び極性気体のいずれにも適用できる次式を提
案した (21)。
子=1 + cl -0.45 q) ーー々げ一、 、,a,
の《U
4・且
内
d内
4,,‘、• • • •
ここで.
A=舎町(a,T;a) …・ (2.3.14)
B = A(β1 T,一 β,) 、.,,FD
咽圃
Aqd
n4
r、
• • • • • • • • • • •
c=手2-叫(7, T;1 )
D=争町(o,T-d)
、JPO
--a qd
• 9u
r‘、• • • •
、,J句
4・・a-qd -
q4
,,‘、• • • • • • • • • • • • • • • • •
・
ここでPcとTcの単位を各身 [atm]. [K]とすると.定数は次のようになる。
α 1.9824 X 10-3
α, = 5.2682 α, = 0.5767 β 1.6552
β 1.2760
7 I = 0.1319 7, = 3.7035 7, = 79.8678
ふ=2.9496
-17-

.1AKKI M itt CC:»
Ss = 2.9190 6% = 16.6169
q = 668«(/».)'P. ^ £ftttaf*TI*q=0.0.
2.3.2 «*5&oare mmxtzjiZTj&Titwitz&tigmTgzmmtommit. f E t a . #•?>$> + *
mWZmVHzm^im^UTt-fZZtfr-CZZa S S ; « £ « # ( ± . IfcSMfcSK (normalized temperature)CDMSitLTa*)^n-5*S M S i t t UTT'lift< . & g £ L T ^ X t . t l T l » § 0
C©f;a6. S H M h O A * O f c » O f l « * * * 0 * f i t S . *fc. UGEKft-f 3EnskogfflSII& i tT i i , b&tf b p x t i . T^=i*>©P-V-TS:0 :^14iS^cD^iSlfi{rS'>l»T*i!6«IgtL
ID * m H 2
i) ®n:izbtfzifm&%ii' [Pa • s] T&50 [K]
f' =0.643X10 ' T " 1
( 2 3 1 8 )
: : t , T : & £ [K] 50 [K] <TS1000 [K] --=727 [°C]
U' = 9.071 x 10"' (0.1375T - 1.67)sy! (2.3.19)
: : T , T -.um IK] 1000 [K] iOffiiaTti, S; (2.3.19) £?H*-f 3„
ii) igEEfrfctfSttfi&Sx* [ P a - s ] *fBg§?&l£p, ( = p / p c , p , :Egf?jgg-e©«) (-*fLT, «Jc^,^*«!)-5o &&
p [g.-'cnf] l i£2 . l©{r=it /c^ff i tc i :«J^&§ 0
0.06S 0 r S 3 . O
[( /a - // *) f x 103 + 10" 4]" 4 = 0.10616 - 0.042426p, + 0.17553p ,' - 0.12295p ,' + 0.028149/) / (2.3.20)
: : t , ju* :®EET©*iS1±t*fSc [ P a • s ] U • a»£EAT©tt t t f f» [ P a • s ]
- 1 8 -
ム=2訓 90
δ16.616ゆ
.1.¥とHl ¥1 リ':{ υゴリ
668・(μ.)'P q- Ti e. 非億性気体ではq=O.O。
この式の推算精度は.Thodosらの次元解析法による務度とほぼ同程度とわわれている t目、2.3.2 推算式の選定
理論式による方法で計算した値と信頼できる実測値との偏差は.常圧では.ポテシシャ JL
模型を適切に選べば数%以下とすることができる。還元衝突積分は.基準化温度 (nor回 lized
lemperalure)の関数として表わされるが,関数式としてではなく.数表として与えられている。
このため.計算機への入力のための領綬をかなり必要とする。また.高圧に対するEnskogの理論
式では. b及び bρxは,アルゴンのP-V-T及び治性係数の実測値に基づいて求め線図とし
て与えられてL唱。このため.精度はあまり良くなく.かっ,計算機への入力に適していない。
一方.経験式の中で.対応状態原理による方法では臨界定数以外に臨界温度での粘性係数値を
必要とし,適用できる物質も不活性気体に限られている。
以上の状況を考慮し, Thodosらが次元解析法により得た経験式を選定する。
11)水素 H2
i )常圧における粘性係数μ・[Pa.sJ
TらSO[K]
μ・=0.643 x 10 7 T 0銅
ここで. T:温度 [K]
50 [1¥] < T壬1000[1¥ J = 727 [.C]
μ・=9.071 x 10-7 (0.1375 T -1.67)5/8
ここで. T:温度[1¥1
1000 [K]より高温では,式 (2.3.19)を外挿するo
ii)高圧における粘性係数μ[Pa.sJ
. (2.3.18)
…・ (2.3.19)
対臨界密度 p,(=ρ/ρ 肝 ρ 臨界温度での値)に対して.次式で求める。密度
ρ[g 'cni'Jは第2.1節に示した方法により求める。
O. 06~ρz 壬 3.0
[(μ一μつεxlO'+ 10"]凶=0.10616 -0.042426ρ官+0.17553ρ
-0.12295ρ.. + 0.028149ρJ …… (2.3.20)
ここで, μ・:常庄での粘性係数 [Pa's]
μ :当該圧力での粘性係数 [Pa.s]
-18-

JAHKI M 93 - 029
f = Tc'-'VCM"" Pc 2 y l) (2.3.21) T c :Bg^SS [ K ] P t :G§SE;rj [atm]'
' atra T®i[ 'C*5o 1 [atm] = 1.013 MO5 [ P a ]
M : %?& [g/g-mol]
T\=33.2 [K] P c = 12.80 [K] M =2.0158 [g/g-mol]
O r<0.06IC*fLT(i^; (2.3.20) **Hf-T5o
[fli * ] John A. Jossi. Leonard I. Stiel and George Thodos. "The Viscosity of Pure Substances in the Dense Gaseous and Liquid Phases*. A. I.Ch.E. Journal, vol.8. Na 1 (March 1962). p59~63.
(2) ZMT-K^CO, ^mTftTcozRamitjimcH, i ) aEET'©tti«t#a n' [ P a - s ]
T r S1.5
H' Z = 3.40 x 10-' T V (2.3.22)
1.5<T,S30
ft' f = 1.778 x 10-' (4.58T, - 1.67)5-" (2.3.23)
; : t , f®^^j i± ia ( i )H) c i^bo Cft£©{fc£&©BJll££ltii£2.1filc$ttoT^-fo ZOtefr?. -&f t$c*CO©Tc. P , I4KT©a0o
T c =137.91 [K] Pc = 34.54 [atm]
^ > C H , f f l T t , P . a H T o S ! ? . T , =190.55 [K] P c = 45.45 [atm]
- » f c f t * C 0 t © T , . P« l iHT©a0o To =304.2 [K] Pc = 72.85 [atm]
[ffl A] Leonard I. Stiel and George Thodos. "The Viscosity of Nonpolar Gases at Normal Pressures" A. I.Ch.E. Journal, vol.7. Ka 4(December 1961). p.611 ~-615.
- 1 9 -
ε= T,!/6/(M!/'P,'/')
T,臨界温度 [K]
Pε:臨界圧力 [atm]・
• atmでの値である。
HEiiI-¥1 9:1-029
1 [atml=1.013xWS [Pa]
M 分子量 [g!g-mol]
水素のT" P cは第2.1表に示すように,以下の通り。
L=33.2 [K]
P c = 12. 80 [K]
M =2.0158 [g!g-moll
ρ,く0.06に対しては式(2.3.20)を外掃する。
[出典]
• (2.3.20
John A. Jossi. Leonard 1. Stiel and George Thodos. "The Viscositr of Pure
Subs tances in the Dense Gaseous and Liquid Phases.. A. L Ch. E. Journal.百01.8.
N~ I(March 1962). p59~63.
(2) 二原子分子CO.三原子分子C02及び炭化水素CH.
i )常圧での粘性係数 μ・ [P a • S]
T, ~五1. 5
μ • E = 3.40 x 10寸 T,"!拠
1. 5 くT. ~30
p,* E = 1.778 X 10-7 (4.邸 T,-1.67)5/1
ここで. [.=の定義は上記(l)益)に閉じ。
……H ・H ・.(2.3.22)
-・・・H ・H ・.(2.3.23)
これらの化合物の臨界定数は第乙 1表にまとめて示す。このなかで.一酸化炭素COのT,・
p,は以下の通り。
L = 137. 91 [K]
P c = 34.54 [atml
メタン CH.のTc. P clま以下の通り。
T c = 190. 55 [K]
P c = 45.45 [atml
二酸化炭素C02のT" P ,1ま以下の通り。
L =304.2 [K]
P c = 72.85 [atml
[出典]
Leonard 1. Stiel and George Thodos. “The Viscosity oi Nonpolar Gases at Normal
Pressures' A.I.Ch.E. Journal. vol. 7. N~ 4(December 1961). p.611 ~615.
-19-
•

.JAEKI-M 93-029
i i ) , !5[ETOtt1±#.& U [ P a • s ]
0.02S/o,S3.0
iili- H')? x i o 3 + 1 0 " ] " ' = 0.10230 + 0.023364 p, +0.058533p.* - 0.040758 p .' + 0.0093324 p ,* - (2.3.24)
-»&!%%: Pc =0.301 [g/cof] *• 9 > : /Oc =0.162 [g/cnf]
- » f l ^ * : Pc =0.468 [g/caf]
John A. Jossi. Leonard I. Stiel and George Thodos. "The Viscosity of Pure Substances in the Dense Gaseous and Liquid Phases". A. I.CluE Journal, vol.8. Not 1 (March 1962). p. 59 ~63.
Z4 m&mm
2.4.1 ffftjt<Z>«£ &fc#$®}tf?nEUi. tttt^stra#<c 8iittc#i»fc5tfc. a a c * - * * * * ? - * * *
(i) a n st i ) HTET©3»5S
EnskogiChapnianli. flittl*&K*f-r.53i&5t :£(2.& 1) £;ft*fc©il^L;<53£©T-C
A . 25 r ( a-mkT)" 2
_ h i t t ^ i ( 2 . 3 . D ^ J t g - r - S t . A * t / £ ' i : © f f l J C ^ ( O B i # ^ : * ^ 4 L - C ^ S C i : 3 5 ^ ^ 5 o
[ ( gmkT)" ' 1 J6_ X • L ff ff2 fi„ J 5 f» " /* (2.4.2)
3- f«* T" "H" " ' = T "T c* "" ( 2 4 - 3 ) , » 25 p . . x 3 2 u.
A" = ~M" ( T 0 , 0 0 1 I ( 2" 4- 4 )
- 2 0 -
2.4
.J:¥EHI ~ :¥1 93-029
u)高圧での粕性係数 μ[Pa-s]
0.02~ρ , ~3.0
[(μ一μつεXIO'+ 10-・J'/4= 0.10230 + 0.0おお4ρ,+0.0招533ρf
-0.倒07田ρ"+ O.似)93324ρ,4 ... (2.3.24)
臨界密度ρeは,第2.1表に示す。代表3化合物は以下の通り。
一酸化炭素 :ρ<=0.301 [g/cufJ
ン:ρ<= O. 162 [g/cufJ
二酸化炭素 :ρ<= 0.468 [g/cufJ
タメ
[出典]
John A. Jossi. Leonard 1. Stiel and George Thodos.寸heViscosity of Pure
Substances in the Dense Gaseous and Liquid Phases¥A. I. Ch. E Journa1.官。1.8.
Nn I(Uarch 1962). p.59 --63.
熱伝導率
2.4. 1 推算式の概要
熱伝導率の縫算式は.粘性係数と同様に.理論的に導いた式ι経験に基づき実測データから
導いた式に大別される。圧力に対する考慮の仕方も,まず理想気体状態と見倣せる常圧P=I
[atmlてーの温度依存性を定め,これに圧力効果を加える方法を採っている。
())理論式
i )常圧での理論式
EnskogとChap岡目は,粘性係数に対する理論式,式(2.3.1)を求めたのと同じ仮定の下で
気体分子運動を解析し次に示す単原子分子気体に適用できる熱伝導率の理論式を得た H 針。
25 r (nmkT)'/2 1 =τ::::1'........, IC市 f• .l:'::; L nσ・~~. J
...・H ・H ・H ・-…・ (2.4.1)
上式と式(2.3.I)を比較すると. ,l*とμ・との問に次の関係式が成立していることが分かる。
[J叫 Tyz]πσ2 Q.
16 1 ・5 f. 伊
25 '"' r _ 16 1 ..• _ 5 f. n =一一 C.f,・一一一;:--a~ =一一一一 C.u 32 ~... 5 f.'" -2 f. Vμ
…… (2.4.2)
.....・.......・H ・.(2.4.3)
定容分子熱C.・・01= C.・Mであり.fA!f,μ=1とおいて.次のように書き換えることができる。
λ・~; [をC..mo,) .....・H ・...・H ・..(2.4.4)
-20-

.JAKHI M 9!i 029
M J A* _5_ (2 4 5)
it, (2.4. 5) ©SS^EuckenH^tif^o
%&&£&&?$> 6 tub, ttc£ig?#?affc?ttnstAK©E*#<;*§i\> &fc*^© «F5-«r. 3ti ix*A^-jC«kSfl- U:,>fctatc (A,*.,), lift (At.b) &Cf#^?J©rt:^ iS-g-fflleie (A!.. ,o.) © f t t # x . § t . *Sfc#¥A* (me>J:?(zmtrtzti!><?'£?>0
A* = AT,+(AT„, + AT i b + AT-.,,,,) = AT. + A%, (2.4.6)
t : t ^S-Pa^HMfrKWLTtt. 4U(*?0-?AUtlcfttt-«5t (2. .. 4) £&©<k-5«c£
A* = AT- + A%. = - ^ - ( f . - C . + f i » , C i . , ) (2.4.7)
*HF5>^T( i , C.. .„. = 3 R / 2 T * 3 C t * ^ . i t (2.4. 7) JCfcHT, C,, = 3R - 2. C,„, = C , . . . . - ( 3 R / 2 ) . f , , = 5 / 2 , f , . , = l i : U &©BI#5*;£?#/;0
A* = "if (T R + C w ' ] ( 2 A 8 )
Sffim^^iS^-r-S^r. C . . . . , - C . . , . , = R T ' * 0 . C . . . . / C . . . C = « (JfcftJt) J: *>. A* «•»?©«}:•?ca-TctA'T'^So
A M I 4 L " , = , ° 1 4 C ' — ' J
= "if [ 9 ~ 4 / K l C-" «-4-» *©&. f ,„•= I C t i T f , . ,= 4 / 3 £ f •oSfit-rrt-tf'JKBStt. 9 c © M S * * i 6
M I 4 R + 3 %•' — \X \ A R + O C». » • '
= _ | l [ 7 - ( 5 / 3 * ) ] a n o i ( 2 4 1 0 )
£* l -5" 6 ' o
21
.J..¥I-:I¥I ¥1 9:1 O:!9
あるいは,
M' A・ 55土プ7~2 …(2.4.5)
式〔乙 4.5)の左辺をEucken因子と呼ぶ。
ftl.'・E係数か分子の運動量の輸送を表わすのに対し熱伝導は分子衡実に伴うエネルギーの
交換伝達過程であるため.特に多原子分子気体では内部自由度の影響が大きL、。熱伝導への
寄与を,並進エネルギーによる分 (A; ,)と回転 (λ 二ふ振動(A乙ρ及び分子内の化学
結合の回転 (il人.,..)の和と考えると.熱伝導率λ・は次のように表わすことができる。
λ ・ ""À~ , +O~.t+λ! i b + l. ~ ft.川.)三 λ乙+A ~.t ・H・-…"・…・ (2.4.6)
そこで,多原子分子気体に対しては,単原子分子気体に対する式{乙 ;.4)を次のように書
き換える。
λ ・ =λ~r +λ?na=tf(fHCH+い C山) …...・H ・....・H ・(2.4.7)
単原子分子では. c Y. •• I == 3 R /2であることから.式(2.4.7)において. c ・,=3R
2. C i n. = C Y.・0'一 (3R/2). f.,=5/2. f'o.=1とし.次の関係式を得た。
λ・=よr+R + C""'.' 1 M 1 4 n , "'."'" J H ・M ・.(2.4.8)
理想気体を仮定すると. Cι..,-C.....,=Rであり c...../C.. .., κ〈比熱比〉よ
り ilO を次のように表すことができる。
λ ・ -μ・ r~CD~O' -~C. mo' 1 一一一一一一一一M 1 4 "P.~O ・ 4 山 t J
""....!!:..二 r~ニ互ζιiρ ーM I 4 J "..mu, -・ (2.4.9)
その後 f'n' ==に替えて fi..=4/3とする改良モデルが提案され.d<の改良式が得ら
れた。
λ・ LfヱR + -4-Cv. mo, 1 M 1 4 •• . 3 --..", J
=ft[7-t/3叶C....o, H ・H ・(2.4.10)
この他.分子衝突として非弾性衝突を考えた理論式が提案されているが,式中のパラメータ
計算が非常に複鮫て~り実用的でなL 、。
益)高圧での理論式
圧力の効果を表現する式として実用的なEnskogの理論式は,結性係数と同様に次式で表わ
される (16)
-E且nd

.IAKK1 M i« 029
A / A ' = bpi(l/bpX) + 6 / 5 + 0.757469 bp x] (2.4.11)
<2) n m st i ) -gilEZOmka.
m&mmomm(zm^<mu^t. IMOZHZ. *##<tei£&jav• ©«*©(&©f -
l>5*s aifeWffi9S^t>*.®S©Sl^tLTThodose)*^3i:»Sf&C*^l»Tj|*LT^
ThodostMisicii, * M K 3 * $ * ^ (£4. 9 )(CJjrf £o(Z. tt&tS&T?' (CjQx.T^§»^
s t (2 .3 . 3) (c£E#-f !*C. . .„ , £mHTfc7tMVr£m\ #C©ffiB9i5:£f#fc , M ' .
A * > r = oT:2o l Cp.„ ; 'R d (2.4.12)
: : T ,
f = T ^ M ' V P r (2.4.13)
Z<D*K&&mik?Zt:#>. *®'&. BoytThodosli. IfffiTWSfcaMst+gglC.fcoTg
CH«-r*CtCi»»T«aLT»C3cl»«f*»* fco Wfc. *©«fc-3C4s<Ci:Cj:»>.
A * = aT' T«b P/ V." M c R' (2.4.14)
A ' , t: = tfzJT? (2.4.15)
&£l i . C©ffif53it£**>. ? U : / h > & a ^ * y > © * I I ^ # ^ f l f t (monatomic gas)
A*- f = 9.96 x 10"s [e O M " T ' - -o3Lrr] (2.4.16)
c o ^ S ^ m - P f l - i ^ U f c (diatomic gas) . E.m+ftttfc (triatiomic gas) tcfejgb Jftft£iR«>fcAs T>*-T-<t>;< ^^©^ISTSHFi t f t : (polyatomic gas) Kf tLTt i f i
ft £11. fcttLfcEH*. *B ; Ff l - : Ff t f t©«- : F«Bt t *«WE©*r**<Z)C#L*JB ? # ^ * * T ( i E K H * E * » S t f S » « » t > * 0 . 5$ (2.4.15) ttJBBMtCBUTajB-C
- 2 2 -
.J:¥EHl ¥1 ~I:l U:!9
λ/.A.・=bρW/bρx ) + 6/5 + 0.757469 bρ 必 . (2.4.10
(2) 経験式
i )常庄での経験式
熱伝導率の理論に基づく推算式は.上述のように.大半が給性係数η・の値その他のデー
タを必要とし実用上不便が多4‘。そこで.次元解智子法等に基づく経験式が種キ提案されて
いるが.理論的根拠をもち筒度の良い式としてThodosらが次元解析法に基づいて提案してい
る相関式が有名である。
ThodosとMisicは,熱伝導率が式(2.4.9)に示すように.結性係数7/"に加えて定容分子
熱CV. DlO I あるいは定圧分子熱c.・・01 にも依存することから,粘性係数に対する次元相関
式 (2.3.3)に定圧分子熱c.....01 を加えて次元解析を行い.d<の縮問式を得た l23)。
λ・.r a T~ z~ CP.~o:c Rd 、.,,qL 'A a'
qL
,a‘、• •
ここで,
(= nノ6M'ノZ/P~/三 …………・ (2.4.13)
しかし.上式では,A・を求めるのにCP. .01 の値を必要とする欠点がある。
この欠点を解決するため,その後 RoyとThodoslま,常庄での熱伝導率は温度によって変
わるか圧力には依存しないこと.並びに対応状態原理から鎗送係数は物質の臨界係数と密緩
に関係することに改めて着目して次元解析を試みた。即ち.次のようにおくことにより.
.A.' aTa Tc. P/ Vcd M' R' . (2.4.14)
次の相関式を得た '24>。
λ・.( =βz:' T~ ...・H ・...・H ・....(2.4.15)
彼らは,この相関式をネオン,クリプトン及びキセノンの単原子分子気体 (monatomicgas)
の実測データに適用し,対臨界温度T,の関数として次の実験弐を得た。
γ ・ι=9.96 x 10-5 [ e…一品寸 . (2.4.16)
この方法を二原子分子気体 (diatomicgas) ,三原子分子気体(triatiomicgas)に拡張し
成功を収めたが,アンモニアやメタン等の多原子分子気体 (polyatomicgas)に対しては温
度依存性か異な勺ており精度良い実験式を得ることができなか勺た。
彼らは,失敗した原因が.単原子分子気体の分子運動は並進運転のみであるのに対し多原
子分子気体では更に回転運動及び振動運動もあり.式(2.4.15)は並進運動に限って適用で
きるからであると考えた。そこで,並進運動だけでなく回転運動及び振動運動の寄与を説明
できる方法を考案し.これを炭化水素化合物に適用したほ 51。その方法とは, λ・.?;が並進.
回転及び振動運動の寄与の和として次のように表わされると仮定し.
。,uq4

.1AKH1 M m 029
I
A*- r = (A*- r ) , . + ( A ' « f).o. +(A*« f ) . i b (2.4.17)
(A*- f ) , , l i ^ ; (2.4.15) JCi;-oTS*5^o (A*- r ) . „ , t ( A ' - f) . .b £ # * r t £ © l i t i T ' i l - O T . • l * i £ l o © J O I . - 7 ' £ # ; L X-C^*?-fo A* • r t (A* • f ),,*<
^t.xt^Ei^iasT r t©ra^*i^i*L^o *©&m. mtincixtommTttubzct
X / X , = f(T,) (2.4.18)
: : t ' , X , ( i T , = 1.0 -C©Xffl«[-t;*§„ afc-ili, X, t K ^ ^ T S f t c o ^ C S S ^ B a
ii) mrnvfomfk^ i^E^.ft (dense gaseous region) Rtfm&®&fcmmt&&tzVZ't£< JtfftC. ict>
« c # - r S t ( * n T ( ^ ; 0 LfrU Thodos'i©igE' 2 8 ,#tf«::. PredvoditelevtCiSSlft W&ft< 2 7 '^ t . . *jjfc&fc*tU - A * l±®m<DMm.kLXBt>£tlZ>ctt><B)libfrKte-, fc. -&CT, Thodost.fi. A-A* / ^ J g t t f ^ l : , B S ^ S K c f c ^ f r S f t S £K!gU
( A - A*) iT = /Sz? p? (2.4.19)
ccx, C = V/'Miyl/PY> (2.4.20)
0 = aR 5 / 6 (2.4.21)
2.4.2 itjraose
x^-b(DX: &&m&mw.jSM/g.kmtm\bfrt>. it\odos>bim'£Ltz!kJimvTmzm'3<mw-
fftoiHtot-CHKUBra LTt, 'SfiJMtfr ^ S J l c g S L tza
(1) * * H 2
i ) S E t f f l i £ i $ r [W/ (m • K) ] 0.5ST.S50
( A* f )/418.4 = 44.08 X 10"6 [exp (0.0102T,) - exp(-0.0474T,)] (2.4.22)
: : t ,
- 2 3 -
.J..¥EI¥I ¥( ~:! υ29
λ.. '" = 0... C)" + (λ・.C).D. + (λ・・().i. ……........・H・.(2.4.17)
tλ ・'0..は式(乙4.15)によって表わす。 lλ・・?:).0 t と(A・.O.‘.を分商量する
のは容易でないので.これを 1つのグループと考え.Xで表わす。 λ・・ Cと(A.. ?:入zが
温度に依存することからX も温度に依存すると考え.炭化水素化合物の熱伝導率~iiIfデータ
からXと対臨界温度T,との関係を検討した。その結果,単純に 1本の曲線でまとめること
はできなかったが.メタン以外のエタン,プロパン等のパラフィン類,オレフィン類などは
両対数グラフ上で互いに平行に並んでいることを発見した。そこで.次のような相関式の形
式を提案している。
X/ X. = f(T,) . (2.4.18)
ここで. X,は T,=1.0でのXの値である。彼らは. X,と炭素原子数との悶に密接な関
係があることを発見し. X1の値が未知の炭化水素化合物に対しX1を推算する方法を提案し
てL唱。ただし,彼らの文献中には.メタンに対する実験式は提案されていなL、。
語)高圧での経験式
高圧気体 (densegaseous region)及び液体の熱伝導率は密度だけでなく比熱C.にも
依存するといわれていた。しかし.Thodosらの実験印刷並びに. Predvodi televによる理論
的検討山〉から,剰余熱伝導率λ-A・は密度の関数として表わされることが明らかになっ
た。そこで.Thodosらは.A -A・が密度と分子量,臨界定数により表わされると仮定し.
レーリーの次元解析法を適用して次の関係式を得たほU 。
(λ 一λつr=βZ7ρ? . (2.4.19)
ここで.
r TV'M'/2/P~/3 …・・ (2.4.20)
H ・H ・-・ (2.4.21)β a R5/6
2.4.2 推算式の選定
熱伝導率の推算式は,同じ鎗送係数である枯性係数の推算式と同様な歴史的展開をたどってき
ているので.粘性係数推算式選定と同じ理由から.Thodosらが提案した次元解析法に基づく推算
式を応いる。しかし後らは,水素の高圧での推算式を提案していないので,この推算式だけは,
他の文献の中で関数形で表している推算式から適切に選定した。
(1)水素 H2
j)常庄での熱伝導率λ・ [W/ (m • K) ]
O.5~ T.壬50
( A. n/418.4 = 44.朗 x10-5 [exp (0.0102 T,) -exp ( -0.0474 T,)J ...・H ・.(2.4.22)
ここで,
η3
。L

.JAKKI - M 93 029
C = Tc"*M"VP«"> (2.4.23)
Tc. P. . M©je*SEMlMitt2.3.2(lHCHl;o
[Hi ft] Dipak Roy and George Thodos. "Thermal Conductivity of Simple Gases at Normal Pressures". The Canadian Journal of Chemical Engineering vol.46. April 1968. p. 108-113.
ii) S E T f f l t e » $ ^ [W ' (no • K) ]
A = A' + A A (2.4.24)
A ' : #JEET<Dift£#¥ [W/ (m • K) ] A A : $J&&£*fs [W/ (m • K) ]
200 [K] ST £11250 [K] T'Ji,
A A = 1.163 x 10 ' A (T) • AP (2.4.25)
: ; t .
A(T) == 8.0323 - 7.9882 x 10" T " + 3.7718 X 10" T - 8.9760 x 10" T' 5
+ 8.4080 x 10" T 2 (2.4.26)
AP = P/9.80665 x 104 - 1.03323 [kgf/cnf] (2.4.27)
POmmi. [ P a ] . AP©*te(i[kgf/atf] TfcSo 9.80665xl04(i [ P a ] fr£ [kgf/'crf] ^<Z>#tt*JHMKT'*3o
tlfl ft] BBHJ?. M'S. <H IGHTEX : &&?iJfS y ;? > • Xf— i * S t S # t ± t * « f 3 - K j . JAERI-M 7232 (1977^ 8 fl) .
(2) Z i f » f C O (-»ffcK*> i ) S E T c D ^ f e ^ * A * [W/ (m • K) ]
0.5ST f £10
( A* r)/418.4 = 34.98 x 10" [1.0 - exp( - 0.095T,) ] (2.4.28)
[ffi ft] 2.4. 2(1) i ) Kl^Uo
- 2 4 -
.J..¥EHI. ¥1 93.029
( T, 1/6 M'/'/P,V' . (2.4.23)
Tp 1九.Mの定義及び単位は乙3.2())に同じ。
[出 典]
Dipak Ro}・ andGeorge Thodos. “Thermal COllductivity of Siruple Gases at Nor岨 I
Pressures¥The Canadian Journal of Chemical Engineering vol.46. April 1968.
p.108~113.
話)高圧での熱伝導率.l [W ' (m • 1¥) ]
λ=λ・+a l
A・:常圧での熱伝導率 [W/(m・10]
A λ:剰余熱伝導率 [W/(m • K) ]
200 [K]壬T~ 1250 [K]では.
a l = 1.163 x 10-< A (T). AP
ここで.
-…………・ (2.4.24)
H ・H ・...…・ (2.4.25)
A(T) == 8.0323 -7.嶋田 x10-' TOS + 3.7718 x 10-% T -8.97印 x10-・TI.S
+ 8.4回oX 10-6 T' … H ・H ・-…… (2.4.26)
ap = P/9加 665x 10・-1.03323 [kgf/ CDfJ -・ (2.4.27)
Pの単位は [Pa]. t.pの単位は[kgf/ cnf]である。
9. 80665 x 10'は [Pa]から[旬f/cofJへの単位換算係数である。
[出典]
田所.瀬谷. rHIGHTEX:核熱利用メタン・スチーム改質器特性解析コード
JAERI-M 7232 (1977年 8月).
121 二原子分子CO(一酸化炭素〉
i )常庄での熱伝導率λ・ [W/ (m'K)]
O. 5~ T. ~ 10
(λ. n/418.4 = 34.98 X ¥0-' [1.0 -expC一0.095T,)]
[出典]
2.4.2 ol i )に同じ。
-24-
. (2.4.28)

.JAKR1 M 93-029
ii) &ET®mfcmm* rw./ (m • K> J 0.034/0,40.5
( A - A ' ) r • zc5/418.4 = 14.0 x 10" [exp (0.535p •) - 1 ] (2.4.29)
0.5< ,0 ,42.0
U-H')C' ZoV418.4 = 13.1 x 10" [exp (0.67/>,) - 1.069] (2.4.30)
2.0<p r 42.8
(X- k')C' zcV418.4 = 2.976 x 10" [exp (1.155p,) + 2.016] - (2.4.31)
p r < 0 . 0 3 (Col>-C(2. i t (2.4.29) £*M*L"C*ft.5o
ZZZ'. z« = P , V , / ( R T . ) :&%!£%%%
R : -»m«:^3S=82.0568 [cnf • atm/g-mol • K]
= 8.31441 [nf-Pa/K-g-mol]
- )KYfcK*©VcR^z . ( i {aT©J i ' Jo
Vc = 93.1 [crf/g-mol] zc = 0.295
[ffl A ] Leonard I. Stiel and George Thodos. "The Thermal Conductivity of Nonpolar Substances in the Dense Gaseous and Liquid Regions". A. I.Ch.E. Journal, vol.10. Na 1 (January 1964). p. 26 —30.
(3) zi!ii#-?co2 (.zmmm i ) ftBLrcD&fcmm A *
0. 4 4 T , 4 5
( A * n/418.4 = 6.54 x 10" [exp (0.2826 T.) - exp ( - 0.3876 TV)]
(2.4.32)
[Hi A ] 2.4 2(1) i ) Cllslbo
±102)ii) i ; J : 0 * « > 5 o
(4) C H 4 ( y * >)
i ) utmTonk&om A •
- 2 5 -
• .J:¥EI¥I ¥1 9:J -029
話)高圧での熱伝導率λ[W/(m • K) ]
O. 03~与 ρzZ五 0.5
( λ -Aつ{'. zc' /418.4 = 14.0 x 10-・[exp (0.535ρ , ) 一1 ] …・・ (2.4.29)
0.5<ρ , ~2.0
( λ 一λつc ・zc' /418.4 = 13.1 x 10-・[exp (0.67ρ ,) -1.069] …・・ (2.4却)
2.0< ρ r 三五2.8
(λ-AつC・zc'/418.4= 2.976 x 10-. [exp (1.155ρ ,) + 2.016J …(2.4.30
ρ,<0.03については.式 (2.4.29)を外挿して求める。
ここで.Zc=PcVc/ (RTc) 臨界圧縮係数
Vc 臨界モ)(.,体積
R 一般気体定数=82.0568 [cot'. atm/g-mol • K]
=8.31441 [m'. Pa/K. g-moJ)
一般化炭素のVc及びzc(ま以下の通り。
Vc = 93.1 [cof/g-molJ
Zc = 0.295
[出 典]
Leonard l. St iel and George Thodos. “The Thermal Conductivity of Nonpolar
Substances in the Dense Gaseous and Liquid Regions¥A. 1. Ch. E. Journal. vol. 10.
Na 1 (Januarr 1964). p. 26 -30.
(3) 三原子分子CO2 (二酸化炭素)
i )常庄での熱伝導率λ・O. 4~五 T , ~五 5
( A' 0/418.4 = 6.54 x 10-5 [exp (0.2826 T,) -exp (-0.3876 T /)J
. (2.4.32)
[出典]
2.4. 2 (J) i )に同じ。
話)高圧での熱伝導率
上記(2)ii )により求める。
(4) CH. (メタン)
i )常庄での熱伝導率A・
戸
hu
η'u

JAERI-M 93-029
273 [K] ^TS1270 [K]
A* = - 1.869 x 1 0 ' + 8.727 X 1 0 s T + 1.179 X 10"' T' - 3.614 X 10" T (2.4.33)
; ; T , T : S S [K]
[ffi A ] J.W. Miller Jr. . P.N. Shah and C.L.Yaws. Chem. Eng.. vol.83. Na 25(1976). p. 153.
ii) I E T © i £ l ¥
±§2(2)ii) i c t O ^ a & S o
- 2 6 -
J:¥EHI-:>.I 93-029
273 [K]壬T壬1270[K]
A. = -1.869 X 10-3 + 8.727 x 10-. T + 1.179 X 10-7 T2
-3.614 X 10-11 T' . (2‘4.33)
ここで. T:温度 [K]
[出典]
J.W. Miller Jr.. P.N. Shah and C.L. Yaws. Ch肌 Eng..vol. 83.恥 25(1976).p.153.
ii)高圧での熱伝導率
上記(2Jii)により求める。
26-

1 • IA
KH
I M
93
029
« G
<n
S « 9K
!& ^ •5S L
O in
-=r C
O in
•^r C
O •SJE
» <o
o C
D t^
oo oo
oo t—
C
D
Hd
N C
O C
O C
M
CvJ CXJ
CM
C
M
CM
C
M
Hd
N
o C
D o
o o
o° C
D o
c>
4»B
t& 1CU
t& m
^ <=>
CO
—.
CD
ty^, in
t-^ C
O era
oo C
O in
s ty^,
CD
in co
cx> CTJ
•^
" C
D in
in C
M
CM
C
O
w
r—i
®5 o
CO
CD
, C
O C
M
CO
r-oo
o C
O C
O o
CD
CO
CD
CM
•s*
_> °» O
o C
O •*3*
*—4
CM
C
M
CM
C
M
Bfc^ <=>
o C
D C
D C
D C
D C
D c>
*—'
Bfe £g <i
•R HdS
o -a*
-<a-L
D lO
c—
in O
O 3
HdS C
O C
M
LTJ C
O ^r
^ CT)
•*J-"l
_/
ra CM
c\i
-er o-i
iri od
t-^ tft^
' ' C
O c—
^
-a* "•s*
CO
CO
i£§ SI ix
i£§
ffi C
D oo
o|NJ oo
in C
O C
M
CD
CO
o|NJ C
M
05
CN1 iO
•"# oo
I—1
05
• 1
I C
O in
CM
•^r
CD
to 0
3 in
CO
*£ C
O C
O C
D cn>
CD
CO
CM
C
D
*£ <
—1
en C
O C
O •q
" in
&
Jfl: JI&
' '
05
S 'Hi
CO
CO
t—
t—
c—
CD
—H
c—
r-
ffl- ^
o -y-
,_; -*r
^ -^
,_; C
M
CD
ffl- ^
CM
oo
OS
oo C
O c-
CO
-O
CM
C
M
CO
SS E-
M
—
oo C
D -=3*
CO
o in
CM
o
C2
CO
CD
CD
CO
e o
CD
•*
* c—
CJ3
CM
C
D
^ O
CD
o C
D C
D C
D C
3 —
' '—
' CM
' •rr
CO
-^r C
D o
^ C
O •
^ C
M
"^r C
O ^*
in O
O
<£S
W
X 1
CM
IT to
09 —
—
#
X 1 X
o o
2C X
X X
X .u
c X
o u
o CM
o o
o
W
m
< «*
m* A
A A
A CD B
•.
•o 3K
3K <>•
<N CD
K IN
•o «\
«\ %
h
3=
1 —
N
^ 8
D 1
1 «
c <
1 11
•*> H
^ c
~-*
I -S3 » •+-im
a
•M
« * G
«\ 1
m M
-IN A S '1 :\ A M
4? in
•- C
D
a
•27
-
-一'〆甲いた一
7r-29由
{}NZ
元素及び無機化合物の臨界定数
臨 界 定 数 l臨界o圧z3縮05係数~物質名 化学式 分子量 機準沸点M [g/moIJ 臨界温度臨界圧力臨界密度臨界モル体積
Tb [KJ Tc [KJ I P c [atmJρc [g/crrfJ I V c [crrf/moIJ
n -水素 n -Hz 2.0158 20.39 33.2 12.80 0.0310 65.0
ヘリウム 4 H. 4.0026 4. 21 5. 1889 2.24 0.0698 57.3 0.301
一酸化炭素 CO 28.0104 81. 7 132.91 34.54 O. 301 93.1 O. 295
二酸化炭素 COz 44.0098 194.7 304.2 72.85 0.468 94.0 0.274
メ タ ノ、 CH4 16.043 111. 7 190.55 45.45 O. 162 99 0.288
エタ ン CzHs 30.070 184.6 305.43 48.17 0.203 148 0.285
プロパン C3Hs 44.096 231. 1 369.82 41. 95 0.217 203 0.281
n-ブタン C4H 10 58哩 123 272. 7 425. 16 37.48 0.228 255 0.274
1 -Hexene CsH 12 84. 161 336. 7 503.98 (31. 10) (0.240) (350) 0.263
第2.1:表
p。....,
調d
粘度と熱伝導率ーデータの検索と計算法一」、蒔田 薫著、 「ケミカルエンジニアリング・シリーズ i
(槻培風館発行、昭和50年5月。
典)出

JAERI-.M 93-029
3. mw-^<DM^:mt(Ditmmm
«UM»a*»«-r-5fc»©a:«»^tLTtt. *»7:-.**JiH»s©a<*tt-r*s„ -miT-
ffl*^ffi^K«ottK*©HB*^e«ttlcSUi'ti^O3»<aK«=tt->Tfc0. £ * * « • * « . L^L , & ^ ; c £ < © # | « ! l 7 r - ^ & g £ f t T ( , < 3 ^ t t £ # ; L 3 < > : . -©ftJj|(;:<iKA/<i:ll3fFH,! t f - K * f U : © J S l i S * f t - e < £ l ' . -2f. c«i*-C. 8*©»f?S«3IB§. A^l^f lDWir-* * « * L & « f l : £ f f « © ± . tt»W#f*|jt\ £ « © I M K » < f c « « C J I H » s a t t t t * i L T ©JftlStt (Recommended Values) &%\AZMfc'& (Selected Values)***LTl»S 0 cftt>©
*tt*At^w*fi'Sfrso
3. 1 SE t t«®«K<i : i t t tm i f f i 0SS
s. 1.1 m m
§*nstfe-c?!i^^tiri^©TS§{=A^-rsct*<-C'§5o -n>i!coi>-cssififflfFJS
r{ts$.?&0 z<Dm&, mmi!:tmiiT-?tcDmm&mwLTi>6ztfrgi>0
# (-5 *>&*). 4 # . Hl*}2#) ^gtf , c n « 3 C o ^ T I B ^ t t « i ^ i E * S S n T l ' 5 f i K t E * © mm. ftjfc&ffia$£»isufce***3. i a«=*-r0
* B National Bureau of Standards (%*PJS) ©JlfcttH *tT^*<i955^t*<, 6 ft®^mmmm<%5o
- 2 8 -
園田・
J AEHI -~'I 93 -029
3. 推算式の選定値との比較評価
ここでは,前章で選定した熱物性値錐算式について選定値と比較し.推算精度を評価する。
t髭算精度を評価するための比較相手としては,実測データを用いるのが本筋である。実測デー
タを用いるときにはその信頼性を予め確認しておく必要があり.特に. 1950年頃以前のデータは,
測定方法や試料の純度等の問題から信頼性に乏しいというのが通説にな司ており,注意を要する。
しかしあまりに多くの実測データが公表されている現状を考えると,この作業には膨大な時間
と手聞を要し,この方法は現実的でなL、。一方,これまで,種今の研究機関.大学等が実測デー
タを収集し信頼性を評価の上,統計解析を行い.各種の設計や化学計算に用いる熱物性値として
の推薦値 (RecommendedValues)あるいは選定値 (SelecledValues)を発表している。これらの
推薦値集あるいは選定値集も数多く出版されており.それらを全て収集し,評価するためには膨
大な労力と時間を必要とする。
そこで,文献に比較的多く引用されていて入手が容易であり,かっ,ベースになっている実測
データ等が明磁で信頼性が高いと思われる選定値集を選び,その熱物性値に基き,記載されてい
る実測データのばらつき傾向を考r!して. f詮算精度を評価する。
3.1 選定値集の概要と比較評価用の選定
3. 1. 1 郷要
選定値集はこれまで50を超える膨大な数が出版されているが,それらはいくつかの選定値集の
巻末にまとめて列挙されているので容易に入手することができる。これらについて選定値の作成
方法を調べてみると,次の2通りに大別するとことができる。
(J) 独自に収集しデータベース化している実測データを統計解析して最確式を導き,これに基い
て作成する。この場合,最確式と実測データとの誤差を図解していることが多い。
(2) それまでに学術雑誌等に公表されている熱物性値推算式あるいは選定値集を評価し,引用し
て作成する。ただし.引用した推算式あるいは選定集値の選定理由が明確でないことが多L、。
前者の方法は.膨大な労力と時間を費やすため,限られたわずかの研究機関が行勺ているにす
ぎない。
膨大な数の選定値集の中から特にその名が広〈知れわたっており.信頼性が高いと思われる 6
件(うち海外4件,国内2件)を選び,これらについて熱物性値が記載されている温度と圧力の
範囲,作成方法等を調望ました結果を第3.1表に示す。
これら 6件を比較すると,推算式との比較評価上次の特徴を各今が有していることがわかる。
米国 National Bureau of Stalldards (標準局)の選定値集
発行年か1955年と古く、 6件の中では信頼性が劣る。
一28-

JAKKI M 93 U29
tztiL, ^EJt». temmRv&£mm^^rmfem-t)<5.z-t>tix\,^&i£mwit. « t ^ i©%glCol>THTTR*:^mScM>'X-rA®ffiffljgg|eil (#Jf,~#Jl200 [K] ) £ # ' < -LTl 'So ^iff l-r-?£lR«. l?<ffiLril«»it-&*«>. Z(D3.frZmfem&ffl&LX^Zx, *>-
Bar in © j j ^ f f i m
BAPTAQTHK (Vargaftik, 7 A f f 7 f y ? ) ©ffiil
[K] &mz.ZAU, 1000[bar] J c S 5 ^ E * T ' ^ ^ T V ^ 0 ig^1B<i. iHK*^©5lfflT'*»). *©Xit©^:*liD->Tggr'*-5o ?lffliltt©«*«fll(iHBt.^-p<£^o B ^ t 8 ^ ^ ^ © S ^ t t l t
E**cBBLT«^/j»)i«£E*r«S«[*^Lr^**<. SKIES*!* <. 4/=. - « f cK*C
B*&att3*£©gg*t t
3. 1. 2 S £
TOttKEaaS^j&niSJBTfllSSStlTl'SfflT. ffiE (WCffBE) £ifE<t£#tfTI?« t5©*<S*Li>o - # . ffiffiii. t U S * g S ; t L T < & E ^ ^ ^ E * - e ^ - L r ^ ^ L r i ^ © X, tfc*TigEii3E£#i*T§¥ffiir5i&glittl'o c©**## .L , MfliKie-tfcj&eitfl© fiBf • ffiiJf*Jttt©±. fllJ|cit©it«ff«ir{ift0a£fi«*l6*tLTffli\ fffi©g/£«**>
•fiTE : T P R C f - ? - > ' J - X
-fA©ffiffl»g£|Effl£8Uart/<-LTl''5o SE : B*Jftft14¥£©»e*« r»^14/x> K ? » * j
B£&1Mi^£ (Japan Society of Thermophysical Properties. JSTP) © « £ t t £ l i .
- 2 9 -
圃・・・J孔正HI ¥1 9:1 029
T p r~ Cデータシリーズ
常庄のみで高圧での選定値か与えられておらず.かっ.密度について全く記載されていない。
ただし定圧比熱,粘性係数及び熱伝導率について選定値が与えられている温度範囲は.ほとん
どの物質についてHTTR水蒸気改質システムの使用温度範囲(常温~約1200[K] )をカバー
している。実測データを収集.評価して最篠式を求め,この式から選定値を作成している。ベー
スとな司ている実測データは1950-60年代に得られたものが大半であるので.選定値の信頼性は
高いといえる。
BarInの選定値集
この選定値集は,熟化学的特性を取絞っているため定圧比熱のみが対象となり,かつ,常圧で
の値しか与えられていない。しかし最近出版された選定値集の中ではかなり高温まで記載され
ている。
B APfAφT 11 K (Vargaftik. ワルガフチック)の便覧
一原子分子から有機化合物さらには混合物まで非常に多様な物質について解厳気体を含む気体
状態及び液体状態での密度,熱容量,粘性係数,熱伝導率等約15種の熱物性値を,低温から1000
[K]を超える高温. 1000 [bar ]に至る高圧まで与えている。選定値は.文献からの引用であり,
その文献の大半はロシア請である。引用文献の選定根拠は明らかでなL、。
日本機械学会の選定値集
圧力に関してはかなり高圧まで選定値を与えているカ九温度範囲か狭<.また.一酸化炭素に
ついては気体に対する選定値は飽和状態での値のみが与えられているにすぎなL、。さらには,選
定値作成に用いた推算式の妥当性が明確でない。
日本熱物性学会の選定集値
HTTR水蒸気改質システムで取扱う気体についてかなり高圧まで選定値を与えているが,温
度範聞は日本機械学会の選定値と同様に狭い。選定値作成に用いた推算式の妥当性は明確ではな
いか.第3.2表に示すように,多〈は1980年代に提案された縫算式や選定値集に基づいており,
推算式の信頼性は高いといえよう。
3. I. 2 選定
前章で述べたように,定圧比熱,粘性係数及び熱伝導率の推算式は.低圧下の理想、気体状態
での値に圧力効果を加える形で構築汚れているので,低圧(特に常圧)と高圧とを分けて評価
するのカ、望ましい。一方.密度は,状態方程式として低圧から高圧まで統ーして表現しているの
で.敢えて低圧と高圧を分けて評価する必要はなL、。この点を考慮し,前節に述べた選定値集の
長所・短所を比較の上.推算式の比較評価には次の選定値集を基準として用い,他の選定値集も
参考に比較することとした。
常圧 :TPRCデータシリーズ
TPRCデータシリーズは,選定値カ、与えられている温度範囲がHTTR水蒸気改質シス
テムの使用温度範囲を慨ねカバーしている。
高圧:日本熱物性学会の選定集値「熱物性ハンドブックJ
日本熱物性学会(JapanSociety of Thermophysical Properties. JSTP)の選定値集は.
-29-

JAEHI- M 93-029
^•E©*/T;^*lTl'So L ^ t . CO]®?*-?-.?!*, H # « * £ £ © ri£{fc©t?*<ttt
i>£©-?'"'. B*s»i&tt¥£©3£fl*Kft;LTc©a££Pfc^So mviirfii«g^^rt^^^ie*©«fflfii:oi,«T(i. -*i£T-*3:9i?ai<*ti-a»fci\> -e
c f - ^ f l - x i i ©ifcic fffi -ro
3.2 JttePfffi
© ^ ^ f t » i W ^ * * « f i l t ^ ^ « [ * ( r ^ $ ^ i r i ^ i e t * i t g L f c ^ * * ^ l c ^ - r 0
3.2. 1 $ IS * * . -BMfcK*. nKf tKS&t fy i ' x ro i 'T . J t t t te***8. 1 Bfr 6*3.4 HKJjrfo
cftbO0i:fci<t, ftttf*. S¥^^ffim©f6 ($¥S£f l ) p . . , . fc«Jfc*fr6©* (%JT lit) p . , , . t©S*fc tT^a - r§ '<—b> h?s^(departure) -Tg;bUc*>©T'£>3o
[«**] - mmm%.m] '<—b> ht£M= 100x (3.2.1)
[ £ # 3 £ t t ]
C t l ^©0^"a , ^©Ct*^t,7!i^T'feoo (1) igEfcttStei". Peng-Robinson-Redlich-Kwong ©ttffi#gSK.±3ttJM&£:£*3;efii :
©n. BP*>. <—1> Ms^fc*;L-a^ 0
(2) C©^li(6SfJT^#<, gjaJcS5^«6^«^L.T^50
(4) H T T R * 3 R a a » S r © t t f f l * f t (BPfc. Sf t 300~ftl200 [K] . E * 0.1~» 5.0 [ M P a ] ) T( i , -ftffcft*. - a f k f l t * » t f y ^ > C « f U f t f t j tORSl i . EA 5.0 [MP a] iCfc^T£x_fSSffl!|-Cfc£l2 [°t>] . 800[K] *[email protected]!li5 iitS* 0.5 [96]
tffiT-f-So 1.0 [MPa] WTKlKfUi', #1 >•£(, <0.2 [96] S S T ' * 5 0 *^ i r* f tT<4 , «JM»BEli#HH^fi<tHa 0.1 [96] £ T H 3 o « ± ^ 6 . Peng-Robinson-Redlich-Kwong ©tfcgl^gstli. *3$ii::*f L t ^ ^ l C t f g ^ < g&K
- 3 0 -
... .;;-
' .JAEHI -:-'1 93 -O~9
最近出版されたもので, HTTR水蒸気改質システムで取銀う水素.一酸化炭素.二酸化
炭素及びメタンの気体について,使用温度範囲はカバーしていないがある程度広い温度範
囲で選定値を与えている。ただし二酸化炭素の熱伝導率については.高圧データがなく
常庄のみ示されている。しかし,この選定値データは,日本機銃学会の f流体の熱物性値
集」を引用しており.こちらには高圧データが示されている。そこで,二酸化炭素の熱伝
導率については,日本機械学会の選定値集を基準選定値に選んだ。なお.一酸化炭素の粘
性係数については.科学校術庁が1970年代後半までの実測データを評価し最確式を求めて
いるので!3 5) 日本熱物性学会の選定値集に代えてこの式を基準とする。
旧ソi主で出版されている選定値集の適用性については,これまであまり評価されていない。そ
こで.付録-3に,ワルガフチックの便覧に与えられている熱物性値と選定縫算式並びにTPR
Cデータシリーズ等との比較評価を示す。
3.2 比較評価
水素.一酸化炭素,二酸化炭素及びメタンについて,密度,定圧比熱,粘性係数及び熱伝導率
の選定推算式から求まる値と選定値集に示されている値とを比較した結果を次に示す。
3.2.1 密度
水素.一酸化炭素,二酸化炭素及びメタンについて,比較結果を第3.1図から第3.4図に示す。
これらの図において.縦軸は,基準選定値集の値(基準選定値)ρs・2 と推算式からの値〈推算
f直〉 ρ"t との差を次式で定義するパーセント誤差(deparlure)で表わしたものである。
[推算値]一[基準選定値],{一セント誤差 100><.
[基準選定値] 、J1
0ム
-qd
,,z、
第3.4図以降の比較結果も同様である。横輸には温度をとり,圧カをパラメータとして比較した。
これらの図から,次のことが明らかである。
(J) 高圧になるほど, Peng-Robinson-Redlich-Kwongの状態方程式による推算事直と基準選定値と
の差, /!IJち.パーセント誤差が拡大している。
(2) この差は低温側で大きく.高温になるに従い減少している。
(3) パーセント誤差の温度あるいは圧力依存性は.物質によって異なるが.概ね単調な減少ある
いは増加となっている。
(4) HTTR水蒸気改質器での使用条件(即ち,温度 300~約1200 [K ] .圧力 O.I~約 5.0
[M P a] )では,一酸化炭素,二酸化炭素及びメタンに対し.推算式の誤差は,圧力 5.0
[MP a]においでさえ低温側でも約 2 [。色], 800[ Klを超える高温になると高身 0.5[96]
と低下する。1.0 [M P aJ以下に限れば,せいぜL、0.2[96]程度である。水素に対しては.
推算精度は非常に良く概ね o.1 [96 ]を下廻る。
以上から Peng-Robinson-Redlich-Kwongの状態方程式は.水素に対して非常に精度良〈密度
を推算することができ.一酸化炭素.二酸化炭素及びメタンに対しては水蒸気改質器の設計や熱
物質収支計算等の工学的な観点からは十分な精度で推算できるといえようc
-30-

•JAKKI M ! « (KW
3. 2. 2 £[£Jt& ft£*£££fS3. 5 0^683. BMl^tc C*lt>O0©*t(a)ti. fEi : fc l>TTPRCf-
?> "J - *£&*££« £U van der ft'aals ©£ftti»:(K!EWg^£Jiil'fc«ifffii©fl:K£ /TL/;t>fflTfe5o TPRC^-^v>J-X©jl^iBti, iRHUfc^aif 1-**£!¥« U fi*I
x JOii-oi-Tii. iR«Lf;^i!lf :->©i:jft!S©SA^#v<©f. ^ f l f c i ^ - ^ K S o ^ TiIffi?i{*^Sg-C0^Eit»C^*^«6. Berthelot ©f tS^g i t^m >T*mET©>£flEJt&£ Sf»LTt>5p ;©^46. ^>(Col<Tte*$iJx-;?©&&i£[S(;i:^£*lTl>&H\, Cft-i© lacii. §t.(r«>c©«^tt*©iBt»*Ji^iBt©Jt«{*w-a-c*b-c*5o -- Q&m%\±'f-£ ( J S T P ) © S ^ t t f t r^JH±/%> K7'y7j (Therniophysical Properties
llandbouk) , -Barin ©gjfc'IBS -Vargaftik ®fMH
Boiblli, E ^ ^ ^ y - ^ t L T f t R L f c f c o r . £ ¥ £ £ « ( * r j f t f t t t^> h 7 7 > j c
(1) ' < - •b> h ^ ^ © S S * > S i ' l i I £ * e c # 1 4 l i . ^ S t - ^ T f l t t S ^ . * U a ¥ a t t « ^ * 5
(2) -^CETii. I f f l l a f r ^ l b i l ^ i J : ? ! : , van der Waals ©l*ffi:£gjS£fflt.>fcffi£»li(i. © *g-C§ -SHiSK-r- *©fgS*BEI£> -51 ' (4S^S^1B £ ft&©Jt;£ifi*©tt t ©^fSf f l f i lC f tMa i R i o T f c ' ; . '<—1> r-glTC't>8Ua 0.2 [96] t (^ (Cfe§„
(3) L^U IMffllbb^aj] 41-?<::. }f$r«^£*£jef££©^[±igI£KfcSiairt£:*:LT
fc'L. * * t c ^LT ( i 5.0[MPa]T'^xl.0[?6] SffJCJRioTl^o c©ltfi(gSfl!l
-e^§<, ji5JS(c4--SIC6El>iS U. 800[K]£fi;L3AET&tttt'2.0[?tf]KTKiK£oTtr>
(D - iEft^^trol^Tfi , S©(b)*^$nn^J:-7JC, ft 200 [K] jrfcl»T^E*cfcl» T$;U1j20 [°6] ©/<—b> MgJt#<<&-S®(±. Jg3^©+memttCtt^SC;>©*fflS £*Bfflrti 270 [K] kLLT'i&O. j£-,T 200 [K] T'©ttttffi»it£ffi£fl!'^MS LT^c*
Sifi9l'^:§<4-ori<-5©li. S*:*Lrfc5ggrii^lEffl!|-e«afiIigJglci£<. van der
l 'TteftfiKtE*©H«*#»2IC^-ro tLh^£. van der Waals ©tt£#g^£fflWc;££Ji;j&ffl„f jp$(i, van der Waals ©it®
^o Jtx>*/l.trh(i, eSitT#-r<J:^4-S*t<i«SaTo ^t.S^ES*T'c:©^EJt[gi«'
- 3 1 -
r.;:
• .L¥EIiI ¥1 ~l:l lJ~~
3.2.2 定正比熱
比較結果を第3.5図から第3.8凶に示す。これらの図の中で¥a)は.常圧においてTPRCデー
タシリーズを基準選定値とし. vas der Waalsの実在気体状態方程式を用いた推算値との比絞を
示したものである。 TPRCデータシリーズの選定値は,収集した実測データ等を評価し信頼
するに足ると判断したデータに基づいて導いた相関式から求めている。図の(a)には.この信額で
きる実測データと基準選定値とのパーセント誤差について包絡する範囲を示している。ただし.
/. 7ンについては,収集した実測データの文献聞の差が大きいので.分子構造データ等に基づい
てj里惣気体状態での定圧比熱仁?を求め.serthelotの状態方程式を用いて大気圧での定圧比熱をV
計算している。このため, メタンについては実測データの包絡範囲は示されていない。これらの
図には.さらに次の選定値集の値と基準選定値との比較を併せて示しである。
日本然物性学会 <JSTP)の選定値集 f熱物性ハンドブック JCThermophys j ca 1 Pruper ti es
lIandbouk) •
-Barinの選定値集
-Vargaf t ikの便覧
図の(b)は,圧力をパラメータとして比較したもので,基準選定値は f熱物性ハンドブックJIこ
示されている値である。
これらの図から,次のことか明らかである。
tl) パーセント誤差の温度あるいは圧力依存性は,物質によ勺て異なるか,観ね単調な減少ある
いはt曽加とな「ている。
(21 常圧では.図の(a)から明らかなように. van der I¥'aal sの状態方程式を用いた推算値は.信
頼できる実測データの誤差範囲あるいは基準選定値と他の選定値集の値との誤差範囲内に概ね
収まっており.パーセント誤差でも概ね 0.2[96]以内にある。
(3) しかし図の刷から明らかなように.推算値と基準選定値との差は高圧になるほど拡大して
おり,一般化炭素,二酸化炭素及びメタンでは圧力5.0[MPa]で10[%]を超えている。た
だし.水素に対しては 5.0[MPa]でさえ1.0[9o]程度に収まっている。この差は低温側
で大きし高温になるに従い減少し. 800[1¥]を超える高温であれば2.0[96]以下に収ま勺てい
る。この理由は物質によって異なり,次のとおりと考えられる。
① 一酸化炭素については,図の(b)に示されているように,約 200[K]において常圧におい
てさえ約20[Oó] のパーセント誤差があるのはι算式の中で理想気体に対する~適用温
度範囲が 270[1¥]以上であり,従って 200[1¥]での値は推算式を低温側へ外挿して求め
ており.この外挿精度か悪L、からである。
② 一酸化炭素,二酸化炭素及びメタンについて低温側で高圧になるほどパーセント誤差が
極端に大きくなっているのは.図に示しである温度では高圧倒で飽和温度に近く. vas der
Waalsの状態方程式による推算精度が悪くなるためと考えられる。因みに.これら物質につ
いて飽和温度と圧力の関係を付録2に示す。
以上から. '1an der Waalsの状態方程式を用いた定圧比熱の推算式は. ¥as der Waalsの式の
精度に起因し.高庄・低混側で基準選定値との差か極端に大きくな『ていることが明らかとなっ
た。比エンタルピhは.次式で示すような基準となる温度T。から当該温度までこの定圧比熱を
η
‘u

.IAKK1 M 93 029
m'/tlXMibZo
h(1) = J T CpdT + h(To)+ Ah i : (3.2.2)
: : t , A h , , : S S T , , ( > T o ) -C4-f5ffl^ftx>^AtT
j@S*?ff3- K-Ct i i i ^cco i tx>5 ' / I . f ^ f4 i r^a tLTSJ ' j a -> r i ' -S©T. Jtx>j>A
fcl'TC, £»ff&<f£3r-f-5- t i t l e * b i l o o C © J ; ^ 4 - a f i ^ ' i . van der Waals ©ftS?
3.2.3 ttf£1£»
Jtt&8ft£*a9H^£2S3.12[a(C/;p-fo cnt)©H©*-C(a)(i, B5liIc(sIt;<#E(Cfel^T. T P R C f - i ' 5 ' , ; - X « i W K i < i , . , i U 0 . , , . t L r a ^ « J M B * S l ' J ± f f i © a « « f ; (C4x .^ t lT l^3f f i^ tO. -e©H£'<-~1> \-mMtlT*Uzt><DXfo6o i ^ T P R C £ - r - 9 tk&m-f Z®W£$mX7F Lfco
TPRCr- 9 •> <) -XX'li, &EK*?<;r5f&nfe$J£xi' (i#UC/T;?-Enskog-ChapnianI3©§If& (D *« | -* f L.
*"* = a 2 Q (T*) ( 3 - 2 - 3 )
© -mitmn. r.mitimRv-i9y>,z.nu
»' = 266.93 g / f l
M ^ . ) f. (3.2.4)
a 2Q(T ,)*;5Hio 2fl(T ,)/f ( 1£flfi£T--.J'3fr£ 1 / T © H » t LT£a6, d * i f r £ * £ * 6
- 0 * ^ ^ 1 4 ^ ^ ( J S T P ) © J l ^ f i * r«i«ft/x> K 7 » ? j -Vargaftik ©{g!6 ttfc. Vargaftik fflfIHTIi-ieft;^*©ttf4l?IS16?r^-X.Tl^jgSliffift;&miit L T l ^ fc*. fr;l f>f iBET'4ir i»5(f t©aS«[*t i l :R-C§4frofco
0©(b)li. E * ^ ^ " 7 ^ - ^ t L T f l l « t t i * * a s : e ^ i f c | S ; L f c t 0 r . S * ^ ^ « l * ( i r&&t4^> K ?'•>•? J T -*S 0
C*it>©0^t>, iJt©Ct^8fl 'a.^ -C :*5 0
- 3 2 -
..~
圃'
.JAElil ¥1 93 O:!9
積分して求める。
h(1) = J: C.dT+h(T.)+ ah" 、.a'9-
qF4
qd
,e‘、• • • • • • • •
ここで,ム h" 温度T..(> To)で生ずる相変化エンタルピ
過渡解析コードでは通常この比エンタルピを独立変数として取り扱勺ているので.比エンタJI.
どを精度よく推算することが是非とも必要である。比エンタ J~ ピは上式に示すようにC. を温度
に関し積分して求めていることから.高温での比エンタルピを求める場合であっても.低温側に
おいてc.を精度良く推算することが求められる。このような理白から. ¥an der Waalsの状態
方程式を用いた定圧比熱の推算式は見直しが必要である。
3.2.3 粘性係数
比較結果を第3.9図から第3.12図に示す。これらの図の中で(a)は,前節と同じく常圧において.
TP[{ Cデータシリーズを基準選定値μ"I とし, μ., しとして選定推算値あるいは他の選定値
集に与えられている値をとり.その差をパーセント誤差として示したものである。またTPRC
データシリーズに収録されている測定データと基準選定値とのパーセント誤差を丸印で示し.測
定データを包絡する範囲を斜線で示した。
TPRCデータシリーズでは,常圧における粘性係数μ・は次に示すEnskog-Chapman型の理論
式を用い.
①水素に対し,
Kff μャ =σ2Q (T*) -J
nJ -
qL -
qu
,,‘、• • • • • • • • • • • • • • • • •
・
② 一酸化炭素.二酸化炭素及びメタンに対し.
μ .rMT = 266.93 一一一一一一一一σ2 Q (T・) 、‘,,
a-A4
9d
r、
• •
σ2Q(T・)あるいはa2Q(T・)/f,μを測定データ等から l/Tの関教として定め.これから選定値を
求めている。ただし.関数形は明らかにされていなL、従って,基準選定値が各温度毎に測定デ
ータの平均値を表わしていなL、。更には.測定データがない温度域に外縛している。
常圧においてTPRCデータシリーズと比較した選定値集は次のとおりである。
一日本熱物性学会 (JSTP)の選定値集 f熱物性ハンドブックJ
-Vargaft ikの便覧
なお. Vargaf t ikの便覧では一酸化炭素の粘性係数値を与えている温度は摂氏を単位としている
ため,ケルビン温度で与えている他の選定値集と比較できなかった。
図の(b)は.庄カをパラメータとして推算値と基準選定値を比較したもので.基準選定値集は
f熱物性ハンドブッケ Jである。
これらの図から,次のことが明らかである。
-32-

JAHKI M 93-029
(i) M/E-r-jra^otft.-^ii. MfctsfcoMzmzmmL. jgEJt&osi/rr-^.koa^
« £ © £ * < * £ < <£r>TVS.
a L T L ^ t ( i f l » * < . ^ a j r / i S I J i r - e o ^ J i t e ^ b T l ^ o £ttfcJ'.f«ifi] t LX. —SI ft£**fc< 3S#t:oi«Tli r*«!Jtt^>K7*yi'jSCfVargaffik0fi!3lttTPRC7=-^ i / > J - X « k O < S l ^ ^ f i * % i , r i ^ o *©Hl i . ' * - - t r > h m ^ T ' 3 F ^ l ~ 2 [96] . 6 *TJi**;6*jl000 [K] ©i5fiT'fi3 [?o] T&-5., -SSHfc^illC-^Tfi. ±j£©&*j!r> <bT PRCr- ?>>) -*£&<&&"> b'7 y ? tcblt&LfrrZKfritzfr. m&H&">h' yy?frm^m%.m&5-x-xki). *<omiz. 1200 [KI X%S 2.5 [%] x&z>0 L ^ U M /£-r-*©tfi=>o§aft :#5 [96] £i@/t3C t£%x.tllf. C©gS©H(iF=m«c-r5I5i:
**ai«iej:o<g;<*»Lri^o -&Hti%mi±mz&\.*0 ztnomtt. **a*u±ttfc 5 [°6] WrtJ""R*->Tl»SA<. TkHtcot>T<i, i^igtrttSBifll^HilOOO [K] T'ft6 [°b] , 1200 [K] Tf t7 [96] KJ§LTV-5 0 £ £ i f g^£ffi£L/.:Tho(lost>li. ^HS©
^ - X < b £ o £ * ^ < t ^ y ^ A £ & < 5 0 8 § i © i £ f t © 225.6(T rS1.5)©ttt£{Si5tx-i'K *f LT«l»^ ;©t tS^¥^€l | -C1 .62 [96] . **Kol«Ttt97jSL©M£-r-:?fc:*fL-C1.26 [96] ta#LTi'S""o *»j=a«**fcifc«LT**itfai3Hw*afeLfcRs**«c
±S->TVSfrttT'<fc5*«. 5 [96] gjgffl/*—b> hf^ti&ffgffl&tf-^I^KrtCfilffl© «.S>£l*F.3SinsVL''<^i:<rvL«fc-?o * * « c o l » r . i^fi«. #JC1000 [K] Ja±T'<—fe y hBUS*<5 [96] * ± J i o T l » « © t t . *C (2.3.19) ®aJBS£46H*<611»tlOOO [K] tXX&f), c t i £ W * L T l * 3 C i # I i ! B ' r * S o fcfc'U C©'<~fr> h^H©ie(±iS&*t W tt fe 0 Ji * <. TPRCf-^ i " J -Xt f f i©8£f l | t i<D£f t<H<f lHF*<S£l i l l ^< t©
3.9 0<b)©ffA 0.1 [ M p a ] JC^-TJ:-5IC5 [96] gffiTiRiSirJiifflSftSo
#4x.£*lTV5£ffilBffla<&*600 [K] . 500 [K] tXtm^tzib. HTTRTkH^LSt Sffl©1gBJ&#ffl£IBffiKttoT±ia©c£#W;L5frl±*>^t>fcl\,
(5; J 6 » * 4 : * l 1 i a ^ t t t © a * ' f t E W c t ; l ' T f l K K J : - , T i f © J : 9 C « < 3 S f r * g T * * i : . HTTR*^m*ff i l©ff i f f l*#WT'*n«, *?>£&.£«tta5 [96] jyfiKiR-J-5 iffiS! £ t t § 0 y j ' > l c o ^ T f i , 800 [K] £XX'&tlU'*~k>bWim.X5 [ « ] * i @ * c t ( i ttl»A<. « H C t t « « c a i » S * < 4 t * L T l ' 5 o LfrL. HTTR*l£m&Hfl©ffiffi&#PJ (8)1200 [K] WT) T**tl«10 [96] £ g * . & C i l i f t H o *fc. HTTR*SM*WS§©
^ • - b X # x 4 , i r ^ i 6 5 ^ ^ > © ; e A ^ $ ( i , 1000 [K] £[email protected]&fi«T''Jil0 [96] £ T i o t l ^ C t ^ , C©H*<yn-tr^3(f^©ttft^a»C-^^.5KWi/h$l ' t l>^.So
- 3 3 -
J九EHl :¥1 93 日29
()) 測定データ自身のばらつきは.測定精度の悪さ等に起因し.定圧比熱の測定データよりかな
り大きく 5[00 Jに達する。これが原固となり,基準選定値と他の選定値集の値あるいは錐算
値との差か大きくなっている。
(2) 選;と値集同志の差に着目すると.比較した常庄の場合に限『ても. 3つの選定値集の値はー
致しているとは言い撞く.高温になるほどその差は拡大している。全体的な傾向として.-11量
化炭素を除く 3流体については「熱物性ハンドブックJ及びVargaftikの便覧はTPRCデー
タシリーズより{邸、選定値を与えている。その差は,パーセント誤差で平均 1-2 [96] .最
大では水素か約)000[1¥]の高温で約3[96)である。一酸化炭素については.上述の理由か
らTPRCデータシリーズと熱物性ハンドブックとの比較しかで‘きなかったが,熱物性ハンド
ブックが高い選定値を与えており.その差は. )200 [1¥]で約2.5[96]である。しかし.測
定データのばらつき自体が5[96Jを超えることを考えれば.この程度の差は問題にするほど
でないといえよう。
(3) 選定した推算値と基準選定値を比較すると.常圧においては.推算式は二酸化炭素を絵き
基準選定値より低く推算している。二酸化炭素は逆に高L、。これらの差は.水素以外は概ね
5 [06]以内に収ま「ているが,水素については.高温になるほど差が聞き1000[1¥]で約6
[06] • 1200 [K]で約 7[96]に達している。選定推算式を提案したThodosらは.導出の
ベースとなった水素とヘリウムを除く 50種類の流体の 225点(T.~1.5)の粘性係数データに
対して推算式の精度が平均偏差で1.62 [96] .水素については97点の測定データに対して1.26
[96 ]と報告しているけ引。実際に選定値集と比較してみれば提案者が報告した誤差を大幅に
上廻っているわけであるが. 5 [96]程度のパーセント誤差は改質器の設計等工学的な利用の
観点からは問題ないレベルといえよう。水素について,高温側,特に1000[K]以上でパーセ
ント誤差が 5[%]を上廻っているのは,式 (2.3.19)の適用温度範聞がもともと1000[K]
までであり,これを外挿していることが原因である。ただしこのパーセント誤差の値は絶対
的なものはなく. TPRCデータシリーズと他の選定値集との差が聞く様子が選定推算式との
場合と比較すると似た傾向にあることから.他の選定値集と選定権算式を比較する場合には第
3.9図(b)の圧力 0.1[Mpa]に示すように 5 [96]程度で収まると推測される。
(4) 選定推算式の圧力依存性に関連し.推算式と基準選定値との差は圧力によって大きくは変
わっていない。従って,圧力の効果は選定値集と同程度に精度良く表テれているといえる。た
だし.水素と一酸化炭素については,基準選定値(日本熱物性学会編 I熱物性ハンドブックJ)
が与えられている温度範囲が各者600[K]. 500 [1¥]までと狭いため. HTTR水蒸気改
質器の使用条件の全範囲に渡って上記のことが言えるかはわからない。
(5i 推算値と基準選定値との差が高圧域において温度によってどのように変わるかを見てみると.
HTTR水蒸気改質器の使用条件内であれば,メタンを除き概ね 5[96]以内に収まると推測
される。メタンについては. 800 [K]までであればパーセント誤差で5[96]を超ることは
ないが.高温になるに従い差が拡大している。しかし. HTTR水蒸気改質器の使用条件内
(約1.200[K]以下〉であれば10[96]を超えることはない。主た. HTTR水蒸気改質器の
プロセスガス中に占めるメタンのモJJ,分率は. 1000 (1\]を超える高温域では1O [96]~下
廻勺ていることから.この差がプロセスガスの枯性係数に与える影響は小さいといえる。
。。句。

JAEHI M 93 029
(6) ZMitmmt * ? > i : o i . t > 3S3.11ia<bh 3S3.12ia(b)^t>BiI£^£«fc7lc% S K T = 1.5 T . J :01Sg«!<! : igSf ! tT1 i*« t*? | l«^ i [ t©^©f i !DjAi | | ^oTl^o Cftli, i t (2.3.22) &tf (2.3.23) ©fB£frtf-CS:b-!nifl£T'©tet£&ft/z* © « * i $ # T . = 1.5. EPS. T = 1.5Tc ^*rLTH<C-,-Ct»-5^-C*-5o W ± * * t A 5 i : , M^.Uzlhoios'Ummir^mW.^.OX^SHt. «*»**-??& 5 [96] S S
ififflSfi. X ^ « j c { i f f S ^ * i 5 I E H i r * 5 t i ^ 5 o 8B#WK5 [96] * ± g 5 * - & * < * 5 *<. H T T R * J M * l t S T © t t f f l * f r * * % « - r h « 1 l C H B t t l V i Jift3t©flME€4Mff £ ± r - © ^ - x t « o f c i » < o ^ © S ^ « E * l c o t « T ( i . JtKLfcl6Hl*i-C'ti:fc£fcm±M.S*ifc
^**i-rsfc'vctt<. a«fi«©©iitt*iw*c-r*c t&4tt©Mrr*s.
3. 2. 4 * f i » ¥ Jt&*£*££&13BfrS*&160JCjj;-fo cti'iffligfflff'-eOKi, l5»i:K«l«r. HrJEKfci*
T. T P R C f - ? i / ' J - X * $ * l I i A , . , . i : U A ... . t LT*jQi3M6<6Sl»Jifl&©S ^ « * < ^ ^ t . < T T l » S f i « - t O . *©H*'<—tr> h^^T-a*>Lfcfe©T'*5o H*©*.© »# *H»-e*-r »«©**•*-* t c * t>ff« tH«r*5.
ol*T. ffiS«TlilKIILfc^^af'r-^«-»JC^«>Tfc»). iSSIBTIiGeieriScliafer •">«:: i s ^ M f - ^ t i B f t a ^ i - s c S t f r o ' * , , cc-ri »?*»«£«. *x#& 450 EK] H ±. -BtffcM3l#J 400 [K] Sit. *&>$! 400 [K] £t±tLT^So -SMtJUHKol*Tli,
ffEjrte^rTPRC^-^s/y-xtJtRtfcasfiiiitftotfeOT**. ~B*&4*rt4^£ (JSTP) © £ £ « * rtttttt/x>K:7»*J -Vargaftik ©ffiJI
fcfc. Vargaftik fflffiKTIi. ^ ^ * t y * > © t f c e W « * 5 * T i » S f i * l i « f t * *
mizm-fX 9IC -» fbK^»c-^ l^Tl i t tEKT-C©lfe fe#^f iL*^^^nr i "S l»o H©<b»i. E A * ' < 5 y - * t L T f i » « t J 6 i K i S « * J f c « L f c t , © - e . £*i£/£«fll<i
K7' y ? j #3118 LTI, ' * B*«tft¥&©&1IHm rB6ff©»^ttfi«J « " » * £ * * £ « * t
:neos*^ , »c©ct*«flt.^-c*50
(1) ^Sfl-r-*&#©<££-?£«. «Sttff»i*)«C**<10 [96] «K.Tl»*. ctifi, ft
<2> «««»*«=ismjrttfccn^ntEE-cc^fflx-^tifcK-rii. *Hag««-r-*©tf-i o^fBfflflKifcSo jtfc'L. - » fkK**c -5^ r . 700[K] KT©©ST'*S! |7 r -y©If t .o £®m&$L [96] iex .5S! l»«[* l i»LT^5o Cfilc-oUTH:, I I J f r - ^ C t f S o ^ T C
- 3 4 -
' J:¥EHI ~I 93 ~ 029
(6) 二磁化炭素とメタンについて、第3.11固め}、第3.12固め}から明らかなように、温度T=
1.5 L より低温倒と高温側とで推算値と基準遷定値との差の傾向が異なっている。これは.
式(2.3.22)及び(乙3.23)の組合わせで表わす常庄での枯性係数μ・の縫算式がT.=1.5.
即ち. T=J.5Lを境にして異なっているかである。
以上をまとめると,選定したThodosらが提案する推算式の精度は,概ね最大でも 5[96]程度
と推測され.工学的には許容される範囲にあるといえる。部分的に5[96]を上廻る場合がある
が. HTTR水蒸気改質器での使用条件等を考.. すれば特に問題ない。推算式の精度を検討する
上でのベースとなったL、くつかの選定値集については.比較した範囲内では大きな差は見られな
かったが.比較範囲を超える高温側で差が広がると推測される場合があった。信頼性の高い縫算
式を擁立するだけでなく.選定値集の信頼性を明確にすることち今後の課題である。
3.乙4 熱伝導率
比較結果を第3.13固から第3.16図に示す。これらの図の中で(a)は,前節と同様に.1旨圧におい
て. TPRCデータシリーズを基準選定値λa;.I.とし A....として選定権算値あるいは他の選
定値集に与えられている値をとり,その差をパーセント誤差で表わしたものである。図中の丸印
及び斜線で示す範囲の意味するところも前節と同様である。
TPRCデータシリーズでは.常圧における熱伝導率λ・は.水素,一酸化炭素及びメタンに
ついて,低温側ては;収集した全実測データを基に定めており,高温倒ではGeierとSchafer(31)に
よる実測データと傾向が合うように定めている。ここでいう高温側とは.水素が約 450[K]以
上.一酸化炭素約 400[K]以上.メタン約 400[K]以上としている。二酸化炭素については.
全実測データを基に定めている。
常圧においてTPRCデータシリーズと比較した選定値集は次のとおりである。
一日本熱物性学会 (JSTP)の選定値集「熱物性ハンドブックj
Vargaftikの使覧
なお. Vargaftikの便覧では.一酸化炭素とメタンの熱伝導率値を与えている温度は摂氏を単
位としているため,ケルビン温度で与えている他の選定値集と比較できなかった。また,第3.1
表に示すように.一酸化炭素については常圧以下での熱伝導率値しか与えられていない。
図の(ωは,圧力をパラメータとして推算値と基準選定値を比較したもので.基準選定値集は
「熱物性ハンドブックJである。なお,二酸化炭素については,前述の理由から熱物性ハン
ドブック j が引用している日本機械学会の技術資料 f涜体の熱物性値集(3.)を基準選定値集と
している。
これらの図から,次のことが明らかである。
(1) 実測データ自身のばらつきは.粘性係数より更に大きく 10[96]を超えている。これは.熱
伝導率測定時に試料の伝熱メカニLズムとして対流や熟語射を完全になくすことが難しいためで
ある。
(2) 選定推算式による推算値とこれら常圧での実測データと比較すると.概ね実測データのばら
っき範囲内にある。ただし,二酸化炭素について.700[K]以下の低温で実測データのばらつ
き範囲を数 [96]超える高い値を推算している。これについては,実測データのばらつきが元
-34-

•JAKKI M »:! n^t
(3) * « t t « H * © I S J r S i - r 3 f c . iteLfcSE<o*^»rH->-Cfc. 3o©£5£ffil|©«iA<-l i L r i ' 5 t ( i f l * t ' o 1000 [K] WTtfttKf. Z<t>mit9!ti25 [°o] WFtyriR*->Ti.» •Sri*. 1000 IK] £*§*.•&i^ig-Cti. * ^ t Z L » f f c K ^ © « ^ - © H l i i f e * t . 10 [9o] £*i i 5 * ^ A < * 5 o ttfrTfc. -BffcKlfJCol»r. B # « « ^ £ © rftftofffl&ttftj ©It ^ifili. 7001K] £.i)&&T-&fflT-!?$.mz{&<om%&%<Di£i:*i&<-ftiXisi). 1300 IK] -C<i*>iMi£<e<t©M^40 I«o] Kfcg-TSo c* i« . ri£fr©&&liii«J ©fi*s
*IS(CIil959£p<cflfT$*i/;L. H. Chen©*i« < 3 7 ' i r^$*xT^5^; , BP*>, Keyes ® 5 t ' 3 , )
($3 . 2 £ # M ) £1IH\ »^<£ l» ' r -^A"o^ ; ' f '©^a**a6Tl ' -5^ t .T '*5o * © H ffliJ-r-^©iaffi«il!BA*. #ETI±-117[F] *^607[F] (BP%. 190 [K] J5>£ 319IK] ) Xh';, iSKKoi ^ ^ ^ © S J ^ a i J x - ^ l i i a £/l t*i < *IStctffl<fc 9 ic LT*J&fc©*^
©&»iBmj *«*af^fitLrit«-r5c:tttaar*i't*wfu *£***£*TM El » « H T * £ « * 5 ; f a »5 Vagraf t i k © f l « : * a « > T * * a S t t i : LTl fc«Lfc |S*« t ft 3 C/T-TO tt*>\ rffe!grt±/x > K-7" v ? J T'li. -g*fbK*fflttH#S 11^ b < Keyes ©it •&ftH>Tl>«A*14«&lcoi^r©«*Si4A^fe3|$J:0^<4-oTl^©fi . c©SI#©tt
(4) £5eiggit©GE;*jft*Fl*fei::|J|LT(i. J t i £ t T l ^ S a i g f f l * < f i * r t 200-6001K] £K ^©T"HTTR*^m3cSSff l^ f f i*# i r* fLr t ' -5^ iE«l<s :c t l i i ^<£ i^ . rf&Buft^ > K 7 - y ? j * S * S ^ f i t L T S ^ f i 3 S ^ i t f f l ' < — b > h ^ M ^ f i * - e t > 5 [96] j i i R i o T l ' ^ o L ^ L . ^°—tr> f - ^H©±#^< iE*<cf l c -7T*#<^r>Tl»SCt*^ , & £ #
uuitsktot. m^itzmm^ommu. «*»**-et>5 t%] satfiHani-c. x^«
©li't.-o#«-ffi ;«-rSfcJ61t®fi©iSl^^^iS<cJ:«g|i8d5 i-^©M<£5S»A^S"r*>0.
- 3 5 -
• .JM:I<I ¥1 !l:l II~!I
キ 10[00] 11上あることを考えれは,実測データを更に積み重ねていけば,ぱらつき範囲内に
入ることか考えられるので.この観察結果をも 4 てき定錐算式を否定するのは早計であろう。
(3) 選定値集同,志の差に着目すると.比較した常圧の場合に限司ても. 3つの選定値集の値がー
霊堂しているとは言い量産t、。 1000[1¥]以下であれは.この差は概ね 5 [00]以内に収まってい
るか. 1000 1 K]を超える高温では.水素と二酸化炭素の場合この差は拡大し. 10 [?b]を超
える場合がある。なかでも.二酸化炭素について,日本機械学会の rDi:体の熱物性値集jの推
定値は. 700[1¥]より高温で実測データ並びに他の選定値集の値と大きくずれており. 1300
[ K]では基準選定値との差か40[00]にも達する。これは流体の熱物性値集j の値が,
実際には1959年に発行されたし 11.Chcnの文献はτ"こ示されている式,即ち.Keyesの式 l38)
(第3.2表参!!のをruい.数少ないデータから式中の定数を求めているからである。 その実
測データの温度範図が,常圧では一1I7[F Jから607[F J (即ち. 190 [I¥Jから 319[KJ )
であり,高圧についてはこの当時実測データはほとんとなく実際にどのようにして求めたのか
明儀には言及していない。
このことから,二酸化炭素の熱伝導率については熱物性ハンドブックj あるいは「流体
の熱物性値集Iを基準選定値として比較することは適切でないと判断し.常圧から高圧まで幅
広い範囲で選定値を与えている Vagraftikの便覧を改めて基準選定値として比較した結果を付
録 3に示す。なお熱物性ハンドブック Jでは.二酸化炭素の粘性係数も同じく Keyesの式
を用いているが粘性係数についての信頼性が熱伝導率より高くなっているのは.この当時の粘
性係数実測データか熱伝導率データより多かったからであると考えられる。
(4) 選定推算式の圧力依存性に関しては,比較している温度範囲が最大でも 200-600[1¥]と狭
いのでHTTR水蒸気改質器の使用条件に対してどうか正確なことはL、えないが熱物性ハ
ンドブック j を基準選定値として選定推算式とのパーセント誤差か最大でも 5 [96]に収まっ
ている。しかし.パーセント誤差の大きさは圧力に依って大きく変っていることから,熱伝導
率の圧力効果に関して選定推算式と基準選定値は厳密には異なっていることがわかる。
以上をまとめと.選定した推算式の精度は,慨ね最大でも 5[%]程度と推測されて.工学的
には許容される範囲にあるといえる。ただし圧力効果に関しては,低温の限られた温度範囲で
しか評価できず.今後の課題として残った。また,選定値集の中で,日本熱物性学会編 f熱物位
ハンドブ 7クJ及び日本機械学会の技術資料「流体の熱物性値集j は.二酸化炭素の熱伝導率に
ついて高温側て過大な値を与えることがわかった。
上記の比較評価から明らかなように,今後取り組む必要がある課題として,まず,実測データ
のばらつきを低減するため信頼性の高い試験方法による実測データの更なる蓄積か必要であり.
これに基いて信頼性の高い推算式を確立するとともに選定値集の信頼性を明確にする必要があろ
つ。
亡。丹、
u

JAERI-M 93-029
#3.1SE f i « 1 4 * © £ £ * * t * © f i S . BE UK®
W 3S « H € mi£i&mt%'if* ft R € m %
W 3S « H € mi£i&mt%'if* ft R € m s. £ E i t i *
U. S. Department of Commerce. National Bureau of Standards.
"Tables of Theraal Properties of Gases" (U55¥3HT) «•»
* * # X 200-600
i x io- ' - io
30-600
0.1-10 0.1 J U. S. Department of Commerce. National Bureau of Standards.
"Tables of Theraal Properties of Gases" (U55¥3HT) «•» HMtKXtfx
200—3000 1 xl0"s—10
200-3000 1 XIO'-IO
U. S. Department of Commerce. National Bureau of Standards.
"Tables of Theraal Properties of Gases" (U55¥3HT) «•»
zswtas&tfx 200-1500 1 xl0»~10
200-1500 l x 10"'—10
1
Purdue University, Thermophysical Properties Research Center
"Thernophysical Properties of Hatter, The TPRC Data Series."
GeEEtt»:lWW3SHTwo». tttt«&:197553e1f(3,\ ! » £ * £ : M O ^ i f ' " ' )
* * it x <•> 100-1370
0. 0.1013
Purdue University, Thermophysical Properties Research Center
"Thernophysical Properties of Hatter, The TPRC Data Series."
GeEEtt»:lWW3SHTwo». tttt«&:197553e1f(3,\ ! » £ * £ : M O ^ i f ' " ' )
* * it x 100-1370
0. 0.1013
Purdue University, Thermophysical Properties Research Center
"Thernophysical Properties of Hatter, The TPRC Data Series."
GeEEtt»:lWW3SHTwo». tttt«&:197553e1f(3,\ ! » £ * £ : M O ^ i f ' " ' )
-KtffcSastfx 250-1370 0. 0.1013 Purdue University,
Thermophysical Properties Research Center
"Thernophysical Properties of Hatter, The TPRC Data Series."
GeEEtt»:lWW3SHTwo». tttt«&:197553e1f(3,\ ! » £ * £ : M O ^ i f ' " ' )
-KtffcSastfx 250-1370 0. 0.1013 Purdue University,
Thermophysical Properties Research Center
"Thernophysical Properties of Hatter, The TPRC Data Series."
GeEEtt»:lWW3SHTwo». tttt«&:197553e1f(3,\ ! » £ * £ : M O ^ i f ' " ' ) awttawx 200-1370
0. 0.1013
I Purdue University, Thermophysical Properties Research Center
"Thernophysical Properties of Hatter, The TPRC Data Series."
GeEEtt»:lWW3SHTwo». tttt«&:197553e1f(3,\ ! » £ * £ : M O ^ i f ' " ' ) awttawx 200-1370
0. 0.1013
I Purdue University, Thermophysical Properties Research Center
"Thernophysical Properties of Hatter, The TPRC Data Series."
GeEEtt»:lWW3SHTwo». tttt«&:197553e1f(3,\ ! » £ * £ : M O ^ i f ' " ' )
* 9 * it * 280-1370
0. 0.1013
Purdue University, Thermophysical Properties Research Center
"Thernophysical Properties of Hatter, The TPRC Data Series."
GeEEtt»:lWW3SHTwo». tttt«&:197553e1f(3,\ ! » £ * £ : M O ^ i f ' " ' )
* 9 * it * 280-1370
0. 0.1013
I. Bar in?';!/-7 "Theroochenical Data of Pure Substances"
(I989$£fr) ( U )
* * # x 298-5000
0.1 (=l{barj) -
I. Bar in?';!/-7 "Theroochenical Data of Pure Substances"
(I989$£fr) ( U )
* * # x 298-5000
0.1 (=l{barj) -
I. Bar in?';!/-7 "Theroochenical Data of Pure Substances"
(I989$£fr) ( U )
- W U I H W X 298-3000
0.1 I. Bar in?';!/-7
"Theroochenical Data of Pure Substances"
(I989$£fr) ( U )
- W U I H W X 298-3000
0.1 I. Bar in?';!/-7
"Theroochenical Data of Pure Substances"
(I989$£fr) ( U )
—Btffc fstfX 298-3000
0.1
I. Bar in?';!/-7 "Theroochenical Data of Pure Substances"
(I989$£fr) ( U )
—Btffc fstfX 298-3000
0.1
I. Bar in?';!/-7 "Theroochenical Data of Pure Substances"
(I989$£fr) ( U )
* 9 > 1t 7> 298-2000
0.1
I. Bar in?';!/-7 "Theroochenical Data of Pure Substances"
(I989$£fr) ( U )
* 9 > 1t 7> 298-2000
0.1
H. B. BAPTAOTHK ( x ? • < • t7)\,it7f-v9') (197255Brr) ""
* * # X 14-1500
0.1-100 14-1500
0.1—100
H. B. BAPTAOTHK ( x ? • < • t7)\,it7f-v9') (197255Brr) ""
-WfcBaWx 200-3000
IO-'-IO
200-3000
io- J~io H. B. BAPTAOTHK ( x ? • < • t7)\,it7f-v9') (197255Brr) ""
OWUWWx 273—1800
0.1-60 273—1800
0.1-60
H. B. BAPTAOTHK ( x ? • < • t7)\,it7f-v9') (197255Brr) ""
* 9 y it ?. 95-1000
0.02-100 95-1000
0.02-100
(*) mmmotwMi, mmto
S E C T I O N 1
JAERI-M 93-029
第3.1表 書色物性値の選定値集とその温度・圧力 範密
熱 物研 勾7恒1.. 機 関 名 選定値集 と 発行年 物質名
密 度 定圧比熱
2冊~創10 初-s舶水素ガス
1 xlO-'-10 0.1-10 0.1;)
u. S.Deparlment of Co圃 erce. iables of Tber副 lPro(p19er55t年ies発o行f)Ea日ses. 初令、~3(脚 200-3000 NationaJ Bureau of Stasdards. 一酸化炭素ガス
1 xlO-'-lO 1 xlO-'-lO
加 -1目。 200-15仰 i 二酸化炭素ガス
1 xl0-'-10 1 XI0・'-10
1.1 1伺-1370水素ガス
O. 0.1013
お0-1370
設部官鶴iriJizm:i襲i隠ぽ警臨 ter.一酸化炭素ガス
Purdue University. O. 0.1013 ThermophysicaJ 1301
Properties Research Cester 1311' 2ω-1370 二酸化炭素ガス
O. 0.1013
280-1370 メタンガス
O. 0.1013
298-5∞o 水素ガス
0.1 (= 1 (b.rJ)
四8-3冊。一酸化炭素ガス
-ITIErmocIlheee皿sical Bataof Pure 0.1 I. Barinクソレープ Substa
0989年発行) 1141
二酸化炭素ガス却8-3ωo
0.1
却8-2ωoメタンガス
0.1 -ーー寸
14-1500 14-151ω 水素ガス
0.1-1朗 0.1-100
2∞-3ωo 2ω-3∞o 一酸化炭素ガス
H. 6. BAPfAφTt1K 『便覧 気体と液体の熱(物19理72年的発性警行』}
10-'-10 10-'-10
(エヌ・べ・ワルガフチック) '331 幻3-1800 幻3-18伺二酸化炭素ガス
0.1-60 0.1-60
95-1000 95-1仰Oメタンガス
0.02-100 0.02-1伺『 ι
C*)選定値の記載無し,他も閉じ。

*. \i
JAKKI M .4.) »29
-bgW<S«ieffllK]. TSWEfUBaSWil
$ #J tt IS m % 8? IS 3£ 8. it 3tt tt tt % a m e m m m %
X 200~600
1 xl0"3~10
30-600
0.1-10
10-1100
0.1013 (= 1 tatil)
10-700
0.1013 • * 9 V#XttfettLTl,^£t\>
7x 200~3000
1 xl0"3~10 200-3000
1 xio'—10 50-1500
0.1013 70-600
0.1013
• * 9 V#XttfettLTl,^£t\>
J;'x 200-1500
1 xl0"3~I0
200-1500
1 X10"3~I0 190-1700
0.1013
180-600
0.1013
• * 9 V#XttfettLTl,^£t\>
X (•> 100—1370
0, 0.1013
10-2000
0.1013
20—2000
0.1013 fflrLTftlSL
•fiitt&Sttt. ChapMn-Cowlingitlc
X 100—1370
0, 0.1013
10-2000
0.1013
20—2000
0.1013 fflrLTftlSL
•fiitt&Sttt. ChapMn-Cowlingitlc J/x
250-1370 0, 0.1013
80-1500 0.1013
80-1250 0.1013
fflrLTftlSL
•fiitt&Sttt. ChapMn-Cowlingitlc J/x
250-1370 0, 0.1013
80-1500 0.1013
80-1250 0.1013
fflrLTftlSL
•fiitt&Sttt. ChapMn-Cowlingitlc
7 x 200-1370 0. 0.1013
170-2000 0.1013
180-1500 0.1013
fflrLTftlSL
•fiitt&Sttt. ChapMn-Cowlingitlc
7 x 200-1370 0. 0.1013
170-2000 0.1013
180-1500 0.1013
fflrLTftlSL
•fiitt&Sttt. ChapMn-Cowlingitlc
• x 280-1370
0, 0.1013 70-1000
0.1013
100-1000
0.1013
fflrLTftlSL
•fiitt&Sttt. ChapMn-Cowlingitlc
• x 280-1370
0, 0.1013 70-1000
0.1013
100-1000
0.1013
fflrLTftlSL
•fiitt&Sttt. ChapMn-Cowlingitlc
X 298-5000
0.1 (=1 [bar]) • £{CJANAF tV. S. Bureau of Mines <o^-rjummtxnmo X
298-5000 0.1 (=1 [bar])
• £{CJANAF tV. S. Bureau of Mines <o^-rjummtxnmo
; /x 298-3000
0.1
• £{CJANAF tV. S. Bureau of Mines <o^-rjummtxnmo
; /x 298-3000
0.1
• £{CJANAF tV. S. Bureau of Mines <o^-rjummtxnmo
tfx 298-3000
0.1
• £{CJANAF tV. S. Bureau of Mines <o^-rjummtxnmo
tfx 298-3000
0.1
• £{CJANAF tV. S. Bureau of Mines <o^-rjummtxnmo
^ 298-2000
0.1
• £{CJANAF tV. S. Bureau of Mines <o^-rjummtxnmo
^ 298-2000
0.1
• £{CJANAF tV. S. Bureau of Mines <o^-rjummtxnmo
X 14-1500
0.1-100 14-1500
0.1-100 15-1000
0.1-100 80-1200
0.1-60 • ztitx-KimztiT^zimtt, mesmowo
7'X 200-3000
10 3~10
200-3000
IO-'-IO
273-523
0.1-80 73-1273
=£0.1
• ztitx-KimztiT^zimtt, mesmowo
~?fX 273-1800 0.1-60
273-1800 0.1-60
258-1273 0.1-60
220-1400 0.1-60
• ztitx-KimztiT^zimtt, mesmowo
^ X 95-1000
0. 02-100 95-1000
0.02-100 120-560 0.1-50
103-573 0.1-60
• ztitx-KimztiT^zimtt, mesmowo
3Q/-37~38- ___
sYrnTT2
‘ .J.¥U"i[ ¥1 Y:j 1/29
$偵の選定 値集とその温度・圧力範圏(その 1) 上尉温度範囲[KJ.下段が圧力範囲[III.J
熱 物 位 値備 考
密 度 定圧比熱 粘 性 係 数 熱伝導*
200-6ω 30-曲。 10-11ω 10-7'ω -メタンガスはfet院していない。ス
1 xlO-3- 1O 0.1-10 0.1013 (= 1 [at・]) 0.1013 -それまで.選に提定案しさ式れてかいら求る推め算て式いをる。
評価し た200-3000 2ω-3000 50-1500 70-自叩
ワス1 xl0-3--10 1 x1O-s-1O 0.1013 0.1013
200-1500 200-1500 190-17'ω 180-冊。ヴス
1 x 10-3-10 1 XlO-3-IO 0.1013 0.1013
t・3 100-1370 10-2ω。 20-2ωo -実解測析デしてー作タ成の信。額性を評価し.錨十ス
0.0.1013 0.1013 0.1013
250-1370 80-15ω 80-1おO-定れ圧て比い熱る。については相関式が与えら
,JfスO. 0.1013 0.1013 0.1013
-粘基さ性せき係て.係数い数はる.。はC実ha演Ilfデnー-cタ欄にlin~にフィット200-1370 170-20ω 180-1印O
ヴスO. 0.1013 0.1013 0.1013
280-1310 70-10ω 100-1ω。ス
O. 0.1013 0.1013 0.1013 -ー一
298-50ω -主にJーANプAFルをとU号.iS.Bしuてre.作au成o。f Mines ス のテ 周
0.1 (= 1 [bar])
298-3000 ガス
0.1
298-3000 ガス
0.1
Ir ス298-2000
0.1
14-1500 14-1500 15-1000 80-1200 -選そる定れい根はま選拠で定には不値提案表明。にさ基れてき作い成る推。算た式だあし.ス
0.1-100 0.1-100 0.1-100 0.1-60
200-3000 200-3000 273-523 73-1273 ガス
10-3-10 10-3-10 0.1-80 話0.1
273-1800 273-1800 258-1273 220-1400 プJス
O. 1-60 0.1-60 0.1-60 0.1向--60
95-1000 95-10ω 120-560 103-573 ス
0.02-100 0.02-luO 0.1-50 0.1-60
年メトおーSECTION 2

SS* 3 '
JAERI-M 93-029
3S3.1« i t t t t t t f f l I S i * t ^ f f l f i I - E A l G '
i S « M g « £ « * < ! : & * f ^ tt R « m m i S « M g « £ « * < ! : & * f ^ tt R « m * 3£ E Jfc » ?
B*tS«^^ (1863$!tfT) '" ,
* * # x 20~600 0.01-50
20-600 0.01-50
B*tS«^^ (1863$!tfT) '" ,
—§Mfc#9l«#x (68-133 [K]) (68—130[K])
te<
B*tS«^^ (1863$!tfT) '" ,
OWUHWfx 220-1100
0.01-100
220-1100
0.01-100
B*tS«^^ (1863$!tfT) '" ,
* 9 > # x 100~600
0.01~300 100-600
0.01—300
B*ttftt!fe¥& riMItt^ > K7 •>> ? j (199033£*f),M
* * # x 100~650 0.01~50
100-650 0.01—50
B*ttftt!fe¥& riMItt^ > K7 •>> ? j (199033£*f),M
HWUWWfx 70~1000
a 2-100
70—1000
0.2-1000 B*ttftt!fe¥& riMItt^ > K7 •>> ? j (199033£*f),M
rmuwwx 220-1100
0.01-100 220-1100
0.01-100
B*ttftt!fe¥& riMItt^ > K7 •>> ? j (199033£*f),M
j< ? > # X 200-600
0.02-300 200-600
0.02—300
SE L
C T I 0 N 1 |
、てさ穿E
~
JAERI-M 93-029
第3.1表 熱物性値の選定値集とその温度・圧力能
研 1i: 機 関 名 選定値集 と 発行年 物質名費自 物
密 度 定圧比熱 ' 初叶伺 2ト屯仰
水素ガス0.01-50 0.01-剖
飽和状態での値のみ 飽和抗態での値のみ 島2一強化炭素ガス
日本機械学会 『技術資料 流体の熱物〈性1鈎値3年集発』行) cs一 色, (68-133[1]) {回.-130[K])
忽:0-11ω 沼ト11佃二酸化炭素ガス
0.01-1ω 0.01-1加
1ω-6ω 1ω吋叩メタンガス
0.01-<抑 0.01-3ω
1伺斗関 100叶印水素ガス
0.01-50 0.01-号。
70-1側 70-1ωo 一酸化炭素ガス
0.2-100 0.2-1ωo 日本熱物性学会 f熱物性ハンドブックJ (19ω年発行)削
220-11ω 220-1100 二酸化炭素ガス
0.01-100 0.01-100
2ω→ω 2叩~問。メタンガス
0.02-3ω 0.02-鈎O
「
SECTION1 L

•JAKKI M 9 < 029
JJWBKiBHB]. TgWEflJEfflWa]
s g ft © tt « m % s g * ft m S. it » ft tt ft ft M £ 3)1 *
m %
X # x 20~600
0.01-50 20-600
0.01-50 80-1000
0.01-100 80-1000
0.01-60 E©*1000[K] 4TMM.6*lTH5o
-ftaas^x (68~133[K])
ISftH*.ffi7?fflffl[0* (68-130 [K]) (78-130 [K]) (74-130 [K])
E©*1000[K] 4TMM.6*lTH5o
•.:ffcK**x 220-1100
0.01~100 220-1100
0.01-100 273-1200 0.1—50
220-1400 0.1-60
E©*1000[K] 4TMM.6*lTH5o
? > # X 100-600
0.01~300
100-600 0.01-300
273-600 0.01-50
273-700 0.01-50
E©*1000[K] 4TMM.6*lTH5o
X * x 100~650
0.01~50
100-650
0.01-50
273-600
0.01-50
273-600
0.01-50 • *n£-t?K*Bg**iTi*.5Ji3ls$;*.5
J@HU£Hli.
r--HfcgS!l#X 70-1000
0.2-100 70-1000
0.2-1000 70—500
0.1-80 70-500
0.1-10
• *n£-t?K*Bg**iTi*.5Ji3ls$;*.5
J@HU£Hli.
:.2ft«*/fx 220—1100
0.01~100 220-1100
0.01—100 273-1100 0.1-50
220-1100 0.1013
• *n£-t?K*Bg**iTi*.5Ji3ls$;*.5
J@HU£Hli.
? > # X 200-600
0.02-300
200-600
0.02-300
200-480
0.1-70
300-420 0.1-70
• *n£-t?K*Bg**iTi*.5Ji3ls$;*.5
J@HU£Hli.
1
-
S E C T I O
- 3 9
N2 ~|
- 4 0 -
ーJ.¥EHI ¥1 9;1 029
熱物性 値の選定値集とその温度・圧力範囲(その 2)上働温度範囲[KJ.下段が圧力範囲[II'&J
質名 備密
熱物
定圧比熱 導伝熱ー
一一考
度
素 ガス
1""化炭素ガス
20 ..... 側 20 ..... 回o 80.....1側 | ω.....1脚 |・長与端接待足立私想。0.01-叩 0.01-50 I 0.01.....100 I 0.01-印 l
l l・担当委 の裁量に基き,推算式ある飽和状態での値のみ|飽和状態での値のみ l飽和状態での値のみ i飽和状態での値のみ| いは選定値表を選び作成。
(68-133[KJ) (68""'130 [K)) (18""'130 [K)) (74""'130 [K))
化炭素ガス
7 ンガス
素 ガス
!?"sイ蹴素ガス
.~化炭素ガス
タンガス
220-1100
0.01-100
100-600
0.01-300
100-6印
0.01-50
70-1000
0.2-100
220.....1100
0.01-100
200.....600
0.02-300
273-1200
0.1-50
幻3-600
0.01.....50
273-6ω
0.01 ..... 50
70-5ω
0.1-80
213-1100
0.1-50
200-480
0.1-10
る選
あ
'式し
算だ
推た
る。
い成
て作
れき
さ基
提拡岡山
で定は
ま週拠
れは棋
そい定
220-14ω
0.1-60
273-71ω
0.01-50
213-6曲
0.01-印
70-500
0.1-10
220-11ω
0.1013
3叩-420
0.1-10
220-1100
0.01-100
100-600
0.01-300
100-650
0.01-50
70-1000
0.2-10ω
220.....1100
0.01-100
200-600
0.02 ..... 300
ル
-39-40-

JAKK1 M 93 029
MS 3. 2 ^ B#*M*Jl4^#« r*iat t /N> K7-y >J ©iiygfitt&KHll»fc««
a » * fs A 3* # tt
a » * a? a 2 E it * tt tt
* #
•JtlPC
T V PV CJ= log,, — =b(T)+C(T)p
T. V. RT
H.W. Wool ley et al.. U. S. Department of Cowrce National Bureau of Standards. Research Paper RP1932. Vol.41(Nov. 1948).
££©«S:Sg5j>S«-»ffl#Mfc « « * £ * » .
• S i t
s**t*3*£BC-72 /j>aa? ;
<D:7nr5.k©fflBJ2t
-hSE»£» (1987)
- » f t j E U *
TS£3t*+<0«TrcS-rtt!BjJg5Knoiiaaalytic equation of state) 0
*B«ffltt68~1000[Kl. 100[MPa]
P-P„ (/>) =joR • [T-T/x>)] + o (pRT.)-F(p.T)
P„(p) :SSi£E. T.Cp) : f t f t£#aBE (7 : *fffi!?seg
•Xitt R. D. Goodwin. J. Phys. Chen. Ref. Data. Vol. 14. No 4(1985). pp. 849 —932.
S2©#K»«5tfr&. aTfflM«2C*i:**8(«berg
C«, /R =3.5+exp(- £/x) • S A, • x1"'. 1 * 1
X aT/100
Ac,=-r.f(<w erup/p* C. =C,H-T-K$P/<ST)V(*P/<Sp)]/ P 1
• £ * fs3 £
•f£l£2Ji£ CINDAS Data Senies*^?! ,
• £ * P. E. Li ley. T.Uakita et al Material Properties. Vol. 1988.
- K i t * *
S.Angus et al . . International Thenwdynanic Tables of Fluid State-3. Carbon Dioxide. Pergaaon Press. 1973.
PI £
a**H*¥£©t>©t tTE-s :
•»ET?©«)»* 1 a. VT •
- K i t * *
S.Angus et al . . International Thenwdynanic Tables of Fluid State-3. Carbon Dioxide. Pergaaon Press. 1973.
PI £ l + a - r / 1 0 s •
•*ffiT-©*77 1
log[(i7-J7 ,)10 !+7] = ™
L.H.Chen. GA-1038(1959). •
^ ? >
T?e©X«^t-5lfflo
S.Angus and K.M. de Reuck. International Thermodynanic Tables of the Fluid State-5. Methane. IUPAC. Vol.5.1976.
PI £
TEXtt t©»©«»S;f r ' " •
i?(p.T) = 5.(T)+j?.(T' fl
J? . (T)=E C.T'—"• fl
3i(T)=b,+b,[b,-ln(T. I
A n =exp(ai +»i/T) (explB + ( p / p « - l ) p ' - * ( 8 «
•Xft 1 J.F.Ely and H. J.M.Hanie'. • Vol. 20(1981). pp.323~3: : •
tit) J8»a <f>flt©»StMl<t©it«Kttl4^««Bl7 !©8FSaBS"" fcffli'fc.
S E C T I 0 N 1
.J..¥EHl ¥1 ~:l:l υ29
熱 カ
第 3.2表 日本熱物性学会編「熱物性ハンドブック j の選定値作成に用いた総
物質名学
定庄比熱 絵性密 度
-縫算式 l・作成方法。('CJ以上については下記文献中に示されている次の| 左記の校望書方程式から種々の扶懲量..係書置を求め.状想方程式 l 定E比熱を表わす関係弐に代入して求める。
T V PV 1];ー一一ー log,.- =b(η+C(りρ
T. V. 町* 3賢
一齢化炭素
-文献見W.Woolley et al.. U. S. Departllent of co圃陪rceNational Bureau of Staodards. Resωrch Paper EP1932. Vol. 4lCNov. 1948).
• f量算式下記文献中の以下に示す状態J方程式(oonaoa!ytic何回tionof state)。適用範図は68-10ω[KJ.話100[l/PaJ
P一九 {ρ)=ρR・[T-Tぷρ)J+ 1] (ρRT.)・F(ρ.T)
Pσ(ρ) ・蒸気圧. T a (ρ 気液共存温度
σ:対臨界密度
-文献
R. D. Goodwin. J. Phys. Chem. Ref. Data. Vol. 14. No. 4(985). pp. 849 -932.
-作成方注
目本機嫌学会技術資料「流体の熱物性値集Jから引用。B本機械学会の上記選定値集は下記の文献から引用して作成。
二酸化炭素
-文献
S. AngUS et al.. lnternational Ther・o!lynuicTables of Fluid State-3. C8rbon Dioxide. PergaJlOn Press. 1973.
・作成方法下記の文献から引用。
メタン
-文献同左
-作成方法左記の状懇方程式から,以下の関係式等に適正きRo・lIergの数値積分後を周いて求めた。
C~ IR =3. 5+exp( -e /1) • 1: A. • 1'-九
Z軍 T/loo
aC.=ーTJ(O'P/ oT')dρ/ρ2
c. =C.+T'[(oP/oT)'/(oP/δρ)J/ρ2
.文献
同左
同 左
閑 左
-文献
S.A目guSand K.比deReuck. Inter且ationalTberlllOdyna圃icTables of the Fluid State帽 5.Methane. iUPAC. Vol.5. 1976.
[注〕推算式や他の選定値集との比鮫には斜学技術庁の研究報告".,を用いた.
SECT'ON1
-推算式日本援械学会RC-72小温度Z体の換物性に関する研究分私のプログラムの相関式
-文献上記報告書(t987)
-作成方注CINDAS Data Seniesから苦l
-文献P. E. Liley. T.llakita et a 1 llaterial Properties. VoL 1988.
・作成方法日本猿械学会技術資料『涜t
日本機嫌学会のものは下詑
.常圧での値司.
a. .rr 10・n・=
1 + a' r 110'
-高圧での値n
!Og[(布一市・)10'+7J=
-文献L. H. Chen. GA-I038(I959).
か
F
R
M川
縫
+のF
D
u
k
d
J
の
ncz
申・=,T-F
献
η=
間
試
仏
市
.,-轟rk--
権
下
司
可
1/ ,(T) =b, +b. [b,ー10(T.
a可=exp(a,+a,!f) (exp +(ρ/ρ,ー1)ρ・-・(8・
-文献J.F.E!yaod弘J.M. Hanle、Vol.2O([981). PP.323-3

,.*?ERMS
JAKRI-M 93-029
rjft«tt^> Yf~j'7\ ©*S«ftf l i i r ff l^fc***»i*©XlR
H t M % * ft
1 s: it I tt e ff » IS £ if *
B*«*?£RC-72 *SBBl7>*>U--<'^*fflfMii* #©!»«rtti=M-r 5 W3BHfc§?<08rffl**«£»<::Br«
Jb32«£» (1987)
ft £
J - . ^ ' i . «Tffll»ffSC*IC*SRmberg • tt®3;& [SI
CINDAS Data Seniesfr £?!$,>
B r - £/i) • S'A, - I J - ' . 1 l - l 1 x =17100 f5j £
1 SVHo/o'
1 6W/(6P/6p)]/ p2
P. E. Li ley. T.Uakita et al.. CINDAS Data Series on Material Properties. Vol.V-l.Hemisphere Publishing. 1988.
H * « » ? & © fc © l*TE3tltt©»c«!>Ji*5tfr <aft A.
.4 £
a . VT c vr .4 £ l + a-r /10 1 " l + C T / 1 0 e l r
•iftEET-Ottj; •WET-©«X V log[(7-'? ,)10 ! ,+7] = b.+b,pr log[Q - A •)10'+4]=d.+d, p T
L.H.Chen, GA-1038O959). •Xtt
13 £
Tsexittt ©*©«aiet*> t.ff <&> j(p.I)=i;,(T)+iI.(T)fl+A5(0.T) A = 2 g„./T'+(E g,,/T')P+(S g,,/I")P*
ft £
7?.(T) = E Cl""""*
5,(T)=b,+bI[b,-ln(T/b«)] + (£ g i . /DP '+U g^/DP*
1
Aj?=exp(a,+a./T) {exptCa.+a^/T'^/o'-' + (p/p,-l)p ,- ,(a,+a./T+a,A«)]-1.0}
1
J.F.Ely and H. J.HHanley, Ind. Eng. Chem. Fundat. Vol.20(1981), pp.323~332.
• 3tKR
52^3fl) , *«Srr«PWS
- 4 1 - 4 2 -
S E C T I O N 2
、 τ~~.:;:
""'"圃・圃圃圃圃・・・
降
JλEHI <¥1 93-029
Y会編「熱物性ハンドブァク j の選定値作成に用いた推算式等とその文献
•
主 送
熱伝iIJ事圧比熱
愉
枯健保書E
から極々の状態量,徴係書Eを求め.匂係弐に代入して求める。
-推算式日本機械学会RC-72小温度差ランキンサイクル周作動流体の熱物性に関する研究分科会の研究成果報舎書に所蔵のプログラムの相関式
-文献上記報告書(1987)
係
同 左
-作成方法:から.以下の関係式等に基きE口圃berg I CINDAS Data Seoiesから引用。いて求めた。
[t主l
ヶ - E 11) • r A.・x'・¥,・ 1
l..T/lOO
oT')dD! D'
oT)'!( OP/δρ)J/ρ2 -文献P. E. Liley. T.蜘kitaet al.. CINDAS Data Series 00
J.laterial Properties. Vol. V-l. He圃ispherePublishiog・1988.
同 左
司 左
-作成方法日本機械浮会袋術資料 f流体の熱物性値集Jから31用。日本復械学会のものは下記文献の次の推算式から作成。
.常庄での値刀.
a • .rr 10' 71・=τ=1IT
1 + a'" /10・,.
-高圧での償却
ドvlog[(可-71・)10'+7]=b.+b,ρτ
-文献L. H.Ch直n.GA-1038(1959).
.m算式下記文献中の次の推算式から作成。
71(ρ. T)= 71.(T)+司,CT)ρ+A71(C.T)
可・(T)= I: C.T '.'4> /.
同 左 71, (T) =b, +b, [b, -ln(T/b.) 1
A司=exp(a,+a,/T)(exp[(a.+a./T'/f)c'.' +(ρ/ρ.-1)ρ・-・(a.河川+a7/T')]ー1.0)
-文献J. F. Ely and比J.IlJ/a目ley. Ind. En8. Ch帽 . FundaL. Vo1.20(J98J), pp.323-332.
-作成方法
B本書E械学会袋街資料 r~主体の熟物性値集J から事Htio日本犠械学会のものは下記文献の次の推算式から作成。
-常圧での値A・C.♂-
10' λ・=1+ C'" /10'"
'iIi圧での値λ
log[(λ ー λ・)10'+4]=d.+d,ρτ
押川
。s?“
」戸
成イ、
作
h
-b
内J
か
押
川
揚地
E
・2悼
の
(
次
u・
:-の河川
左
一
中一
献
z.
敵同一紙一
UJH
文
推
下
A
十四 g3,IT')P'十(I:g..ITつP'1-' 1-・
-文献物性データ調室研究報告.高圧力デ-~.第 5~ (昭和52年3月),科筏庁費量興局
十寸l
一一
qt
一
N一nHU
一
TI
一
Pし
一「F』
P
、υ

J A K K 1 - M 93-029
+ 1.0
+ 0.5
Hydrogen
Density
- 0 . 5
- 1 . 0 300 400 500
Tempera ture
Pressure [MPa]
0.1 0.1 0.2 1.0 5.0
600
[K] 700
* 3 . 1 H * * K o i » r * K © « ^ f f l l » S : © l l ; « » l
^ +1.0
+ 0.5
o (0 a a
-0.5
•1 .0 1 — 200
3.7%
Carbon Monoxide Density
Pressure [MPa]
0.2 0.2 0.5 1.0 5.0
400 600 800
Temperature T [K] 1000
* 8. 2 B -»{ fcK*«col >T ftK©*£«JMt©ifc«fftf °
- 4 3 -
93-029 .J:¥EHI-~I
+ 1.0 [ポ]
一一一一ー十二一一一一-----ーーーー一'
+0.5
。
-0.5
zd¥(-2ミl.2d)
ωLコパV」伺色
ω口 700 600 500 400 -1.0
300
[K]
水素について密度の選定推算式の比較評価。
T Temperature
第3.1図
+ 1.0巴Carbon Mロnoxide
Density
-0.5
{ぷ]
ω」コパV」Mwa
。。
-Sミ¥(EdlHgq)
1000
[K] 600 400
T emperature
-1.0 200
T
一酸化炭素について密度の選定推算式の比較評価。
η3
A4
第3.2図

•JAEHI M 9:i 1)29
2 78°-o
Pressure [MPa]
O.I O.I 0.5 1.0 5.0
1000 Temperature
m a 3 ii -mimmz^i >T®mcoMfem%a.<z>it$mffi,
I
+ 2.0
+ 1.5
+ 1.0
+ 0.5
3
a Q
-0.5 300
Methane
Density
Pressure (MPa]
0.1 0.1 0.5 1.0 5.0
400 Temperature
500 600 [K]
^ 3 . 4 0 * ?>iz-o\,>r®mom%.m&fte>}t&&ffi
- 4 4 -
'.1 9:l lJ~9 .J:¥I-:I¥I
c!.
ヱミ +0.51': ,
f f~
Carbon Dioxlde
Density
~ ~
・---¥
-0.5 ω」コパVLmwaωQ 1000 800 600 400
一1.0300
[K]
二般化炭素について密度の選定推算式の比較評価。
丁Temperature
第3.3図
+2.0 F両国「
ぷ
¥ ¥¥
¥¥¥.
ai +1.5 c!. 、、、
ω
ぜ+1.0
.;
ω
三 +0.5、九、-ー
ー- ーーー『ーーー-『ー『ーーーーー -ーー一ーーーーーー・・ーー一ー一ー『ー-ーーーーー。
。」コけての丘@白
600 500 400 -0.5
300
[K]
メタンについて密度の選定推算式の比較評価。
-44-
T Temperature
第3.4図

J A K H 1 - M 9:i- 1)29
+ 3.67%
O
o
o
+-> 10
a Q
+ 1.0
+0.5
0
- 0 . 5 f-
- 1 . 0
- 1 . 5
Hydrogen
Isobaric Specific Heat 1 [atm]
'U/iumtmwmM/Miimtammmmm^mn
Reliable Measurement Data Band Shown in the TPRC Data Series.
Estimated b;
Selected Estimate Correlation
JSTP's Handbook
Barin's Handbook
Vargaftik's Handbook
200 400 600 800 1000
Temperature T [K] 1200 1400
£ 3. 5 0(a) * * i r o l ^TtETCD^EJtSlCD^^f tS^ iCDJte^ f i ,
+ 1.0
X +0.5 O
o
o d - ° 5
3 - i .o (0 a. 0) Q •1.5
Hydrogen
Isobaric Specific Heat
Pressure (MPa)
0.1 0.1 0.2 1.0 5.0
400 Temperature
500 T [K]
600
£3 .5 0(b) *^(c-o l>T^Ei t f i©^^} iS; j t©£E^3«! i^ (CKt- .5Jt«B?<i<
4 5 -
u29 -ud .1:¥1-:1¥1-:-'1
+3.67%
Reliable Measurement Data 8and
Shown in the TPRC Data 5eries.
~ +1.0 c>
U :::::: +0.5 。凶
'" U
~ -0.5 '" 。
-1.0
。
[ゆか}
1400 1200 1000
[K]
800 600
Temperature
400 200 -1.5
ωLコリF」同
aω白
丁
水素について常圧での定圧比熱の選定推算式の比較評価,第3.5図(a)
+1.0 [訳] Hydrogen
Isobaric Specific Heat
+0.5
。
-0.5
-1.0
一2・
auk-24015ω-aO)
ω」コリFLmaω口
600 500
T [K] 400
Temperature
300 -1.5
水素について定圧比熱の選定推算式の圧力効果に関する比較評価。
-45-
第3.5図(b)

JAEKI-M 93-029
+ 1.0
+ 0.5
0
- 0 . 5
- 1 . 0
Reliable Measurement Data Band /Shown in the TPRC Data Series.
Carbon Monoxide Isobaric Specific Heat
I [atm]
3 £
_1_
Estimated by
Selected Estimate Correlation
Selected Estimate Correlation
Bann's Handbook
Vargafttk s Handbook
200 400 600 800
Temperature
1000
T [K]
1200 1400
£3. 6 H(a) -SMfcflBltfcol *TffET©igEifc!»©®aijra©Jfc«*Mlo
-15.12
Carbon Monoxide Isobaric Specific Heat
Pressure [MPa]
0.2 0.2 0.5 1.0 5.0
400 600 800 Temperature T [K]
1000
i 3. 6 0(b) - » f c K * K o t »T£EJtlKl©a£fli*i&©E*aMllw mtzit&m®°
4 6 -
93-029 .l:¥EHI -¥1 '
-LE
e-晴
-
d-e-
a一MH-
x--
o-c-E』
n-広明
-n
hM-c-u
w-晦
-a
JE--
n一にω一
岬
-c-1
2
・t-
rEM-
-a-h-
Fl》
-o-Is---
Reliable Measurement Data 8and
! Shown in the TPRC Data Series.
五福一一ー・・ーーー同同-
U +1.0 、、
~ +0.5 a
u
也2
2
U -0.5
訳
-1.0
。
ω」コパ七の立
ωO
1400 1200 1000 800 600
[K] T Temperature
一酸化炭素について常圧での定圧比熱の選定推算式の比較評価。
1000
Carbon Monoxide
Isobaric Specific Heat
800
[K]
600 400
Temperature
。」
コゼ -46 a ω o -6
200
-15.12
第3.6図(a)
4
7
7
i
nwd
内屯
u
r
R
J
F
肘EM
--B+
{渓]
T
一酸化炭素について定圧比熱の選定推算式の圧力効果に
関する比較評価。
-46-
第3.6図(ω

• IAKK1 M <tt (>2tf
oX
+ 4 o /(•.. +2
l/J
a
o 1
0 1/5
a
o - 2
q> - 4 1_ n + J
<_ — K <o n. » Q
Reliable Measurement Data Band Shown in the TPRC Data Series.
Carbon Dioxide Isobaric Specific Heat
1 [atm]
i T n r m "*• Estimated by
Selected Estimate Correlation
Selected Estimate Correlation
J5TP's Handbook
Bann's Hanooook
Vargaftik's Handbook
200 400 600 800 Temperature
1000 T [K]
1200 1400
£3. 7 0(a) :»fc8S*Col 'T#flET©^EElfclfc©»Slt»*©tt«ff«.
a? + 2
u
o
o
1_
ro Q. 0 Q
0
- 2
- 4
- 6
- 8
•10 200
Carbon Dioxide Isobaric Specific Heat
Pressure (MPa]
0.1 0.1 0.5 1.0 5.0
1000
Temperature T [K] -54.9
1200
S3. 7 0(b) I-Slffc^^tro^r^EJtfio^^fiiat^fflE^aScM-r^Jtiiffffio
• 4 7 -
O~!j 吟ゐ山市¥1 !λEhJ
Carbon D.oxide
Isobaric Specific Heat
I [atm]
Reliable Measurement Data 8and
Shown in the TPRC Data Series.
[ぷ]ω
ci +4 u 、、、
言 +2ω a υ
ci -2 0
。
-4
戸hv
ωLコリFL句包
ω
。800 600 400 200
[K]
二酸化炭素について常圧での定圧比熱の選定推算式の比較評価。
T Temperature
第3.7図(a)
含ロ
去
he
d
一Hx-c
oτhn
D一目
n一切
o-c、
ahu-P匂
r-1
au--引HF
e--叫ea
京 +2
一
/
'一///
///
/////
。
-8
" ω c. υ 、、、
Q; -2 '" a
U
I -4 ω a
巴 -6
ωLコパV」句丘
ωQ
1200 1000
[KJ 丁
800 600
Temperature
-10 200
二酸化炭素について定圧比熱の選定推算式の圧力効果に関する比較評価。
-47ー
第3.7図(ω

JAHKI M 93-029
^ +1.0
o + 0.5
o I 0
3
-0.5
<5 -1 .0 a Q
Methane
Isobaric Specific Heat
1 [a tm]
Estimated bv Selected Estimate
Correlation Selected Estimate
Correlation JSTPs Handbook
Bann's Handbook
Vargaftik's Hardback
300 400
Temperature
500 600
[K]
f?3. 8 H(a) / ? >iZ^l^Xlf:IZ?<D%1£&a:<DMfem»3$.(!>Htem&<>
0 s -+ 2 -
sel 0
a
o - 2 a
o I - 4
o
a ai
Q
4 h
6
8
-10
Methane
Isobanc Specific Heat
Pressure [MPaJ
0.1 0.1 0.5 1.0 5.0
300
-14.31
400 500 Temperature T [K]
600
-18.30
£3. 8H(b) t 9 >Koi»-C^ffiJfcf»©*^ffi»^;cDffi*a*JrK-r5Jteif«o
- 4 8 -
~I 93-029 J:¥EHI
Metnane
isobarJC Speclflc Heat
1 [atm]
ぷ~ +1.0
600
/ ,F /
/ /
/
町てうど
---一一--~500
そ¥
300 400
ヨリ凶
己
主ミ +0.5 ω ω C注。ω 也3
" 仁〉~ -0.5
ω L
コ+'
~ -1.0 a ω Q
。
[K]
メタンについて常圧での定圧比熱の選定推算式の比較評価。
T Temperature
第3,8図(a)
Metnane
Isobanc Specific Heat +2
// ~
/
。
-2
-2・aU¥(-2dU12ωaU)
-4
[認]
----~/
/ II Pressure附 j
/ 'ー 0.1
-6
ωLコパて同aoQ 600 500
T [K] 400
Temperature 〆14.31
-8
-10
メタンについて定圧比熱の選定推算式の圧力効果に関する比較評価。
-48-
第3,8図(ω

•lAKIil M 93 1)29
+8
+ 6
VI +4 •5.
sel.,
+? 3.
U) 0 V
3.
- ? 0) l_ 3
- 4 <n n <u Q - 6
- 8
Band for Thirty-nine Sets of Experimental Data Shown in the TPRC Data Series. Hydrogen
Viscosity I [atm]
Estimated by
Selected Estimate Correlation
Selected Estimate Correlation
JSTP's Handbook
Vargaftik's Handbook
200 400 Temperature
600 [K]
^3. 9H(a)-l *^( r -o l<r#£E-C:f f l t t14iSl i©«S} i®i t©Jt«£l¥« (iSi&ffll) 0
2000
Temperature [K]
%3.9 n(a)-2 *ic'5i^xni±vo>^m^M(ommmw-^<Dit^mm (.m&m),
-49-
-¥1 9:1 -1I:!9 .J.-¥EHI
+8 8and for Thirty-nine 5ets of Experimental Data
Shown in the TPRC Data Series +6
。
-4
-6
+4
。,‘
+2
{ぷ]
ωLコパVL句aoo
-2ミ¥(-2ミlzoミ)
600 400 200 -8
[K]
水素について常圧での粘性係数の選定推算式の比較評価(低温側}。
丁Temperature
第3.9図(a)-I
Experimental Data 8and
Shown in the TPRC Data Series. +4
+2
。
-4
-6
内JL'
Zミ¥(一
2ミlEeミ)
[訳]
ωLコパFLmaωO
-8
2000 1800 1600 1400 1200 1000 800 -10
[K]
水素について常庄での粘性係数の選定推算式の比絞評価(高温側}。
-49-
丁Temperature
第3.9図(a)-2

JAERI-M 93-029
^ +4
400 Temperature
500 T [K]
*& 9 0(b) **Coi>Tt t i t«a©*^«»i tOEA»*CM-r«t t«f f«S.
+2 Band for Eight Sets of Experimental Data Shown in the TPRC Data Series.
- 2 -
- 6 ;
Carbon Monoxide Viscosity ! [atm]
Estimated by
Selected Estimate Correlation
Selected Estimate Correlation
JSTP's Handbook
-1 1 1 1_ 200 400 600
Temperature T [K]
i 3.ioii(a)-i -mit^m^-o^rsjEvo^nwMom^mw-^oitmmm O&SM)O
50 -
93-029 JAERI-:¥I
...
+4
+2
ぷぞ
zf¥(-2ミlzmミ
600 500
T [K] 400 300
。
-2
-4
-6
ω」コパ
FLmaωQ
Temperature
水素について粘性係数の選定推算式の圧力効果に関する比較評価。
-' -' r 一戸
ーーーー-
Carbon Monoxide
Viscosity
1 [atm]
8and for Eight Sets of Experimental Data
Shown in the TPRC Data Series.
Experimental Data Point
第3.9図(ω
+
[ゆか]
-Zミ¥(-2ミ120ミ)
。L
コげて句
aωQ
600 400 200
[K]
一酸化炭素について常圧での枯性係数の選定推算式の比較評価(低温側)。
-50ー
T T emperature
第3.10図(a)ーl

JAKK1 M 9 3 - 0 2 9
£ +4
J +2
1 0
1 - 2
.ure
- 4
)epa
r1
- 6
Carbon Monoxide
Viscosity I [atm]
Estimated
Selected Estimate Correlation
Selected Estimate Correlation
JSTP's Handbook
800 1000
Temperature
1200
[K]
1400
SS3.IO[M(a)-2 -K{LM*Icol>T-ffi"ET©tt1±tfSSt©^«!iffS;©itK^ffi («SflH)o
+-> (0 Q.
Q
- 4 -
- 6
Carbon Monoxide
200
Viscosity Pressure (MPa]
0.1 0.1 0.2 1.0 5.0
300 400
Temperature T [K]
w. 3.100(b) -miii^mz-oi ^Ttemm<DMs£mw-$,(Di±j]8)mzM-t % &&mm c
5 1 -
-93--029 :¥1 .J..¥EHI
Carbon M四n。制de
Viscosity
I [atm)
一一一ー一一ーー一一一一一ーーー一一-------F ー一一ーーー一ー--ー←ー一
+4
+2 -Zミ¥(-EミlEωミ)
ω」コ一FLmw
色。。
{ぷ]
。-2
-4
1400 1200 1000 800 -6
[K]
一酸化炭素について常庄での粘性係数の選定推算式の比叡評価(高温倒)。
T Temperature
第3.10図(a)-2
Carbon Monoxide
Vi唱cos.ty
。
-2
-4
[訳}
eE£¥(-EミlewEミ)
ω」コパFLmaoo
600 500 400 300 -6
20G
[K]
一般化炭素について粘性係数の選定推算式の圧力効果に関する比較評価。
-5}-
丁Temperature
第3.10図(b)

JAER1-M 93-029
+ 4
+ 2
Carbon Dioxide
Viscosity
1 [atm]
Experimental Data Band
Shown in the TPRC Data Series.
Estimated by
Selected Estimate Correlation
Selected Estimate Correlation
JSTP's Handbook
Vargaftik's Handbook
Temperature T [K]
Viscosity
1 [atmj
Estimated by
Selected Estimate Correlation
Selected Estimate Correlation
JSTP's Handbook
Vargaftik's Handbook
1200 1400
Temperature T
^3.ns(a)-2 z.mtmm^^T%i±votemmc>Mi£m&3$.<DstVi.wm mum),
- 5 2 -
圃・・
93-029
Experimental Data 8and
Shown in the TPRC Data Series.
JAEHI-:>I
+4
+2
。
A
,
ι-
-4
{渓]
-Eミ¥(-Zミ
lEミ)
ω」コけFL喝且
@Q
600 400 200
[K] T Temperature
二酸化炭素について常圧での粘性係数の選定推算式の比較評価(低温側)。第3.11図(a)-I
Carbon Dio刷 de
Viscosity
I [atm)
Experimental Data 8and
Shown in the TPRC Data Series.
F -ー:::,::.1-ーーー=ご-一一ーー→-ーーーーーーーー・ー
一一ー-ーーー一一一
+4
ai +2 刷 ν,
とえ、、、(
@
ω =主
ω @
=止)
。
[訳]
n''M
ω」コパV」句
aω
。2000 1800 1600 1400 1200 1000 800
-4
[K]
二酸化炭素について常圧での粘性係数の選定推算式の比較評価(高温恨の。
-52
T Temperature
第3.11図(a)-2

•IAKHI M 93 U29
+ 10
+ 8
— +6
i_
•!->
t_ ID Q. d) Q
- 2
- 4
- 6
Carbon Dioxide Viscosity
1.5T e
Pressure [MRaj
0.1 0.1 0.5 1.0 5.0
200 400 600 800 1000 Temperature T [K]
1200 1400
m 3. iiiM(b) nfi*ftM^jio^-ctttt«acDS^fii»s;a>E*a*icB8-r-5itg{i¥ffio
+ + 6|-
+ 4
+ 2
0
- 2
- 4
- 6 0
Band for Twenty-six Sets of Experimental Data Shown in the TPRC Data Series.
200
Temperature
^3.12H(a)-l y 9 > i r -o^T^E-C©«i f4#^©ig^J tgs t©i t ixW<ff i (ffi&ffllJ).
- 5 3 -
-U2~ 9:l ¥1 電lAEHI
+10
+8
,,Jf'rtFF'111
・・
+6
+4
+2
。-2
[訳]
-25¥(-2ミlzωミ)
ωLコパF」市立
ωO -4
1400 1200 1000
[K] 600 800
Temperature T 400
-6
200
二酸化炭素について粘性係数の選定推算式の圧力効果に関する比較評価。
8and for Twenty-six Sets of
Experimental Data Shown in
the TPRC Data Series.
第 3.1!1@b)
+4
+2
+6
。-2
-4
+8 与更
一Sミ
¥(E辻luEミ)
ωLコパ乞maωQ
600 -6
0
[K]
メタンについて常圧での粘性係数の選定推算式の比較評価(低温側)。
内合
υ「「
υ
丁Temperature
第 3.12図(a)-1

JAKM-M 93-029
+ 8
+ 6
+ 4
+ 2
3
(0 Q. 0 D
- 2 -
- 4 -
I
Methane Viscosity I [atm]
Estimated by
Selected Estimate Correlation
Selected Estimate Correlation
JSTP's Handbook
700 800 900
Tempera ture
1000 1100 1200
[K]
% 3.120(a)-2 * 9 > IZ-ol ' T f fET f f l t t i t #»®a«« l» *© i f c«»« ( A f i f l ) .
+ 5
^ 0
=5. I 5 - 1 0
i_ 3 •P i_ (0 Q .
Q
- 1 5 -
- 2 0 -
1000
Temperature T
• • 1
Methane • 1 Viscosity
• 1
1 1
1 1
1 1
1 I
1 1
1
w__ /
1 1
1 1
1 1
1 1
I 1
1 1
w__ /
Pressure (MPal
1 1
1 1
1 1
1 1
I 1
1 1
^ ^ . _ • * •
/ 0.1
1 1
1 1
1 1
1 1
I 1
1 1
^
/ 0.1
1 1
1 1
1 1
1 1
I 1
1 1
/
0.2
1 1
1 1
1 1
1 1
I 1
1 1
/
1.0
1 1
1 1
1 1
1 1
I 1
1 1
/
5.0
1 1
1 1
1 1
1 1
I 1
1 1
/
fcx
-
\ . -
- l .5T c
- . t . I i i i
2000
[K]
ft 3.120(b) * 9 > K O I ' T t t t t f f » ® a S « » i C © J E A » * ^ H f SifcKff«<>
- 5 4 -
93-029 JAEHl-:¥1
+8 {ぷ]
, ,. ,. ..... ..... ..... ..... --
--2ミ¥(一ω帥ミ
120ミ)
F -一一ー「。
-:l
-4
ωLコパF」Mwaω口
1200 1100 6700
[K]
メタンについて常圧での粘性係数の選定推算先の比較評価(高温側〉。
T Temperature
第3.12図(a)-2
Methane
Viscosity
+5
。
-10
-15
phd
{ポ]
-Bミ¥(-@的立
12ωミ)
。」コパFLmwaω口 J.5Tc
-20
2000 1000 。[K]
メタンについて粘性係数の選定推算式の圧力効果に関する比較評価。
aa・
Rυ
T Temperature
第3.12図ib)

JAEKI-M 93-029
-10
Hydrogen
Thermal Conductivity
1 [atm]
Experimental Data I Shown in the TPRC Data Series.
^Experimental Data Point
Estimated by
Selected Estimate Correlation
Selected Estimate Correlation
JSTP's Handbook
Vargaftik's Handbook
200 400
Temperature T [K]
600
»8.1SH(a)-l Jk$lzr>\,*XtiE.T!<?>1&&9¥toM%MXa,<!>}timtt (ffifi«).
I
(0 a <D Q
-15
Estimated by
Selected Estimate Correlation
Selected Estimate Correlation
Vargaftik's Handbook
1000
Tempera tu re
1500
T [K] 2000
*3.i3B(ai-2 fcmi^^z<D®ET®mfcmm<DSfem#ft®it®mffi (.mum),
55-
.JAEHI-:¥I 93-029
,
Experimental Data
Shown in the TPRC
Data Series.
Hydrogen
Thermal Conductlv'ty
1 [atm]
ω
...; +5 、¥(
ω ω
,吋
'" a
ベ
ω 」
コ+' 」伺a ω 。
。
e司M
Experimental Data Point
600 400 200 -10
0
[K]
水素について常庄での熱伝導率の選定推算式の比較評価(低温側)。
T Temperature
第3.13図(a)ーl
Hydrogen
Thermal Conductivity
1 [atm]
--戸---------
+10
[ぷ]
+5
。
-10
ERd
-oJ¥(ZJlzeペ)
ωLコ判」伺乱。。
2000 1500 1000 -15
[KJ
水素についての常圧での熱伝導率の選定推算式の比較評価(高温側)。
P同U
Fhu
T Temperature
第3.13図(a)-2

JAERl-M 93-029
s? + 2
01 L.
+-> CO
a <D
Q
- 2 -
Hydrogen
Thermal Conductivity
200
Pressure [MPa]
0.1 0.1 0.2 1.0 5.0
400 Tempera tu re T
600
[K]
£3.130(b) **Koi^T}&fc#¥©;!£»g3©I£:&a£CM-f5Jt&i¥fflli
+4
O S
s +2
3 •f-> l . CO
a CD
Q
Carbon Monoxide
Thermal Conductivity 1 [atrn)
y^Hi
Experimental Data Point
Estimated by Selected Estimate
Correlation Selected Estimate
Correlation
JSTP's Handbook
200 400 600
Tempera tu re T [K]
*8.14H(aH -» f l :K*K-5^ r f tE -C©f !M5#*©»S« l*a©J tR»« (fi&fl).
- 5 6 -
93-029 JAEHI-:'1
-------~ ~
Hydrogen
Thermal ConductlVlty
+2
。
,々‘
[ポ]
zJ¥(-Sべ15ベ)
ωL
コパFL伺
huoo
600 400
Temperature
-4 200
[K] 了
水素について熱伝導率の選定推算式の圧力効果に関する比較評価。第3.13図(ω
9.9
ExperimentaJ Data Band
Shown in the TPRC
Data Series.
Carbon Monoxide
Thermal Conductivity
I [atm)
+4
。
n,-
百 +2'" '吋
、¥(
., w
Fて
~
腕@
,て)
ωL
コ日FL句
aoG
(渓]
Experimental Data Point
600 400 200 -4
[K]
一酸化炭素について常庄での熱伝導率の選定推算式の比較評価(低温側)。
-56-
T Temperature
第3.14図(a)ーl

•JAEHI-M 9 3 - 0 2 9
3 +-> L.
a 4)
a
800 1000
Temperature T
1200
[K]
*il4H(a)-2 -(tffcK*JCol»rHfE-C©lie**<oa£Ji»iCOJttt lP« (A f i f l ) .
I
+ 4
+ 2
I
Carbon Monoxide
Thermal Conductivity
Pressure [MPaJ
0.1 0.1 1.0 5.0
400 Temperature
600
[K]
*3.140(b) -» f tg t *Co^r *MK**©aSf l l J |E i t©E*»*KB81-* ib«» t f o
57-
.JAEHI -'11 9:1←029
Selected Estimate Correlation Carbon Monolide 11
ト / Thermal Conductivoty 11
-・-司岡町圃・I [.tm]
. •
{ぷ]
:J: +8 '吋、、、
i +4 ω
Fて
ω
" 三一4
。
ωLコげFLωaωO
1200 1000 800 -8
[K]
一酸化炭素について常圧での熱伝導率の選定推算式の比較評価(高温側)。
T
Temperature
第3.14図(a)-2
+4 Carbon MonOlide
Thermal Conductivity {訳] +2
。
-4
内Jι
-Eべ¥(一2ペlE@べ)
ω」コパV」句
aoo
-6
600 400 -8
200
、町
[K]
一酸化炭素について熱伝導率の選定推算式の圧力効果に関する比較評価。
ηt
Fhu
T Temperature
第3.14図(b)

.J.AKKJ-M 93-029
0 s -
I
+ 12
+8
+4
0
- 4
(0
a Q
-12
Carbon Dioxide
Thermal Conductivity
1 [atm]
Experimental Data Band Shown in the TPRC Data Series.
Estimated by
Selected Estimate Correlation
Selected Estimate Correlation
JSTPs Handbook
Vargaftik's Handbook Experimental Data Point.
200
Tempera tu re
g$3.15S(a)-l rM<ti%mtz^l*X%&X>®&imm<DMfeimyS.®!km¥m ( i i B « ) .
33.9 27.6 _ — X - "
40.1
*~P + 20
* +10
l_ (0 a tu Q
Carbon Dioxide
Thermal Conductivity
1 [atm]
- 8 I L.
Estimated by
Selected Estimate Correlation
Selected Estimate Correlation
JSTP's Handbook
Vargaftik's Handbook
800 1000
Tempera tu re T [K]
1200
jg3.i5H(a)-2 ~»<tstmzr>\,*r%E.r'<o%l&mm®Mfetm3Z<i>it®&m ( S M I ) ,
- 5 8 -
-JλEIiJ -¥1 93 -029
、Dε斗 +12
Experimental Data 8and Shown
in the TPRC Data Series. VL
t-
ρ』
-ωw-
d-tE
山
-
叫
-J
K-Au-W
3『
n『
t
11EO-a
EC一[
品
u-4
副-,E
釦一
m一
pu-r
一
・ρ--
』
H-
?lv-
ω 」
3 ...., 」伺
母一 12~o
'" .;. +8 、、、
ま +4'ぜ
ω
'" ,て)
。-4
-8
400 200
[K]
二酸化炭素について常圧での熱伝導率の選定推算式の比較評価(低温側〉。
T Temperature
第 3.15図(a)ーl
40.1 33.9 ーー_x
27.6 __ _-x-ー-〆λーー一
/
/ /
/ /
〆〆
/ /
/ /
/ /
J J
/ /
/ /
/ /
,F J
Carbon Oioxide
Thermal Conductivity
1 [atm]
+20
+10
[認]
-24¥(
一ωJlzJ) .--------。ω」コリF」伺丘
ω白
1200 1000 800 -8
[K]
二酸化炭素について常圧での熱伝導率の選定推算式の比較評価(高温側)。
-58-
T Temperature
第3.15図(a)-2

.1AKKI M 9H lffl
D •>->
i-<0 Q. d) Q
+ 10
- 10
-20 200
Carbon OioxiOe Thermal Conductivity
Pressure [MPa]
0.1 0.1 0.5 1.0 5.0
Temperature [K]
^ a isiatb) umitmrniz-oK *xmfcmm<DM,£mn^<Dg.ii®$k<zMtz>immm,
+ 12
+ 8
+ 4
0
Methane
Thermal Conductivity I [atm]
Experimental Data Band Shown in the TPRC Data Series.
I -&z^zg
^ - - 4 Estimated by Selected Estimate
Correlation Selected Estimate
Correlation
JSTP's Handbook Experimental Data Point
a a
-12 200
Temperature
400
T [K] 600
m3.i60(a)-i y j7 >no t ,^x i&mvomfcmmoMimn^v i immm u&sfD,
- 5 9 -
エ1 ~:l II~~ . J..¥ EIi I
Carbon OIQxlde
Thermal Conductivlty
+10
-10
。
[ポ]
-E戸、¥(一
Zべ120べ)
ωL
コパVL伺
aoo
1200 1000 800 600 400 -20
200
[K]
二酸化炭素について熱伝導率の選定推算式の圧力効果に関する比較評価。
T Temperature
第3.15図(b)
Experimental Data 8and
Shown in the TPRC
Data Series.
Methane
Thermal Conductivity
1 [atm)
述+12
AHV
AJ'-
n
M
u
-
-
E
一一
ω」コてのaωO
~ +8 rイ、、、
i +4 闘
ベ
的
ω
三一4
。
400 200
[K]
メタンについて常庄での熱伝導率の選定推算式の比較評価(低温側)。
-59-
T Temperature
第 3.16図(a)ーl

JAKK1--M 93-029
tB3.16BI(a)-2 / J'XC-ol »T#ET©lBliK«l*©a^flljrSt©Jt«fftf (ffi
3 • ! - >
£ _
CO a. a> Q
+ 2
+ 4
Methane
Thermal Conductivity
Pressure [MPa]
0.1 0.1
0.2
1.0 5.0
260 300 400 440 Temperature [K]
$3.i6ia<b) * 9 >iz^^x&fcm&®mfemma.<DE.j]%i%iz®irzitnma »
60-
93-029
' J.-¥EHI-:¥I
Methane
Thermal Conductivlty
J [.坑mJ
Experimental Data 8and
Shown in the TPRC Data Series.
Selected Estimate Correlation
1200 1000 800
占ぞ
ω
..; +8 、、、(
:;: +4 'て
ω 。'て)
-4 ω L
.3 -8 L
句a ω Q
。
[K]
メタンについて常庄での熱伝導率の選定錐算式の比較評価(高温側)。
T Temperature
y
t
v
t
p」
ロ也
-
H
U
n川-・パu
a-n
L門
-o
d-C
M-剖m
r
o
」
nT目
第3.16図(aJ2
+2
+4
[ぷ]
EJ¥(-2415べ)
ω」コ門戸」句
ao口
440 400 300 260 。
[K]
メタンについて熱伝導率の選定推算式の圧力効果に関する比絞評価。
-60-
T Temperature
第3.16図(bJ

JAERI-M 93-029
4. m m & m mm
s s &1±#8 &&mm * m $4. 10 $4.5 0 $ 4 . 9 0
-mitm* $4.2 0 $4.6 0 , $4,100
=.mimm $ 4 . 3 0 $4.7 0 $ 4 1 1 1
/ ? y $4.4 0 $4.8 0 $4,120
frZo $4 . 6 0*^$4.120C:{±, HT7RikmimW$!s<DttmW£&&&ft. E|J*,, JUST^T"
n-bxtfxm^&milOO [K] (=827[°C] ) £W$:&<KJg®i£$©400[K] ( = 127[*C] )
- 6 1 -
JAERI-M 93-029
4. 熱物性値線図
第2章で選定した錐算式から作成した密度,粘性係数及び熱伝導率の各線図を第4.1図から第
4.12図に示す。定圧比熱については,見直しか必要であり,作成していない。各図の内訳は次の
とおり。
密 度 粘性係数 熱伝導率
水 素 第4.1図 第4.5図 第4.9図」
一酸化炭素 第4.2図 第4.6図 第4.10図
二酸化炭素 第4.3図 第4.7図 第4.11図
メ タ ノ 第4.4図 第4.8図 第4.12図
これらの図から明らかなように,対象とした水素,一酸化炭素,二酸化炭素及びメタンの粘性
係数並びに熱伝導率は,日TTR水蒸気改質器の使用条件内では圧力依存性が強くないことがわ
かる。第4.6図から第4.12図には, HTTR水蒸気改質器の代表的な温度条件, f!fJち.通常時プ
ロセスガス最高温度1100Ui: J (=827[OCJ)と事故時最低温度近傍の400[K] (=127[.C])
について圧力依存性を示した。
l
no

JAERI-M 93-029
1-2
Reduced Temperature Tr=T/Tc 10 20_ 30_
o
0. II 0.
c CD
a T3 CD O 3
-o CD
400 600 800 1000 1200
Temperature T (K]
u.\m * n © m m
- 6 2 -
93-029 J:¥ERI-:¥t
υ円、¥肉、
H』ミ
kA
主的
Cω
。万
ωUコ℃
ω庄
10-1
10-2
Tr=T/Tc Reduced Temperature
lil--!11111」凶
AU守肉
HM・E
・-
10-5
200
〔
円
Eυ¥切〕
Q.
hH
一ωcω
。
(K)
因。線度
T
密
Temperature
の
-62一
素水第4.1図

JAKH1- M 93-029
Reduced Temperature Tr=T/T c
400 600 800 1000 1200
Temperature T [K]
£4. 2d - » f t K * © B f f i
• 6 3 -
93 -029 :¥1 HEHI
υ内、¥肉、
H」包
hH
一ωC
∞。万ωUコ刀@庄
10-2
Tr=T/Tc
10-3
Reduced Temperature
6 4
400
2 10-1
10-4
200
10-2
〔
円
Eυ¥切〕
kA
一日一
ω=ωQ
~
800
(K)
一酸化炭素の密度線図。
-63-
T Temperature
第4.2図

JAEM-M 93-029
Reduced Temperature T r =T/T c
i 2 a_ L
200 400 600 800 1000 1200 Temperature T (K)
C4.8H l l f t K l t O l K i t H
- 6 4 -
.JAEHl --:'1.1 93 -029
Carbon Oioxide Density
Pressure 又二5.0(MPa)
ト、4.5寸~
一一雫
Tr=T/Tc
4 "
Reduced Temperature
2
υ
円、¥aHL円、
hH一的
Cω凸
℃
ωυコ℃也庄
10-1
何,‘白HM・
E
・-
10-3
1200
:¥! 一一←一一十一一
トー「ー十一ーー斗一一斗ー_-1
一十一→一一 斗一-,
ー」一十十十寸ー?っ-「!っ
‘‘u
nHM
・E
・-
〔
円
ευ¥切〕
Q..
KAHazω凸
1000
(K)
200
T
二酸化炭素 の密度線国。
-64ー
Temperature
第4.3図

•IAKK1 - M 93-029
Reduced Temperature Tr=T/T c
2 A 6_
10 -4 _L^ I 1 !_
200 400 600 800 T5W
Temperature T [K) 1200
E4.4H ^ 3 ' > © g g J S ^ i a t
- 6 5 -
!I;~ -029 .1:¥1-:1<1 -~I
Reduced Temperature
υ角地¥包
HL門司
弘主的
coo万
ωυコ刀
ω広
10-2
10-3
T -一一 ,
Pressure =5.0 (MPa)
4 F 一一寸一一2
Tl 10-1
10-2
r-園、
ε u
K¥
tlO 、ー.J
0..
kAtωcω凸
1布B10-4
2而 1000
(K)
E回
Temperature
因。密度線
T
のン
65-
タメ第4.4図

JAEKI-M 93-029
Reduced Temperature T r =T/T c
800 1000
Temperature T [K]
i4.5H * t © t e f i « l l l »
66-
圃圃'
93-029 .J:¥I-:HI-:-'1
Tr=T /Tc Reduced Temperature
30 XIO-5
3 20
出坐皇n
Viscosity
10
O.I[MPa]
Pressure=O.2""5.O[MPa] 一回
-mwa}とえ
hH一的002〉
ート|」ω 1000
[K]
800
T Temperature
400
水素の粘性係数線因。
-66-
第4.5図

JAKKI--M 93-029
Reduced Temperature T r =T/T c
Pressure P [MPa]
' Pressure=5.0[MPa]
0.1 MPa
0 1 2 3 4 5 Pressure P [MPa]
J L J 1 L J i_ 200 400 600 800 1000 1200
Temperature T [K]
B4.6H -K<kf t*0t t&ff i» t t l3o
- 6 7 -
• J:¥EHI:-'I 93-029
Reduced Temperature Tr=T/Tc
XIO-5
XW-5
4.251 I T= t 100[K] I
ミ 4.20L
。 2 3 4 5 Pressure P [MPa]
~l 色伺 白ト-Pressure = 5. O[MPa]
ミ 3ト O.1[MPa]
XIO-5
2.20
I T=400[K] I =ぇ
2.10 2 4 5
Pressure P [MPaJ
200 400 600 800 1000 1200
Temperature T [K]
第4.6図 一酸化炭素の粘性係数線図。
-61-

JAKU1- M 93 029
Reduced Temperature T r =T /T c
0 1 2 3 4 5 Pressure P [MPa]
-+ Pressure=5.0[MPa]
-i r
0.1 [MPa]
J 1 L.
0 1 2 3 4 5 Pressure P [MPa]
_i _ J i i i !_
200 400 600 800 1000
Temperature T [KJ 1200
mnm -m<tt%me>te«ki%&mmc
• 6 8 -
Jλ五Hl-¥1 93 029
~
4
Tr=T/Tc Reduced Temperature
=主
Xl0-5
←一一一一斗
人!; O.l[MPa]
L-J
5
一¥出
P
2
Pressure
4.30
0
4 [ω-mwnb
とえ
h#一回00的一〉
Lヱヲ岨阻j
-'
X 10-5
2.20
2.00
2.10
[MPa] P
2
e
FF
UM
-3
CJW
'1
白wftilt
F』D
a
1. 90
仇
HU
のHU
n,,.
AMu-
1200 1000
[K]
800
T
600
Temperature
400
二酸化炭素の粘性係数線因。
-68ー
第4.7図

.1AKKI M 93 029
Reduced Temperature T r - T / T c
x l 0 " 5 2 3 4 5 6
y.
"H"
XIO"5
2.85
-] r i i 1—! r T — r i i
Methane Viscosity
T=1100[K
0 1 2 3 * 5
Pressure P [MPa]
Pressuve=5.0[MPa]
T=4QQ[K1 0 1 2 3 4 5
Pressure P [MPa]
J I 1 I L 1 r J L 200 400 600 800 1000
Temperature T [K]
1200
£4.8 m * 9 > CD *s i± if m & m o
6 9 -
。29.J,¥EHI ~l 9a
Tr=TfTc Reduced Temperature
4 Xl0-5
1T= IIOO[K] I
[ω-ca]
O.1[MPa]J とえ
kAH300ω一〉
l T=400[K] I 1.35
0 5 4 3
P
2
Pressure
1200 1000
[K]
800
T Temperature
200
メタンの粘性係数線図。
-69-
第4.8図

JAERI-M 93-029
Reduced Temperature T r=T/T c
10 20 30
E
"> O •a c o O E
u.b I i i
i
i| i i I
i Hydrogen Thermal Conductivity U.48U
0.470,
Thermal Conductivity U.48U
0.470,
- T=1100[K] 1 | U.48U
0.470,
.
1 | U.48U
0.470,
.
U.48U
0.470, i i ' t 4 *
n d
Pre ssure P [Ml M i
p ressu re=5 .0[MPa] ; i j !
; i
i 1
y? r \ i 0.1 [MPa]
1 1 I
1 ] jy i \Ar i
t
I j
i
0.2
1 . i 1
0.235
i
0.2 . i 1
0.235
y I L T=400[K] ^ ^ 0.230 u
"< 0.225
0.220 ( i i i i
i
i
0.225
0.220 ( i i i i
i
i
0.225
0.220 (
1 2 3 4 5
0
i i i
0.225
0.220 (
Pn
1
assure
i 1 1
LMHaj
i i 200 400 600 800 1000
Temperature T [K] 1200
E4.9ia frmo&fcmmmm
- 7 0 -
JAERI-l¥1 93-029
Tr=T/Tc
Hydrogen
Thermal Conductivity
30
Reduced Temperature
AHu
nHU
守,,aay
nu
0.6
0.4
[(v--E)¥〉〉}
|T=400[K] I 0.230
...... ぜ
hH一〉一HOコ刀
coo-ωELωε
↑
5
[MPa] P
2
Pressure
《
HU
AHU
q,‘ の
Jh-
AHHV
200 1200 1000
[K]
800
T
600
Temperature
400
水素の熱伝導率線図。
-70一
第4.9図

. I A K K I - M 93--029
Reduced Temperature T r = T / T c
0.08
0.06
0.04
0.02
0.01
I i ; i i i i i T i l l 'I I i I [ I i
X 1 0 " 2 Carbon Monoxide I
Thermal Conductivity -
I
i l .1
^ 7 . 1
7 0
Thermal Conductivity -
I
i l .1
^ 7 . 1
7 0
: T=1100[K]
I
i l .1
^ 7 . 1
7 0
- ^ _ _ _ _ _ — • —
I
i l .1
^ 7 . 1
7 0
I
3 1 2 3 4 5 j Pressure P [MPa] ^ ^
i
F 'ressi re=5 .0[MF >a] F
\ 0.1 [MPa]
F
^ i
1 / /
XI o-2
3.5
—
3.5 - T=400[K]
— 3.4 -<
3.3
— 3.4 -<
3.3
—
! 1
3.4 -<
3.3
1 2 3 4 5 Pressure P TMPal
1 1 \
3.4 -<
3.3
1 i
1 i i i I
200 400 600 800 1000 1200 Temperature T [K]
mum ~mik%m®&fct$mmm .
7 1 -
ー
,JAEHJ ~:'I I 9:j..029
Reduced Temperature
4
Tr=T/Tc
2 6
0.08
7.0
ZF1
3 l十時urep
、EE、Eー 0.06
Carbon Monoxide Thermal Conductivity
,て
+〉〉J、
+ιコ」2
E0 O,O4
仁コ
言X 10-2
一Mn一
-AUν
一
一AHV
一
一an守一
一一一一一宇
l一
3.4
3.2 0 4 5
Pressure P [MPaJ
0.011 200 400 600 800 1000 1200
Temperature T [K]
第4.10図 一酸化炭素の熱伝導率線因。
旬ZE

JAEK1-M 93-029
Reduced Temperature T r =T/T c
2 3 4.
200 400 600 800 1000 1200 Temperature T [K]
72 -
.JAEHl, :"19:1-029
Tr=T/Tc Rωuc倒 Temperature
「十一n0.10
.. 5 [MPa]
Ama D
・
0.08
[(v-・E)¥〉
〉]
O.1[MPa]
Xl0-2
1T=400(K] I
0.06
0.04
.... ぜ
hパF一〉一判。コ刀
coo-eE」@Zト
.. 5 [MPa] P
2.6 o 2 Pressure
0.02
1200
[K] 8JO 600
Temperature 400 a
HHW
RHU
血す,.
aHU
T
二酸化炭素の熱伝導率線図。
-72ー
第4.11図

.IAKKI M 93 029
0.3
Reduced Temperature T r =T/T c
2 4 6
0.2
200
i i i 1 ! I I 1 1 1
; 1 ; 1 ! i Methane — 0.19
— 0.18
— 0.18 0.18
L Thermal Conductivity — 0.19
— 0.18
— 0.18 0.18
(J -L Thermal Conductivity — 0.19
— 0.18
— 0.18 0.18
(J -— 0.19
— 0.18
— 0.18 0.18
i i
i
— 0.19
— 0.18
— 0.18 0.18
i i
i r=noo[K]
— 0.19
— 0.18
— 0.18 0.18
i i
i
i i
— 0.19
— 0.18
— 0.18 0.18
' 0 1 2 3 4 5
— 0.19
— 0.18
— 0.18 0.18
F •ressur e 1 3 [ MPa]
Pressure= 5.0[M 3a] A O.I[N IPa] O.I[N IPa]
XI n-2 XI U
5.2 - T=400[K]
" 5 . 0 4 , (
i i i i 4 , (
1 1 2 3 4 5 Pressure P TMPal
i 1 I
1 400 600 800 1000
Temperature T [K] 1200
54.12H > 9 > co m fe » $ m n o
- 7 3 -
‘lλEHI ¥1 ¥1:¥029
Tr=T/Tc
6
Reduced Temperature 2
l T=J 100[KJ I
nu
nu
内
M
H
V
R
U
E
d
1
0
3
0
0
a
u
a
u
1
1
1
1
内Hd
内H
ν
A
H
U
内HU
一
一
吋
一
「111iLili--』ll,
h
‘HW AHHW
一(¥・
E)¥〉乙
[MPa] p 2
Pressure
0.2
0.1
,司ぜ
』〔パ工〉一判。コ司
C00一mELωz↑
5.2 シイPressure P [MPa]
1200 nHu
nHV
A7'
・
nu
メタンの熱伝導 率 線 図 。
qu
nt
第4.12図

JAEKI-M 93-029
5. * t &
7£ztir\.>zmkimt5z.kizj;o, *<Dimn£miAitz<, -&©&£, suDctima^
(1) SgJgC-oHTfi. S ^ L f c Peng-Robinson-Redlich-Kwong©1£!g;frg5$©!£ffffiJtl£, **K*fLT«fc0.1[9o] £ T E ' J . -»ffc&*. -»ffcf t*R£M * .--<:# L T t £ i 2 [»*] tlTT-feO, HTTR7K^m3t«is©l9:S«a ; lc i iSJi?f lf±r / r>^t i^^WLT^5 0
(2) ^ f f i J t ^ t co^Tl i . MEEX'Onmr:-?frT-mLri*Z>$L$L£%&L. §g£mf*©tt<i S l ^ f l l ' 5 ^ * l t W : . tt^gittLT van der Waals^£fflWc*§£, ^EET'
©figmsii^o.21%] WTr+^-^lt^-cfe-So Mmzb\,->x, frmizttLxi±i.o[:s~}
WTniRi-oTi^o t ^ u z.n<b3mfcaigi'k. &i£-i&&wx'ftm&m<t£i), 5.0[MPalXlilO CM £Mz.Xl^2,o COWMlt, JiR>fctt&S;£g*t©fii$:#C©iggBT
S l ^ ^ T f c - S C i * < B ( j ^ ^ i 4 - - , ^ 0 f ; t , ffK©&i% Peng-Robinson-Redlich Swong ^.^m^t^^iz-oi ^xms%mtbx\ *-s0
(si temmiz-oi>xa, MfeLWhodos<h<D)kKfflrT&<Dm:mmt, i%mz&^xit7m ttrnzmtes [%] i-mizi&t^x&i), *%iz^^xt>m*X'%n [%] x-b%0 nmz ts\,^Xl±jt9>£fegmte5 194] «P^«CR*oT*J0, ^ X I o t ^ T f c l O [%] $-i@/_
•Jo
(4) *if£^$-i;oi^T(i, J t&^SSJEI io&gfBf f l sMie . t tT i^^©/^ . ^^4'Sllfe(i T i ' i l * l£U;Thodos£©ft:rc#fJf£fflffi#fitffi(i, 8!tta5 [96] gXtmaHStt ,
(1) £EJ t&, ttttftaR^iSeil^roiftETOllfflx-^^Mo (2) Wf i#S :S .y : ^fe#^ tC '3^r^ iRiJ f : -^©( i t .o#7 i^#^o <3) mzmRm%iz-o\,^x, m%.mMfflv>m^±£<, *£, g^ft^-^bti-n^jgjg
- 7 4 -
.JAEHI-;o..1 93-029
5. ま と め
水蒸気改質器を用い天然ガスから水素とメタノ -J~を製造するシブiテムを高温ガス炉に接続し
た全体システムの設計並びに過渡解析を行うために不可欠な水素,一酸化炭素,二回化炭素及び
メタンの熱物性値(密度,定圧比熱.fM主係数及じ:熱伝導率)の推算式を選定した。選定にあた
っては.これまでに提案されている代表的な推算式をりストアップし,推算式導出の考え方を調
宜し伝iAI1を定性的に検討した。選定推算式を第5.1表にまとめて示す。
これらのH主持式について,実測データ並びに信頼性が高いといわれてL‘る代表的な選定値集に
示されている値と比較することにより,その信頼性を評価した。その結果,次のことが明らかに
な--,1ニ。
(1) 密度については,選定した Peng-Robinson-Redlich-Kwongの状態方程式の推算精度は,
水素に対して概ねO.1 [ 9ti]を下廻り,一般化炭素,二酸化炭素及びメ夕、"ご対しても約2
[Oo]以下であり. HTTR水蒸気改質~~の設計並びに過渡解骨子上十分な精度を有している。
(2) 定圧比熱については,高圧での実測データが不足している現況を考I撃し,実在気体の状態
方程式を用いる方法を選定した。状態方程式として vander Waals式を用いた場合,常圧で
の推算精度は約0.2[%] 以下ア十分な精度である。高圧において,水素に対してはI. O[~ .í]
程度であり,一酸化炭素,二酸化炭素及びメタンも800[K]を超える高温であれば2 L7O]
以下に収まっている。しかし,これら 3流体の場合,高圧・低温側で精度が悪くなり,
5.0[MPa]では10[9o]を超えている。この原因は,用いた状態方程式の精度がこの範囲で
悪いからであることカ、明らかとなった。そこで,精度の良い Peng-Rotinson-Redlich ~{wong
式を用いた場合について検討を進めている。
(3) 粘性係数については,選定したThodosらの次元解析法の推簿精度は.常圧においては水素
を除き概ね 5 [%]以内に収ま「ており,水素についても最大で約 7 [96]である。高圧に
おいてはメタンを除き概ね 5[96]以内に収まっており.メタンについても10[96]を超え
ることはない。実測データのばらつきを考慮すれば.工学的には十分な精度であるといえよ
つ。
(4) 熱伝導率については,比較する選定値の温度範囲が限られている等のため,厳密な議論は
できないか,選定したThodosらの次元解析法の推算精度は,概ね 5[96]程i芝と推測され,
水蒸気改質器の設計上あるいは過渡解析上十分な精度を有しているとl、えよう。
この比較評価を通して.推算式の信頼性を評価する基となる実測データ並びに選定fjt[集に次の
課題があることが明らかになった。
(]) 定圧比熱,粘性係数及び熱伝導率の高圧での実測データ不足。
(2) 粘性係数及び熱伝導率について実測データのばらつきが大きL、。
(3) 特に熱伝導率について,選定値集問の違いが大きく,また.選定値が与えられている温度
範囲が低温に限られ.さらに限定された狭い範囲の場合が多い。
従「て,より信頼性の高い推算式パッケージを構築するためには,実測データのばらつきを低
-71-
ー唱圃

.JAKHI- M 93- U29
^m^mxm^Ltzmu^ii, Q&®?xm%m®ffi&uxTi>-k>9-xmMnisLk-cmm
H * « « ¥ £ £ * ? © r ^ ^ g j <c*-^i»^'<7^-y* <H*)l-7-*P5Sfilf©tfS:VX7 iA-tr>3' - *a f fHH»±rWf f l s rHr*«o *fc. KS«f f i i$©t t l l«»«C#Kt tJ tSyt ( i . f f » 4 C
©**»it««ii^©ffl<:ii^a*c#-rsB^n**s-r**B*<*o. <m c © * » * * *
- 7 5
.1.¥1-:1¥1 -~I 8;j-U29
滅するための信頼性の高い試験方法によるデータの蓄積か必要であり,これに基づいて信頼位の
高い.また温度範囲か十分広い選定値を確立するとこか是非とも必要である。
本報告書で選定した推算式は,日本原子力研究所の情報システムセンタ一大型計算機上で利用
可能なようにコード化しである。さらに,この推算式コードPROPERTYには,本報告書で検討した
選定値集との比較検討を行えるように,これらの選定値を組手込んである。
水蒸気改質器の設計を行う上で,この他.水蒸気の熱物性績が重要でちる~ ~れについては,
日本機械学会発行の f蒸気表Jに基づいたパッケージが日本原子力研究所の情報システムセンタ
一大型計算機上で利用可能である。また.配管破断時の臨界流評価に必要な比主主比は,付録4に
示す式(付 4. I )を用Lて定圧比熱から精度良く求めることかできる。
水蒸気改質器の改質プロセスガスの熱物性値を縫算するためには,本報告書で選定した各単体
の熱物性値縫算式の他に混合気体に対する混合則を確立する必要があり,今後,この検討を進め
る計画である。
一15{7ら
•

JAERI-M 93-029
*5. im m % L fc & tt IS
isans* * ft * *
RT a(T)
V-b V(V+b)+b(V-b) . a(T)=a(T)-a*(T.)
[af(T)] , ,» = 1 +(0.37464+1.542266)-0.269926>l)x(l-T , "*). a - (T«)=0.45724 Pc
b =0.0778 • P.
ZZX: P : « « E * t a t n ] . V : =:;H*»[ crf/g-»l]. T: «JttfiS[K]. B : HRSW*3£*=82.0568[ar • ati/g-«l-K]
E
it ft
E 100[K]£TS400[K]-Cii,
C? /4.1840=1.46910+1.60057 xlO"2xT-4.44048X10"' xT 2+421220xi0-'xT >
400[K]<TS1500[K]T-Ii. Cf /4.1340=3.56903-4.89590X10-'xT+6.22549xl0-T
x ? 2 - l . ^SextO^'xT'
250[K1STS615[K)-C«. CJ /4.l840=O.256859-6.46329xlO-,xT+1.31865xl0-7
xT'-2.65440X10"" x r
6l5[K)<TSl500[Kltli. CJ /A. 1840=0.210345+9.44224 x 10* xT-1.94071 x 10"»
xT 1 -2.35385x10-"
200[K]STS590[Ki CJ /4.1840=0. li S
XT:
590[K]<TSI500[K.l CJ /4.1840=0. IS!!
xT--
E T
ffi C .
. / 6 2V \ / 9'V \ / 2 a 6a-b C. =C?+(C....,)Tx4.1840/41.3187M. ( A C . „ , ) T = - T J dP. =8* •
• \ BV } . \ SV I. \ V V
ZZX: C. : SEifcfSMJ/g • K]. AC.... , : i^HHft©»£W-atw'g-«ol-KI. M: #-f»[g/g-»ol]. P:E2i[atm
E T-©
T£50[K]Tli, U' =0.643 xlO-'xT0- "
50[K] <TTii, U' =9.071X10"TX(0.1375T-1.67)""
zzz: *£':ttttg»[Pa-s]
T.S1 5-Cli. » • x f = 3 . 4 0 x l O - , x T , , , « . f=T. '• '* /«•"
1.5<T,£3(VCtt. #* x f =1.778X10-1X(4.58T,-1.67)5"
E
©
o,S3.or-i±, [ ( t f - ^ ' ) x f x lo J + 10-,]'-'4=0.10616-0.042426 x p, +0.17553X o ,J-0.12295X p.'+0.028149X p,«
CCT-, tf : t t t t«»[Pa-s ]
0.02Sp,S3.0r-(i. [ill -U") X S X103+10"«] '"=0.10230+0.023S
G
E r-©
0.5£T,S50T-li, ( A • x 0/418.4=44.08x 10"5x [eXp(0.0102T,)
-exp(-0.0474T,)]
ZZX: A* :*»»£*¥[«/(»•©]. f=T c"' ,xM"VP « a "
0.5STrS10-C(i. (A 'x f)/418.4=34.98X10-[1.0-cxp(-0.095T,)]
0.4^T,g5"Ci4. (A'xf)/418.4
E T ©
200[KUT51250[K]-m, A = A' + AA AA=1.163xlO-«xA(T)xAP ACT)=8.0323-7.9882X10"'T*-'+3.7718X 10-*T
-8.9760xl0- 4 xT , '+8.4080xl0-'xT' AP =P/9.80665X104-1.03323
ZZX. A :«H£»¥n/Oi-IO]. T:«8EB]. P:E*[Pa]
p rS0.5"Cli. (A-A") x f xz«V418.4=14.0xiO-'x[eip(0.5o-.
0 . 5 < p , £ 2 . 0 m (A - A') x f xz.'/418.4=13. lxio-'x[exp(0.67
2 .0<p ,£2 .8 -m, ( A - A ' ) xrx2. , /4l8.4=2.976xl0- , x[exp(l . lc
ZZT-. z.=P.V./(RT.) : ffl»E«ff»
S E C T I 0 N 1
J:\~:H) -~I 93 -029
熱物性信
第 5.1表選定した熱物性錐
水
4・- . 化 炭 素棄
密 度
的一吋一
+
町一川
a(T)=a(T) . a・(T.)R:r,
[a(T))l/Z = 1 +(0.374倒+1.54226ω-0.26搬 ω勺x(1-T, '''). a'ω=0.45724 一一Pc
民b =0.0778-
P.
ここで. P:絶対圧力(at圃1. Y: モル体制~/&叩1). T:絶対温度[K).R: 一般気体定量生=低価回[~'at的1闘1・K)
零
庄
カ定 で
の圧 値
比
高熱 庄
での
僅
C.
常
圧
で
の
値μ
常圧
でのA・
熱
伝
率での
値
λ
2OO[K] ~星 T~590[Kj:1c; /4.1840=0. l'吋!
xT-
100[KJ ~T~400[K]では,C~ /4. 1840= 1. 46910+ 1.60057 x 10-2 xT-4. 44048 x 10-1
xT'+4. 21220x 10-' xT'
おO[Kl~五T壬615[K] では.c; /4.1840=0.25償却-6.組問x10-0 xT+1. 31865x 10・y
XT2一之民44OXI0・"xT'
400[KJくT壬1500[K]では.
C. 14.1840=3.56903-4.89590 X 10-< xT+6.22549xl0・TxT2 -1.19686x 10-'・xT'
615[Kj<T~1旬。[K!では.c; /4. 1840=0.210345+9. 44224x 10-5 xT-1. 94071 x 10-0
x1・2-2.ぉ385xl0・..
590[K] <T&; 15oo[K c; /4.1840=0. 1:;::1
• Iθ2y ¥ c. =C~+CC.. ..,}, X4.1840/41. 31幻弘 (aC.. ..,),=ーTII一一一 IdP.
・¥8T2 I (手)プ(子ーヰここで.C.:定圧比熱!JIg.K!. .d.C・...1 :定圧分子熱の剰余[ol.atalg唱。1.K!. M:分子量[&lg-.ol].P:圧力[atm
T壬50[KIでは,
μ・=0.643X 10-1 xT'・H
T.~1 5では.1l' xE=3.40xl0-1xT,".... E=Tc"'/GI'/z
50[K) <Tでは,μ・=9.071x 10・'x(0.13花,T-1.67)“
1.5<T. ':>30では.μ. x E=I.π8XI0・τx(4.隠れー1.67)"・
ここで, μ・:枯佐係数[Pa.sl
ρ , ~3.0では,[(μ一μ・)xExIO'+IO-‘]'/・=0.10616-0.042426×ρ,+0.17553x /) ,2-0. 12295xρノ+0.028149Xρ,‘
0.02~ρ ,;:0 3.0では.((μ -1l・)x E XI0'+10-0
]"・=0.10230+0.02336
ここで.μ:給性係数[Pa.sl
0.5~T,壬 50では,
(λ'x n/418.4=44.08xW'x[exp(0.0102T,) 10.5&;T,孟10では 10.4孟T,壬5では.
-exp(ー0.0474T.)) I (λ. x ()/418. 4=34. 98x 10-0 [1. O-CIP( -0.鵬,T.)! I (il'x 0/418.4
ここで, λ・:熱伝導率[胃'/C血.K)].t =Tc'/o XM'/21P .2ノS
2OO[KJ ~T孟 1250[K] では,.1.=.1.・+.d..1.
a.1. =1.163x 10-0 XA(T) X aP A(T)=8.0位3-7.9882x 10・ 'T1• ・ +3.7718x ¥O-2T
-8. 9760x 10-' xT'・+8.4080X 10-1 XT2 .d.P =P/9. 80665x 10・-1.03323
ρ,妥0.5では,〈λーλ・)X r xz."/418.4=14.0x10-lx[exp(O.5に
0.5<ρ,=02.0では.〈λーλ・)X r xz.・/418.4=13. 1 X 10-' X [exp(O. 6:
ここで. il:熱伝導率[胃vc皿・防1.T:温度[Kl.P:庄カ[Pal2.0<ρ,Z五2.8では,{λーλ・)x r xz.・/418.4=2.976xI0-' X [exp(l. 1
ここで. z.=P.Y./C町.):臨界圧縮係書E
一
a
,••• -
MNH
一nHU
日
TE'
)nthw
「トL
戸、
-u

• JAI-.Iu M '.» H29
I & S /£ L fc » 14 tt * St
48
ft K *
J6992OJ : )X(I -T , "«). a" (Tc)=0.45724
- » ft K *
R 2Tc
P<
K = 82 .0568 [of • atn/g-mol -K]
6.46329 < I 0 " ! x T + 1 . 3 l 8 6 5 x 10" 1
••440 •< 10" " X T '
• 9. 4 4 2 2 4 x l O - ' x T - | . 9 4 0 7 1 x 1 0 - ' S385X10-"
200[K]STg590[K]T-(±. C? /4-1840=0.105914+4.03552X10"' xT-3.03235X10"'
XT*+8.29431X10" "XT*
590[K]<TS1500[K]-Cli. C? /4.1840=0.135069+2.89483X 10*XT-1.64998X10"'
xT*+3.53157X10-" XT»
270[K]£T£790(K]-C-ra, C; Ik. 1840=0.458066-2.61341 x 10'* xT+2.07904x10"*
xr-1 .25017xi0- 'xr
790[K]<TS1500[K]-CU. Cf /4.1840=0.0258866+1.60802 x 10"' XT- 6.67069 x 10"'
XT, + I.06432xi0- , ,XT'
r ! I dP. a:v 2a 6 a - b \ / a 2 a - b \* =R J - ( / P +
V 3 V* / \ V* V 3 0 \ dV I. \ dV
• Ricaf-atm/g-mol -K], H: »^«[g/g-mol]. P : JE^tatm], T:fiS[K]. V: tAttflNaf/g-wl]
T, £1.5T'li. u' x f = 3 . 4 0 x i O - ' x T , , - , \ f=T."7(H" , xP J ,«")
1.5<T, S30-CI4. U' x f =1.778xlO-Tx(4.58T,-1.67)•'•
0.02gp,S3.0T-(±. [(.it- u") x f x 10' + 10"4] '"=0.10230+0.023364X p r+0.058533x p r
2-0.040758x p r'+0.0093324x p ,*
;S*io- ![i.O-exp(-0.095T, )1 0.4£T,S5TI±,
(A•'x f)/418.4=6.54xI0"s[exp(0.2826T, -exp(-0.3876T,2)]
273[K]£T£t270[K]?-ti. A* =-1.869 xl0- 3+8.727xl0- ,xT+1.179xl0- 7xT ,
-3.614X10"" XT'
p,S0.5T-fi, (A-A") x f xZ c'/418.4=14.0x10"'x[exp(0.535p,)-l]
0.5<fl r^2.0r-|i, (A-A*) xfx Z c V418.4=13. lxlO-'xtexpC0.67p,)-l. 069]
2 . 0 < p r £ 2 . 8 m (A-A") x f X2.V418.4=2.976X10"'x[exp(I.155p,)+2.016]
ZZX. z.=P.V./(RTO:BMffi««R
- 7 7 - 7 8 -
S E C T I O N 2
J.¥J'.hi .¥1 'J:l IJ~~
長 選定した熱物性推算式
物
化炭素 棄炭化
賞一一霞 メ タ ン
R2Tc'
~1)992w') メ(1 -T , '〆'). a' (Tc)=0.45724 P.
敬三82.0568[a1 . atmlg-目。l・K]
6.46329< 10" xT + 1. 31865x 10ーマ.140< 10'" ><T'
200[K] ;>;T孟590[K]では.C~ /4.. 1840=0.105914+4.0お52x10-0 ><T -3.03235>< 10-'
xT'+8.29431xI0・"x!,
270[K) ;:>;T壬790[K)では.c; /4.1840=仏458066-2.61341 xlO-o xT+2. 07904xI0-1
XT2- 1.お017x10-' xT'
9.44224ベ¥0"ベT-1.94071 x ¥0" ろ385ベ10司"
590[K] <T孟1500[K)では.C~ /4.1840=0.135069+乙89483x10-0 xT-l. 64998x ¥0"
xT'+3.53157xI0・11xT'
T切 [K)<T;:>;15∞[K)では.C; /4. 1840=0.0258866+1.印802x¥O-'xT-6.67侃9xl0-'
xT'+1.侃432xiO・"xT'
HfL)e (手).=R'. (子-ぞ)/(P-:' +ぞ}R:c:r1. at皿/g-mo1• K]. 11:分子量[g/g-mo1J. P:圧力[at田].T:温度[K).V:モ}j,体積[CZ//g叩 1)
T.壬1.5では,μ・ズE'=3.40xlO" xT,・・・.E' =Tc'〆"/01'/, xp c ,.'S)
1.5くT.~30では.μ. >< E' =1. 778XI0" ><(4. 58T,一1.釘)5/'
0.02~ρ ,豆 3.0では.
[(μ ー μ・)><E'x10'+10'O)1/‘=O. 10230 + O. 023364 xρ. +0. 058533 xρ. ' -O. 040758 xρ.'+0.ω93324xρ,・
0.4 孟T.~5では.(λ'x 01418.4=6. 54x 10"' [exp(O. 282飢
-exp( -0. 3876T乃]
273[K)壬T::OI270[K)では.λ・=ー1.869X]O・'+8.727xI0-'xT+l. 179XI0-' xT'
-3.614xI0・11xT' ';8>< 10・'(1.u-exp(-O. 095T. )J
ρ. ~O.5では,
(). -A・)x ~ xZc' /418.4= 14. Ox 10-' x [exp(O. 535ρ.)ーlJ
0.5く ρF孟2.0では.O-A・)x!;' x z. '/418.4= 13.1 x 10-' x [exp(O. 67ρ,)-1.069)
2.0<ρr孟2.8では.(J.-A・)x ~ xz.・/418.4=2.976x10-' x [exp(I.155ρ,)+2.016J
ここで. z.=P.Vc/(貯.):臨界圧縮係数
-77-78-
S Ecj|ON町2'---l

•IAKKI M 93 IC9
m &
53%gB«IS±^*HTTRIf®^g<rSE<.«l»ti-ro *fc. &SX^g|J<Dg-*:#jgf*?iJffl&«
- 7 9 -
lAEHI . '.1 9:1. {):!9
謝 辞
本報をまとめるにあたり,有益な御助言と終始暖かL、御指導をいただL、た高温工学試験研究炉
開発部の数土幸夫HTTRgt画室長に深〈感謝します。また,高温工学部の宮本喜農熱利用授術
研究室長には貴重なコメントを扱いた。ここに記して深い感謝の念を表す。
nE
η4

• IAKK1-M 9 3 - 0 2 9
# # £ m [1 ] K.Hada et al.. " Thermal Transient Analysis for Structural Integrity of High
Temperature Components in HTTR." Proc. 1st JSME/ASME Joint Int. Conf. on Nuclear Engineering, d-30. Nov.4-7. 1991. Tokyo Japan.
L 2 ] M.Hirano and K.Hada. "Development of THYDE-HTGR : Computer Code for Transient Thermal-hydraulics of High-temperature Gas-cooled Reactor", Report of the Japan Atomic Energy Research Institute, JAERI-M 90-071CApri] 1990).
[ 3 ] {0R(i\ P.G. Hill and R.D.C. MaclKillan. "The Properties of Steam : Current Status." Trans. ASME, J. Heat Transfer. Vol.HOCAugust 198f). pp.763-777.
[4] mm m, Jtrii7A^>if~r')>r- >')-xi, ttgt^fe**--?-^®^
[5 J XiL &=. rgRffl-#©fc»©«tt^Kfl|*i6J . H W I « f f B t t . W»80#12fl. [ 6 ] B * & & t t ¥ & « . rjButtft/N> N'7'-y?J . mrngg, 1990^5M. [ 7 ] R. C. Reid. J. M. Prausnitz and T. K. Shernood. "The Properties of Gases and
Liquids, Third Edition". McGraw-Hill Book Company, 1977. [ S ] J.D. van der Waals. Doctoral Dissertation, Leiden. 1873. [ 9 ] O.Redlich and J.N.S. Kwong, Chem. Rev., vol.44(1949), p.233. [10] Ding-Yu Peng and D.B.Robinson, "A New Two-Constant Equation of State."
Ind. Eng. Chem. Fundam.. Vol. 15.No. 1(1976). pp.59 ~64. [11] M.Benedict. G.B. Webb and L.C. Rubin. Chem. Eng. Prog.. Vol.47(1951). p.419 &
O- J. Chem. Phys. Vol. 8(1940). p. 334*. [12] L.Riedei, Chem. fng. Tech.. Vol.26(1954). p.83. [13] D.J. Berthelnt. J. Phys. Vol.8(1899). p.263. [14] Ihsan Barin, "Thermochemical Data of Pure Substances, Part I , " VCH
Publishers. 1989, pp.1 ~15. [15] S. Chapman and T.G. Cowling. "The Mathematical Theory of Non-Uniform Gases",
3rd Edition, prepared in cooperation with D.Burnett. Cambridge University Press, London, 1970.
[16] D.Enskog, Kgl. Svenska Vetenskapsaked. Handl. Vol.63, Na 4(1921). [17] L. I.Stiel and G. Thodos. " The Viscosity of Nonpolar Gases at Normal
Pressures", A. I.Ch.E. Journal, Vol.7, Na 4(December 1961), pp.611 ~615. [18] H.Shimotake and G. Thodos, "Viscosity: Reduced-State Correlation for the
Inert Gases," A. I.Ch.E. Journal, Vol.4, Na 3(Sept. 1958). i.p.257 ~262. [19] A.K. Abas-Zade, Zhur. Ekspl. i. Theoret. Fiz., Vol.23(1952;. p.60. [20] J.A. Jossi, L I . Stiel and G. Thodos, "The Viscoity of Pure Substances in the
Dense Gaseous and Liquids Phases", A.I. Ch. E. Journal, Vol.8, Na KMarch 1962). pp. 59 ~63.
- 8 0 -
.I:¥EI<I-¥1 93 --029
参 考 文 献
[1] K.Hada et al..“ Thermal Trassiest Asalrsis for Structural 1I1iegrit). of High
Temperalure Componenls in HπR.. Proc. Isl JS!lE/AS!lE Joinl lnt. Conf. on
Nuclear Engineering. d-30. Nov.4-7. 1991. Tokyo Japan.
l 2 ] M. Hi rano and K. Hada. “Deve!opmenl of THYDE-HTGR : Computer Code for
Transienl Thermal-hydraulics of High-temperature Gas-cooled Reactor¥Report
of the Japan Atomic Energy Research /nstitute. JAERl-!I 90-071(April 1990).
[ 3 ] 例えば. P. G. Hill and R. D. C. MacMi Ilan.“The Properties of Steam Current
Status.. Trans. ASME. J. Heat Trallsfer. Vol.llO(August 1980. pp.763-777.
[ 4 ] 蒔田 董ケミカルエンジニアリング・シリーズ 1.紘度と熱伝導率ーデータの検
索と計算法い蜘培風館,昭和50年5月.
[ 5 ] 大江 修三設計者のための物性定数推算法1.日刊工業新聞社,昭和60年12月.
[ 6 ] 日本熱物性学会編熱物性ハンドブック J. 働養賢堂. 1990年5月.
[ 7] R. C. Reid. J. M. Prausni tz and T. K. Shernood. “The Properlies of Gases 耳目【i
Liquids. Third Edition¥McGraw-Hi Il Book C,1mpany. 1977.
[ R ] J. D. van der Waals. Docloral Dissertation. Leiden. 1873.
[9J O.Redlich and J.N.S. Kwong. Chem. Rev.. vo1.44(J949). p.233.
[10] Ding-Yu Peng and D.B.Robinson. “A New Two-Constant Equatioll of State..
lnd. Eng. Chem. Pundam.‘ Vol. 15.N~ 1(1976). pp.59 --64.
[11] M.Benedict. G.B. Webb and L.C. Rubin. Chem. Eng. Prog.. VoI.47(I95l). p.419及
ぴ J.Chem.Ph)s. Vol.8(1940). p.334等.
[12J L.Riede1. Chem. Ing. Tech.. Vo1.26(I954). p.83.
[I3] D. J. Berthelnl. J. Phys. VoJ. 8(1899). p.263.
[14] lhsan Barill. “Thermochemical Dala of Pure Subslances. Part 1.. VCH
Publishers. 1989. pp.l --15.
日5J S. Chapman alld T.G. Cowlillg. “The Mathematical Theory of Non-Uniform Gases¥
3rd Edition. prepared ill cooperatioll with D.Burnett. Cambridge University
Press. London. 1970.
[16J D.Enskog. KgI. Svenska Vete尚 kapsaked.Handl. Vol.63. N~ 4(1921).
[17J L. J. Stiel and G. Thodos. “The Viscosity of Nonpolar Gases at Normal
Pressures". A. 1. Ch. E. Journal. Vol. 7. N~ 4(December 1961). pp.611 ......615.
[18] H.Shimotake and G. Thodos. “Viscosity: Reduced-State Correlation for the
'nerl Gases.. A. 1. Ch. E. Journal. Vol. 4. N~ 3(Sept. 1958). l.p.257 --262.
[19] A. K. Abas-Zade. Zhur. Ekspl. i. Theoret. Piz., Vol. 23C1 952~. p.60.
[20J J. A. Jossi. L. l. Stiel and G. Thodos. "The Viscuity of PurιSubstances in the
Dense Gaseous and Liquids Phases¥A.I. Ch. E. Journal. Vol.8. N~ l(March 1962).
pp.59 ......63.
-80-

.lAKKl M W;f U2H
[21] D. Reichenberg "The Viscosity of Pure Gases at High Pressures." NFL Rep. Chem. 38. National Physical Laboratory. Teddington. England. August 1975.
[22] R.C. Reid et al.. "The Properties of Gases and Liquids". 3rd Edition. McGraw-Hill. 1977. p. 430.
L23] D. Hi. sic and G. Thodos. A. I.Ch.E. Journal. Vol. 7(1961). p. 264. [24] D. Roy and G. Thodos. "Thermal Conductivity of Simple Gases at Normal
Pressures." The Canadian J. of Chemical Engineering. Vol.46(April 1968). pp.108 -113.
[25] D. Roy and G. Thodos. "Thermal Conductivity of Gases. Hydrocarbons at Normal Pressures". I & EC Fundamentals. Vol.7. Na 4(Nov. 1968). pp.529~534.
[26] J.T. Kennedy and George Thodos. A. I.Ch.E. Journal. Vol.8(1962). p.59. [27] A. S. Predvoditelev. J. Phy. Chem. (U.S.S.R.). Vol.22(1948). p. 339. [28] L.1. Stiel and G. Thodos. "The Thermal Conductivity of Nonpolar Substances in
the Dense Gaseous and Liquid Regions." A. l.Ch.E. Journal, Vol.10, Na 1 (Jan. 1964). pp.26 —30.
[29] J. Hilsenrath. C.W. Beckett et al., "Tables of Thermal Properties of Gases. Comprising Tables of Thermodynamic and Transport Properties of Air, Argon, Carbon Dioxide. Carbon Monoxide, Hydrogen, Nitrogen, Oxygen and Steam." United States Department of Commerce National Bureau of Standards Circular 564(Nov. 1955).
[30] Y.S. Touloukian and T. Makita, " Thermopbysical Properties of Matter. The TPRC Data Series, Volume 6, Specific Heat, Nonmetallic Liquids and Gases." IFl/Plenum, New York-Washington, 1970.
[31] Y. S. Touloukian. S.C. Saxena and P. Hestermans." Thermophysical Properties of Matter. The TPRC Data Series, Volume 11. Viscosity." IFl/Plenum, New York-Washington. 1975.
[32] Y. S. Touloukian, P. E. Li ley and S.C. Saxena, "Thermophysical Properties of Matter, The TPRC Date Series. Volume 3, Thermal Conductivity. Nonmetallic Liquids and Gases," IFl/Plenum, New York-Washington, 1970.
[33] JiSti, H. B. BAPTAOTMK, " C n P A B O q H H K 110 TEnJIOOH3MqECKHM C B O B C T B A M TA30B M JKMflKOCTEK, M 3 H A H H E BTOPOE, HO II O J1HE HHOE M I1EPEPAEOTAHHOE" , M 3 fl ATE Jib CTBO «HAyKA» TJIABHAH PEflAKUHfl <X>I43MKO-MATEMATimECKOfl JIMTE P ATy PLI, MOCKBA, 1972. w>ma, B • •mwatmrnm. r«jt %fctmfc<Dfmw&)®.Ki, B • vinttt, fPS^Oim, Bg*n.49ifl0£.
- 8 1 -
.J.-¥E1il ¥1 !-J;! O~~
[21J D. Reichenberg“The Viscosi ty of Pure Gases at High Pressures. " NfL Rep. Chem.
38. National Ph~'sical laborator)". Teddington. England. August 19'.'5,
[22] R. C. Reid et aI.. “The Propert ies of Gases and Liquids". 3rd Edi tion. McGra冒ー
Hill. 1977. p.430.
[23] D. &i!sic and G, Thodos. A. 1. Ch. E. Journal. Vol. 7(1961). p.264.
[24J D. Roy and G. Thodos. “Thernal Conductivity of Simple Gases at Nor鵬 1
Pressures." The Canadian J, of Chemical Engineering. Vol.46(April 1968).
pp.l08 -113.
[25J D. Roy and G. Thodos. 寸hermalConductivity of Gases. Hydrccarbons al Normal
Pressures". 1 & EC Fundamentals. Vol. 7. No. 4(Nov,1968). J:p.529-534.
[26] J. T. Kennedy and George Thodos. A.1. Ch. E. Journal. Vol. 8(1962). p.59.
[27J A. S. Predvoditelev. J. Phy. Chem. CU. S. S. R.). Vol. 22(1948). p.339.
[28] L. 1. Stiel and G. Thodos. “The Thernal Conductivi ty of Nonpolar Sub5tances in
the Dense Gaseous and Liquid Regions." A.l.Ch.E. Journal. Vol.10. No. 1 (Jan,
1964). pp.26 -30.
[29] J. Ili lsenrath. C. W. Beckett et al.. “Tables of Thermal Properties of Gases.
Comprising Tables of Thermodynamic and Transport Properties of Air. Argon.
Carbon Dioxide. Carbon Monoxide. Hydrogen. Nitrogen. Oxygen and Steam."
Uni ted States Department of Conullerce National Bureau of Standards Circular
564(Nov. 1955).
[30] Y. S. Touloukian and T. Maki ta. “Thermop!Jysical Properties of Matter. The
TPRC Data Series. Volume 6. Specific Heat. Nonmetallic Liquids and Gases. "
lFliPlenum. New York-Washington. 1970.
[31] Y.S. Touloukian. S.C. Saxena and P. Hestermans." Thermophysical Properiies
of Matter. The TPRC Data Series. Volume 11. Viscosity.. IFI/Plenum.
New York-Washingion. 1975.
[32] Y.S. Touloukian. P.E. liley and S.C.Saxena. “Thermophysical Properties of
Matter. The TPRC Date Series. Volume 3. Thermal Conductivity. Nonmetall ic
liquids and Gases." IFI/Plenum. New York-Washington. 1970.
[33] 原著は. H. E. BAPfAφTMK. “CIIPA80lfHMK IIO
TEII江OφM3MlfECKMM C80OCTBAM fA308 M
iKL1江KOCTElII. 113江AHL1E BTOPOE. LIOIIO刀HEHHOE
M llEPEPAEOTAHHOE". M3且ATEJIbCTBO
<<HAYKA)) fJIA8HA.H PE且AKUM.H φM3!1KO-
MATEMATMlfECKOO 刀MTEPATYPbI, MOCKBA. 1972.
邦訳は,日・ソ通信社制訳部, 「i更覧気体と液体の熱物理的性質J.日・ソ通信社,
和歌山市,昭和49年10月.
-Z4
n口

.IAEK1-M 9H-029
[34] \Hm%mm^. r^g** sMominmmi, B #«*££. ag^ss^sE. [35] m?&®frmm%>. asx-^ajsw^s^ mtw&T-!? mzm (88*154 3 E).
pp.49 ~68. [36] H.CeierandK. Schafer, All gem. Warmetech.. Vol. 10(1961). pp.70~75. [37] L.H.Chen. " Thermodynamic and Transport Properties of Caseous Carbon Dioxide."
CA-1038 (August 1959). [38] F.G. Keyes. "The Heat Conductivity, Viscosity. Specific Heat, and Prandtl
Numbers for Thirteen Cases," Project Squid Technical Report Jfa 37. HIT. 1952.
- 8 2 -
.J:¥EHI-:¥l 9:1-029
[34] 内田秀雄他15名技術資料流体の熱物性値集J.日本機械学会.昭和58年 8月.
[35] 科学技術庁振興局,物性データ調査研究報告流体特性データ第2巻(昭和54年3月).
pp.49 --68.
[36] H.Geier and K. Schafer. A11gem. Warmetech.. Vol.lO(1961). pp.10--15.
[37] しH.Chen. “Thermodynamic and Transport Propl"rties of Gaseous Carbon Dioxide. •
GA-I038 (August 1959).
[38] F. G. Keyes. “The Heat Conductivity. Viscosity. Specific Heat. and Prandtl
Numbers for Thirteen Gases. • Project Squid Technical Reporl No. 37. Mrl'. 1952.
-82-

• J AH Hi M 93 ()L>9
ami m%u: mmmmw-itmmm
' r - X 1* « i i f t l E 2) [ M P a ] fl S [K] 1 * * & a 0.101325 ( = 1 [atm]) 500
2 * * a* s 4.9346 ( = 50[barD 400
3 y n s& a 5.0 600
4 * ? > & £ # ? ; 5.0 600
» - x i ?fcitg>gtEE, 500[K] c:fc<+.5®g
(1) X T - y 7*1 :1 i . |>H^(U**J6§o
* * » . £ T » =20.39[K] i t > , # B I i « * » j £ T » . , * t « ; : R i e d e U C ( i t (2.1.23) ) ©¥„ ( i t (2.1.26) ) , « c ( i t (2.1.25) ) &C/Qtt&®1B£fc-5o
TV, = T t / T c = 20.39/33.2 = 0.61416
Wb = -35 + 36 TV, + 42^nT„. , - T V , 6
= -35 + 58.6167 - 20.4750 - 0.05366 = 3.0 = 0.315 Vb - i n P .
0.0838 f , - i n T , . , _ 0.315 x 3.0880 + I n 12.80
0.0838 X 3.0880 - £n 0.61416 = 4.7197
3.5222 0.7463
Q = 0.0838(3.758- o . ) = 0.0838(3.758-4.7197) = -0.08059
RiedelitcD&t?.£^&© ±-5 (::/£ 3 © T ,
A* = - 3 5 = +2.8206
B* = -36Q = +2.9011 C* = 42Q+ a . = +1.3349 D* = - Q = +0.08059
* t t t * f i K T r = T/T, = 0.7 Kfctf S f l t t f j a s i E P v p,r JitfC<©±-5 fcfc*.
I n P . M = A* - ^ r - + CT£nT, + D*T,6
• 8 3 -
• .L¥EHI ¥1 日3υ29
付録 l 選定した熱物性値推算式の計算例
第 2章で選定した熱物性値推算式の計算例を示し,式中の各係数がどのような値をとるか明ら
かにする。次のケースについて,
ケース 物 質 熱 物 性 値 圧力 [MPa] 温 度 [K]
水 素 密 度 0.101325 (= 1 [atm]) 500
2 水 素 密 度 4.9346 (=50(bar ]) 400
3 メタン 密 度 5.0 600
4 メ タン 熱伝導率 5.0 600
計算例を各ステップ順に以下に示す。
ケース I 水素の常圧, 500[K)における密度
(1) ステップ偏心因子ωそ求める。
標準沸点T.= 20. 39 [ K ]より,対臨界標準鴻長T...並びにRiedel式(式 (2.1.23))のWb
(式 (2.1.26)) ,α'c (式 (2.1.25))及びQは次の値となる。
Tb., = Tb/T, = 20.39/33.2 = 0β1416
耳'.ー35+手ー+42Rn Tb.. -Tb., . .1. b. r
= -35 + 58.6167 -20.47印-0.05366
= 3.08剖
α 0315 Wb - fn p,
0.0回8W.-fnT...
0.315 x 3.0880 + Il n 12.8o 3.5222 0.0田8x 3.0880 -R. n 0.61416 0.7463
= 4.7197
Q = 0.0838 (3.758 -α,)ニ O.佃38(3.758 -4.719η
= -0.08059
Riedel式の各係数は次のようになるので,
A‘=ー35= +2.8206
B+ = -36Q == +2.9011
c+ = 42Q + a. = +1.3349
D+ = -Q = +0.伺059
対臨界温度Tr= T/T, = 0.7における対臨界蒸気圧 Pvp,r は次のようになる。
IlnPv.., A+一千+口nT, + D+ Tr"
向。00

JAEH1-M 93-029
= 2.8206 - ( " l " 2 ' ^ ° 7
1 1 ) + 1.3349in0.7 + 0.08059 X 0.7*
= 2.8206 - 4.1445 - 0.009481 = -1.7905
.-. P.p., = 0.1669
w = -logi0 l \ p . r - 1.0 = 0.7776 -1.0 = - 0. 2224
*%iz®--<tzi.nz, i'AW^^StCDXHIt"' O T ; £ t r a ^ a > = 0 . 0 © ^ J i ^ l f i i © ^ !*Wi'®T', ;;tiiw=o.o t-r-So tets. # % * T ! : . I M E P . u ! [mmHg] ^f td/ j r f Antoine©jW^3*to3 fc,
B lOgwP.P.HI = A ~ t + c
CC-C, t : JgJS [°C] u) = -0.2232tKZo
(2) 7y--jf2 : Peng-Robinson-Redlich-Kwongjt©^gra(T)SO:b^Jfa6.5o a ( T ) = a ( T ) • a ' (Tc) £ L T . a(T)&tfa*(Tc) ti#*StC2.1.19), ^ (2.1.20)
[ a(T)]"' 2 = 1 + (0.37464 + 1.54226a) - 0.26992a)2) x (1 - T." 2)
= 1 + (0.37464 + 1.54226 X 0.0 - 0.26992 x 0.02) X [ 1 - f - J | | j ' " |
= 1 + 0.37464 X (-2.8808) = -0.07926
.-. a(T) = 6.2826 x 10"3
a*(T<) = 0.45724 R ' T c ' = 0.45724 82-05682 • 33.22
Pc «-™"« 1 2 8 o = 2.6519 X 105
ii£->-C. a (T) t i ^©t t t<£So a (T) = a(T) • a*(T.) = 6.2826 x W x 2.6519 X 10s
= 1666.1 \fm'™! 1 L (g-mol)2 J
(sl#<:. b i i i t (2.1.21) ^t.ftfflflt<i:5
b = 0.07780 - ^ - = 0.07780 - ^ 2 - 0 5 6 8 * 3 3 - 2
Pc v - v " ' " " 12.80 = 16.559 [caf/g-mol]
- 8 4 -
(2)
JAEHl-M 93-029
( +2.9011) = 2.8206一一一一一一一ーー+1.3349.11 n 0.7 + 0.08059 x 0.7"
0.7
= 2.8206 -4.1必5-0.009481
-1.7905
P..., = 0.1669
従「て,偏心因子ωは次のように求まる。
ω=一logwP叩.r-1.0 = 0.7776 -1.0
=リ.2224
本文に述べたように,古典的な多数の文献山に示されているω=0.0の方か選定値との誤
差カ、少ないので.ここではω=0.0とする。
なお.参考までに.蒸気圧 PVP.旧[田皿IIg]を次に示す Antoineの式から求めると,
!Og,0 PvP.HO A一一旦ーt+c
ここで t 温度 [OC]
ω= -0.2232となる。
ステップ2 Peng-Robinson-RedJich-Kwong式の定数a(T)及びbを求める。
a (T)=α(T)・aぺT,)として, α(T)及びa・(L)は各身式(2.1.19),式 (2.1.20)
から,次のf直となる。
[α(T)]V' = 1 + (0.37464 + 1.54226ω-0.26伺2ω')x (1-TY')
f. (500)ν21 = 1 + (0.37464 + 1.54226 x 0.0 -0.26992 x 0.0') x I 1ート一一 I I
l . I 33.2 J J
= 1 + 0.37464 x Cー2.邸佃)
-0.07926
a(T) = 6.2826 x W-'
τ"町、 2
a*CT,) = 0.45724 "p~c = 0.45724 82郎飽2・33.2'
12.80
= 2.6519 x 10'
従って. a (T)は次の値となる。
a(T) =α(T)・a.('f',)= 6.2826 x lO-' x 2.6519 x 10'
= 1666.1 I旦旦2旦:-1L (g-mol)' J
同様に, b は式 (2.1.20から次の値となる
D中 82.0568・33.2b = 0.07780 一一~= 0.07780.
12.80
= 16.5四[CDf/g-moJ]
-84-
一一司回

•IAKK1-M 93-029
(3) X f ^ 3 : 3!%im&. i t (2. 1.29) ffl&i*£St £ * * . £ =
tf.&tf/^liit (2.1.27) fr £&©*£££«<,
a ( T ) - P _ 1666.1 x 1 iS , = R 2 T 2 82.0568 X 5002
= 9.8976 x 10"
o _ b • P _ 16.559 x 1 P 2 — RT 82.0568 x 500
= 4.0360 x 10"'
SEoT. B,€B2kte->X\,>2»,
i t (2.1.29) (±&©fcfcf) 0
x 3 - O - i S O x 2 +(B,-3B?-2Bl)x-(.B1 • 0 , - B}- /S2
3) = 0
1 - /8, = 1 - 4.360 X 10* = 0.9996
3, -ZB}-2Bt = 9.8976X10 7 - 3 x(4.0360 X 1 0 " 4 ) 2 - 2 X4.0360X10"4
= 9.8976 X 1 0 ' - 4.8868 x 10 ' -8 .0720 x 10-' = -8.0670 X 10-' (=-2B2)
Bi'p,- Pf-B,3 = 9.8976 X10"7X 4.0360 X 1 0 " - (4.0360 X10" 4 ) 2 - (4.0360 x 1 0 ' ) 3
= 3.9947 XIO" 1 0 - 1.6289 X10" 7-6.5744X10"
= -1.6256 X10"7 (== -B?) ftoT, M<^£3ik-ft®ftl±lk®kt=l)0
x3 - 0.9996 x 2 - 8.0670 x 10"' x + 1.6256 X 10"7 = 0
(4) X f ^ 4 : 3 <fc£gjt£Jif < o -*£<:, &©3&;£il5t
aox' + a , x ! + a s x + aj = 0
a ; + ( a i ' + 4 a , 8 ) ' / i 1 _,_ f - a , + ( g i
i + 4 a , i ) , / i 1 a, A - [ " - « « + ( a . ' + 4 a , > r 1 1 , I" - a , + ( g i
i + 4 a , i ) , / i 1 3a 0
; : T ,
„ - a,2 a 2
9 ao2 3 a»
2 ai 3 ai « a ; , as " 1 " n 3 ~"~ 27a„3 3ao2 ao
a o = l . a i= -0.9996, a 2 =-8 .0670MO" 4 , a 3 = 1.6256 x WZRKirZ, t . £ * © « I 2 # C ©
J; •J I ' ^ - so
„ _ a,2 , a, _ (-0.9996)' , (-8.0670 X 1 0 4 ) a , - - g - + - g - - 9 + g
- 8 5 -
1 Jλトml-~I 9:1-029
ステップ 3・ 3次方程式.式 (2.1.29)の各係数を求める。
β:及びβ2は式 (2.1.27)から次の値となる。
(3)
1666.1 x 1 82.0568 x 500'
DA-
--;
一
T
、、,J-
IE
ぐ一R
a一1
8・
= 9.8976 x 10-7
β b ・P 16.559 x 1 -一-RT 82.0568 x 500
= 4.0360 x 10-'
従って, β , ~β2 となっている。
式 (2.1.29)は次のとおり。
x3 - c1一β,)x' + (β,-3β,'-2β,) xー(β1・ββJ-βi)= 0
上記β" β2の値を代入すると各係数は次の値となる。
1一β2= 1 -4.360 x 10-' = 0.9996
β,-3β.'-2β, = 9.8976 X1Q-7 - 3 x(4.03曲 XlO-')'-2 x4.0360xlO-・
= 9.8976 x 10-7 - 4.邸68X 10-7 - 8.0720 x 10-'
= -8.0670 x 10ぺ(さ一2β,)
β1・ムーβJ-βi= 9.8976 X 10-1 X 4.0360 X 10-'ー(4.0360X 10-')'一(4.03旬 XI0・y= 3.9947 x 10-'.ー1.6289X 10-7
- 6.5744 X 10-11
-1.6256 X 10-7 (さーβ,')
従司て,解くべき 3次方程式は次のとおり。
ピー 0.9996x' -8.0670 X 10-' x + 1.6256 X 10-7 = 0
(4) ステップ 4: 3次方程式を解く。
一般に,次の3次方程式
ao X3 + a, x' + a, x十 a.= 0
の恨の一つは次式から求めることができる。
a, 3 ao
x = [一α,+(す+4a ,')'ノ~]ぺ
ここで,
a 2 a J a2 2 一一一一一一+一一一-,- 9 aa' 3 a.
α22af az・a, a, 一一一一一+一一一一一一+一一-
I - 27a.' 3a.' a.
向=1. aJ=-O.9996, a2=-8.0670><1O-., a3=1.6256x10-7を代入すると.各キの値は次の
ようになる。
、
.a'-f nu-
-A阻x-のU百
a
't-Mw
一oo-
Fhd
oo
α1-af h-(一0.9996)', 一一一一+ー~一一一一一一一一一一ー+9 .
3 9

JAER1-M 93-029
= -0.1110 - 2.7339 x 10" ; = -0.1113
_ 2a,3 _ a .»a, , _ 2x(-Q.9996) 3 _ (-0.9996) x (-8.0670 X 1 0 ' ) a 2 - 2 ? 3 + a 3 - 2 ? 3
+ 1.6256 x 10"' = -0.073985 - 2.6879 x 10"' + 1.6256 x 10"
= -0.07425 ( = - ^ f f
( a , ! + 4 a , ' ) ' " = [(-0.07425) 2 + 4 x (-0.1113) 3 ]" 2
= [5.5136 X 10"3 - 5.5135 X W-'l'" = [1.2108 x io-']«"• ( ^ H » r ( i / J ^ » ^ H T 8 f f i * T H - » L f c e * ) = 3.4796 x 10"4
0.07425 + 3.4796 X 10-' ) , f 0.07125 - 3.4796 X 10' 4 ) (-0.9996) ' ) + i 0.07125-3.4796 X 10'< 1 2 J I 2 J 3
= 0.3341 + 0.3331 + 0.3332 = 1.0004
xfr\im.OtK&®l*&fflft{Zfr<D&olzmt>£ft&frt>T°h%o BP"&. - a j » ( a 2
2 + 4 a j 3 ) I / 2 ,
ai = 2a, 3/27 r ai = - ( 1 - ft) = - 1 fr <b,
M 1/3 - g z + ( g ;
2 + 4 a , 3 ) ' / 2 1 , f - a i + ( g i
i + 4 a , i ) ' / i i a, 2 J L 2 J 3a„
1 / 3 1/3 « i , _ _a_L | ai 2 J I 2
3 - 1 / 3 1/3 2« i I , 1 2ai ] ai _ a t ai ai .1 +[—2*L.} _.
\ { 2 X27 J I 2 X27 J I 2 X27 J 3 3 3 3
= - a , = 1.0
(5) X f ^ 5 : ®m&$itb%a
V = x - ^ = 1.0004 • 82.0568^X500 = 4 i m Q [ c D j / g . m o l ]
'' = T-=iow = 4- 9 1 1 2 x l o" 6 [^C D f ]
#%*-C<C. r*i!i)tt/N> K ? 7 ? J T-li 4.911 X10"5 [g/cnf] t ^ b n t l ^ ^ .
- 8 6 -
93 -029 JAERI-M
-0.1110 -2.7339 x 10-' -0.1113
(-0.9朗6)x ( -8.0670 x 10-・)3
α 2生主こ主!..J..~ -.1x( -0.9四6)S ー
2 -27 3' ""' - 27
+ 1.6256 x 10-す
= -0.073985 -2.飽79x 10-・+1.6256 x 10-'
=一O仰 5ト与)(α2' + 4 a,')l/2 = [(一0.07425)2+ 4 x (ー0.1113)']1/2
ニ [5.5136x 10-' -5.5135 X 10-']'/2
= [1.21じ8x 10-']ω(実際には小数点以下8桁まで計算した結果)
= 3.4796 x 10-'
( -0.9996) 3
、.. 2
・EEE
・J
4
-nu--4-
X
一
Fhv
一
nuu-nt一
AA
一。,u
q九》一
EU-
nL-
tA-
ηt-nu一--
nり一
,.EEE
・‘t+
x = (~m514796 × l~]
= 0.3341 + 0.3331 + 0.3332 = 1.0004
一的 >>(αzz十4αl3)1/Z,xがほぼ1.0となるのは近似的に次のように表わされるからである。即ち,
α2主 2a/127,al =ー(1-s2)三一1から,
=[-=b+(ai+4α ,')つ/~ [一α2+(プ+4α,')つ/, a, 3ao
== [一号ιJ+ト今) a, 3
~{2a f 11A , iza1311ノ3
2 x27 J 'l 2 x27 J 一主.!..- a, a, a,
3 3一一τ-τ-a, == 1.0
ステップ 5:密度を求める。
モル体積Vは次式から求まる。
(5)
R.T 82.0568 x 500 v xー下一=1.0004・ 1" vvv = 41045.0 [cofゾg-molJ
従「て.密度ρは次のとおり,
M 2.0158 ρ=一一=一一一一=4.9112 x 10→[g/cof] v - 41045.0 - ..."..~ ., .v "0
「熱物性ハンドブックJでは 4.91I x 10-5 [g/cnl' 1と与えられている。
-86-
参考までに,

.IAEKI - M 93 029
- i r - x 2 7fc|?©i^flE50gUE. 400[K] t r - te i fag lg < 1) X T -y 7" 1 : -H'OH^O) £.#*!>-3o
(2) 7sT~j-f2 : Peng-Robinson-Redlich-Kwong^ffl£l&a(T)&tfb£;fc&.5
[ a ( T ) ] 1 / 2 = 1 + (0.37464 + 1.54226w - 0 .26992M 2 ) X ( 1 - TV' 2)
•»"««['-i*r] = 0.07425
.-. a(T) = 5.5124 X 10"3
a*(Tc) = 0.45724 ^ ~ - = 2.6519 x 105
A C
.-. a(T) = a (T) • a*(T=) = 5.5124xl0- 3x2.6519xl0 6 = 1461.8 [ f ~ ^ r ]
b = 0.07780 • - ^ - = 16.559 [cnf/g-mol]
(3) X r » ^ 3 : 8 f t * a i C © # » * * » S o
0 - a ( T ) » P _ 1461.8 X 49.3462 _ 72135.9 p ' R 2 T 2 82.05682 x 4002 1.0773 x 109
= 6.6958 X 10' 5
a - b ' p - 16.559 X 49.3462 _ „ ft9.„„, fil - ~1VT~ 82.0568 X 400 " a w 4 B 9 5
l - > t , Peng-Robinson-Redlich-Kwongi^£g^Lfc#c©3&#fSie
x 3 - ( l - / 9 2 ) x 2 + (/3, - 3 / 3 2
2 - 2 / 3 2 ) x - ( / S , . £ 2 - 0 2
2 - £ 2
3 ) = 0
1 - jS, = 0.97511
£ , - 3 0 2
2 - 2 j82 = -0.05158(s - 2 / S 2 )
/S, • /S2 - / S 2
2 - /S,3 = -6.3352 x 10"4 (= -yS 2
2 ) (4) 7.TvfA : 3ikJjmttm<a
a , = - - £ h - + - # f - = -0.1176 [ = - a , !
9ao2 3 a 0 " I ~ 9a„ ;
a i = ~ "fer + a ' l & 3 + a s = -008481
( a 2
2 + 4 a , 3 ) 1 X 2 = (7.1929 x 10"3 - 6 5133 X 10~ 3 )" 2
= 0.02607 i£->X. 3 i » C * g i t © f f i © l o ( i « T f f l 1 S t ^ 5 o
- 8 7 -
• 029 9:1 JλEI1I-:'1
水素の高圧50気圧, 400[1¥]における密度
ステップ偏心因子ωを求める。
ケース lと変わらないので省略。
ステップ2 Peng-Robinson-Redlich-Kwong式の定数a(T)及びbを求める
ケース 2
)
l
{
[a(T)]1/2 = 1 + (0.37464 + 1.54226ω-0.26992ωつx(1 -T,1/2)
r. r 400 11/' 1 = 1 + 0.37464 x I 1 - I一一一
l' l 33.2 J
(2)
= 0.07425
a (T) = 5.5124 x 10' 3
R'中 2
川 c)= 0.45724マナ=2.6519 X 105
a(T川(げのT町)=寸吋α削(山.ぺm川(げ侃山T巴刊c)=斗叫5“5即 10一3切刈刈刈X刈川川2.6焔6白5日1削…4削 [ 苦悲去:器詐剖号手引L可] ロ中
b = 0β7780・下ナ=16.559 [CIIV g-moI]
ステップ3: 3次方程式の係数を求める。(3)
72135.9 1.0773 X 109
1461.8 x 49.3462 82.0568' x 4∞2
P一一2
H一T
「zr-一Ra一l
aμ
= 6.6958 x 10' s
= 0.024895 16.559 x 49.3462 82.0568 x 4∞ β 占二E
RT
従って, Peng-Robinson-Redlich-Kwong式を展開した次の 3次方程式
x'ー(1一β,)x' + (β)-3β? -2β,) x一(β3・ムー β22ーβ,')= 0
の各係数は以下の値となる。
1-β, = 0.97511
β)-3β" -2β-0.051団(==-2β,)
β1・β2ーβ22ー β" -6.3352 x 10-' (==ー β,')
ステップ4: 3次方程式を解く。
前ケースと同様に求めると,次のとおりとなる。
(4)
aこr + -T-= -0.1176 r == - a,', 1 日ao2 I 3ao - V..L.l.IV l - 9ao2 J
α_ ~_a)~ + a,. a, 2一一三百7十一3一+a, -0.回481
(a,' +4 an1/' = (7.1929x 10-' -65133X 10-')1/'
= 0.02607 3次方程式の恨の lつは以下の値となる。
-87-
従って.

JAEK1-M 93-029
x : r. [ - g . + t a . ' + ^ . r r , [" - a , + ( a , ' + 4 a , ' r f a, L 2 J [ 2 J 3 a 0
= 0.3813 + 0.3085 + 0.3250 = 1.0149
(5) X f - 7 ^ 5 :®Jg£3cJ66o
w R * T i n u o v 82.0568 x 400 ,,-,. n c V = x p — = 1.0149 x 49.3462 = 6 7 5 - 0 5
# % i r , r f i%Hi^> F7 ' -y?J "Tli, 5.0[MP a ] • 400[K] TcDS&Jgte 2.960X10"
[g/cnf] Tr<fc3o
5 r - X 3 > ; ? > © 5.0 [MP a ] , 600[K] JCfclJSSgJg
(1) X f - ^ 1 : iB'[>H?-a>£#a!>5o 9UP9U.6T,, =111.7[K] , BSfffiKT. =190.55 [K] , E i # E i J P c = 4 5 . 4 5 [ a t m ] ^ ,
ttffi!^¥»£Tb.r3EO:fcRiedel5$©iFb, ac&t fQl i&Cff i t / i . g , , Tb.r = T b / T . = 111.7/190.55 = 0.5862
W„ = -35 + - = ^ - +42£nT b . r - T „ . , 6
1 b . r
= - 3 5 + 61.413 - 22.432 - 0.04058
= 3.940
0.315V b + l n P e _ 1.2411 + 3.817 3.0838
5.8520 a ' 0.0838 V b - £ nT b., 0.3302 + 0.5341
Q = 0.0838 (3.758 - « • ) = -0.17548
A* = -35Q = 6.1418 B" = -36Q = 6.3173 C" = 42Q+ a, = -1.5182 D* = - Q = 0.17548
: W ^ , Mf&ftUBlT, =0.7 f c f c i t 5 W E g ^ l l ^ , P » B . , ( i ^ © i [ t / < j : ^ e
£nPvp., = A* - - 5 - + C " £nTr + D ' T , '
= -2.3208
.-. P.p., = 0.09820
- 8 8 -
93-029
x = r一α,+(a,'+4α,')凶 1 , r- a , +( αl+4aげ/~l2 J' l 2
JAEHI-M
= 0.3813 + 0.3085 + 0.3250
= 1.0149
ステップ5:密度を求める。(5)
R. T • ~..~.. 8.:2.0団8x 400 v x・一一一一=1.0149 x 士 675.0549.3462
M 2.0158 ρ=一一=一一一一 =2.9862x 10寸 [g/cnrJV 675.05 W.V~VW "'v Lo
参考に熱物性ハンドブック j では, 5. 0 [M P a] , 400 [K]での密度は 2.960X 10-3
[g/cofJである。
メタンの 5.0[MP aJ ,切O[KJにおける密度
ステップ偏心因子ωを求める。
標準沸点T.=111. 7[K] • 臨界温度T , = 190. 55 [K] .臨界圧力p,=45. 45[atm]から,
対臨界保準沸点T..,並びにRiedel式のWb.αc及びQは次の値とな';;0
T.., = T./T, 111.7/190.55 = O.坊 位
ケース 3
)
l
(
36 哩rb -35 +干τ了+42.11nTb., -T ... 6
-35 + 61.413 -22.432 -0.04058
げ一則
。』一広
司AV
一円札
+一+口一辺
司晴一引d
rJ-一向毛
υ
-E E-
-EA-AHV
= 3.940
α 一一旦主主主L土旦旦p,, - 0.083811' b - .11 nTb.,一
= 5.8520
Q = 0.0838 (3.758 -a,) = -0.17548
従って. Riedel式の各係数は次のようになる。
A. = -35Q = 6.1418
S-= -36Q = 6.3173
c-= 42Q + a, -1.5182
D+ = -Q = 0.17臼8
これから対臨界温度T,=0.7における対臨界蒸気Pv..,は次の値となる。
inPvp., A+ー辛+C. inT, + D' T,'
= -2.3208
-88-
PvP., = 0.09820
従って,偏心因子ωは次のとおり。

.IAKKI-M 93-029
u> = -logicP.p.. - 1.0 =• 1.007896 - 1.0
i«(7)ffl^4RgT:liaj = 0.011 t ^ ^ - ^ t l T f c ' J . faVXtik™'li X!*&>-= 0.008 i t t - >
(2) ZTyf2 : Peng-Rob!nson-Redlich-Kwongit;ffl^S5ta(T)S:0 :b^*«)50
a ( T ) It, 5t (2.1.19) 0 a ( T ) S t f i t (2.1.20) ffla* (T„) # > £ a ( T ) = a ( T ) • a 'CTc) t L T * * 5 o
[ a ( T ) ] , / ! = 1 + (0.37464 + 1.54226 <u - 0.26992<o2) X (1 - TV 2) = 1 + 0.3868 x (-0.7745) = 0.7004
.-. o(T) - 0.4906
&&, <y = 0.011 £ L £*§£-(:: l i ,
[ a ( T ) ] ' / 2 = 1 +0.3916 x (-0.7745) = 0.6967
.-. a (T) = 0.4854
kteO. (o = 0. 007896 kLtz&ttz-,tz 1.1 [96] L # ^ f c £ # l \ ,
a . ( T c ) , 0.45724 * ^ = 0.45724 8 2- 0 5 6 8 ! X 1 9 0- 5 5 2
P c « • — 4 545 = 2.4596 x 10 6
.-. a ( T ) -= a ( T ) . a * ( T c ) = 1.2067 X 106
-•Jj. b l i & © f & i # 3 o
b = 0.07780 R p J c = 26.7651
(3) X f , 7 ' 3 : 3&#gi$;©#IS[£:£a6-5 0
a ( T ) « P = 1.2067 x 106 x 49.3462 R 2 T 2 82.0568 X 6002
= 0.0245652
E * P = 5.0 [MP.] = 1 .o 1 325% X l 1 0° 6 [ [ p P a/at m ] = 4 9 " 3 4 6 2 [ a t m ]
b • P 26.7651 x 49.3462 RT 82.0568 X 600
= 0.0268260
6. tgOte. Bgf058^1/i.
- 8 9 -
.J:¥EHI-¥1 9:1-029
ω=一logIOP,p" - 1.0 1.∞7896 -1.0
文献(7)の第 4版ではω=0.011と与えられており,他の文献(付-!}ではωτu.008となっ
ている。
(2) ステップ2 Peng-Robi nson-Redl i ch-Kwong式の定数a(T)及びbを求める。
a (T)は,式 (2.1.19)のα (T)及び式 (2.1.20)のa・CTc)から a(T)=α(T)
a ・CTc)として求まる。
[a(T)]'/' = 1 + (0.37464 + 1.54226ω 一0.26992ω')x ( 1 -T ,1/')
1 + 0.3868 x (-0.7745)
= 0.7004
a(T)士 0.4906
なお.ω=0.011とした場合には,
[α(T)]I/' = 1 + 0.3916 x Cー 0.7745)= 0.6967
a (T) = 0.4854
となり.ω=0.007896とした値とたった1.1 [%]じか異ならない。
R'中 82.0568'x 190.55' a・(T.)τ0.45724マテ=0.45724 V~.VVVV • ,
= 2.4596 x 10"
a (T) .=α(T)・a*(T.) 1.2067 x 10"
一方. bは次の値となる。
ロ・中b = 川7807f=お 7651
(3) ステップ 3: 3次方程式の係数を求める。
βa (T)・P2ω7x 10" x 49.3462 I - -1f'干「一一 82.0568 x 600'
= 0.0245652
5.0 x 10" [Pa] 圧力 P= 5.0 [MPa] • ^.^';.;~v .:' ::. rL~_aJ/_.__ , 49.34昭 [atm]
1.01325 x 10' [Pa/ at
β 一主工旦 2:6.7651x 49.3462 -~ - 82.0568 x 600
= 0.02回260
(付 1 )斎藤統計熱力学による平衡物性推算の基礎J.ケミカルエンジニアリングシリーズ
6.培風館.昭和58年 1月.
-89-

JAEKI-M 93 029
V = x R T P t L T , x(±«fc©3<$CfriIjt©l»-e.&-5o
x 3 - ( I - ^ ) x ' + ( £ , -3 jS« 2 -2 /8 , )x- ( jS ,« et-0t*-0f) = 0
«-^ati^©etn»:5o 1 - 02 = 0.973174 j8, - 3 / 9 2
2 - 2 / S , = -0.031246 0,» jS, - £, 2 - /9, 3 = -7.9953X10 s
(4) Xf 7 -/J : 3^^gst -)!¥<o Cffl t-xm a, = -0.115645. a 2 = - 0 . 0 7 8 3 2 7 ^
a,1 + 4 a,' = 6.13514 x 10 s - 6.18643 x 10 ' < 0
t « 5 . ft^T. f«2y-X©J;?CLTf f i£-3c* .5Ci^-C#t t l \ , * § f H f » ® S S L*IB l<Tft¥< t . 3^^eitOffi f i3otfe*ff iT<Jcc?)t*.- l ; t^So
x, = 1.00421 x, = 0.002382 x, = -0.03342
mz. a2
2 + 4ai
3 = 0tLXx&$.tbZ tft.(?)3:0l~teZo
r -az+(az2+4a^y j ' , f ~ a: - (a» '+4a, ' ) ' ' ' f ' a, x = [ 2 J + [ 2 J - ~ 3 -
_ I" (-0.078327) f 3
9 _ (-0.97317) x ~[ 2 J - 3
= 1.00358
(5) X f - ^ 5 : &m. p € • * * 9 .
V = x • -OT = l m 2 l . 82.0^600 = 1 ( W 1 9 3
„ _ M _ 16.043 n f t 1 c f t 1 o r /_JT P - "v" = 1 0 0 1 9 1 = 0.016012 [g/cnf]
r&M±^> K7*-y ? j T « . 0.01593tg/cnf] i i j - ^ t t T f c O . -t©^(it>r^0.515196] T*So
- 9 0 -
JAEIiI-:1.1 93 -029
β1 ;;:βzとなり,水素の場合併J<<ん}と異なる。
Vニ xRT Pとして. xは次の 3lX方程式の解である。
x'ー(1一β,)x' + (β,-3β:'-2βz) xー(β,・ βεーβJーβ.')= 0
各係敷は次の値となる。
1 -βz = 0.973174
β1ー3βz'-2βz = -0.031246
β2・β2一β22ー β,. -7.9953 x 10-'
(4) ステップ4: 3次方程式を解く。
このケースでは.α1=-0.115645.αz=← 0.078327から
ai + 4 a,' = 6.13514 x 10 • -6.18臼3x 10' < 0
となる。従って,前2ケースのようにして般を求めることかできなL、。大型計算機のSSLを用
いて解くと. 3次方程式の板は3っとも実恨で次のとおりとなる。
x, 1.00421
x, o.∞2382
x, -0.03342
仮tこ.a/+4aI3=0としてxを求めると次のようになる。
r -a,+(a,'+4a,')''1 ,r-a, -(a':+4a,')'-, 1 x =1 2 1 T l 2
a, 3
3
,
z
守
asaaEJ
、J
一
守
4-
qL-
qa一
00一
町一2
・-nu一
(-
rE
・E
・-tx
X2-.i二0.97型7)旬 3
= 1.003鵠
(5) ステップ 5:密度ρを求める。
第2.1.2節に述べたように.最大正値x,が解となる。従って.モJL体稜V並びに密度ρは次
の値となる。
v x' ~T = L00421. J!2.0568 x 6∞ -・--n- L00421・=1001.93 p 49.3462
M 16.043 ρv 而王草子=0.01印 12[g/CDf]
f熱物性ハンドブック jでは.0.01593[g/col]と与えられており.その差はわずか0.515[%]
である。
-90-

.JAKK1 M 93 029
'r-Xj *?><£> 5.0 [ M P a ] , 600IKJ ' C f c l ; r a £ f c » g
i t (2.4.33) JCT=600[K] £ f t A U A* Ci#Cffltt££© 0
A*[W/(m«K)3 = -1.869 x 10 s + 8.727 x 10 5 x 600 +1.179 x 10 T x 600' - 3.614 x 10" x 600s
= -1.869 x 10 s + 5.236 x 10 ' + 4.244 x 10 * -7.806 x 10 ' = 8.513X10 '
T P R C 7 : - J ' i / ' ; - > C - C l i 0 . 0 8 5 8 LW tm • K) ] £ 4 x . £ t r t 4 s 0 . ^ © g l i t r ^ 0.78l!°o] T & o o (2) 7. f -."/ 2 : ^ E t O i f c « $ A £*#>-5<,
V - X 3 J » > £ . I£tl 5.0 [ M P a ] , jgJ*600[K] ICfctfS*fffi^&Kp, l if t tDflift-So
p , = p / p , = 0.016012/0.162 = 0.09884
ee^r. *fe#$(0»aj^ii^ (2.4.29) £HH>30 c©s:4>©r©«[JiWTt4-*;. r = TV-'M'-VP.^
= (190.55)"' x (16.043)"V(45.45)2'3 = 2.3988 x 4.0054/12.7357
= 0.7544
z , =0.288 frh. » f c a i ^ A l i * f f l J ; - 5 t r * i § o
( A - A*) • C • Z//418.4 = 14.0 x 10 " [exp (0.535/>,) - 1 ] = 14.0 x 10-' [exp (0.535 x 0.09884) - 1 ] = 14.0 x 10 " (1.0543- 1 ) = 0.760 x 10 *
• jt - 0-760 x 10" x 418.4 , x .
= °" iVT&M1 x 0 .288 ' 1 8 ' 4 + 8 5 1 3 X 1 0 2 = 2 1 2 8 X 1 0 ' ' + 8 5 1 3 x 1 0 ' = 8.726X10 - ' [ W / G n - K ) ]
H ^ C Vargaftik©ffi!e-C{iffi*50[bar] . 300['C]O573.15 [K] )C*>OT8.21x lO* [W, (m • K ) ] t % i t t ) * l T l ' 5 o £?- . 1 [bar] . 300["C] TJifi .OlxlO'IW/On • K)J
£*?•«. "itTCfcO. 300[°C] ICfc!t550[bar] t Hbar] i r O M A - A' ) I i 0 . 2 x l 0 * [ W / ( m - K ) ] t ' « £ 0 . ± a > © « t t « ( 3 [ ^ L ; r * « 0
- 9 1 -
.f.¥EHI ¥1 9:1" 029
ケース4 メタ〉の 5.0[MP a J. 600[1¥]における熱伝導率
(11 ステププ常庄での熱伝導率λ・を求める。
式(乙 4.33)にT=600[1¥.]を代入し.λ・は次の値となる。
.lO[W/(moK)] = -1加9x 10"' + 8.花7X 10-5 X側
+1.179 x 10宮 X6仰・ -3.614 X 10-11 X創)0'
-1.869 x 10 • + 5.236 x 10-' + 4.244 x 10 •
-7.剖6x 10"' = 8.513 x 10"'
TPRCヂータシリーズではO.0858 l W . (m . 1¥.) ]と与えられており.その差はわずか
0.781 [00] である。
(2) ステッブ2:高圧での熱伝導率Aを求める。
ケース 3から.圧力 5.0[MPa).温度600[1¥)における対臨界密度ρEは次の値となる。
ρρ/ρε= 0.016012/0.162 = 0.09884
従 η て,熱伝導率の算出には式(2.4.29)を用いる。この式中のCの値は以下となり.
r = Tc"6M'/'/P1"
= 090.55)凶 x(16.倒3)凶 /(45必 )2/3 = 2.3槌8x4.∞>54/12.7357 = 0.7544
z < =0.288から,熱伝導率λは次のように求まる。
(λ 一λつo {"・ z//418.4 = 14.0 x 10・[exp(0.535ρ ,)ー 1]
= 14.0 x 10"・[exp(0.535 x O.凹部4)-1 ]
= 14.0 x 10・0.0日3-J)
0.71印 x10 •
il = 0.760 X 108 X 418.4 +、."0 z.' ・H
0.71印 xlO・ x418.4 ~";;;'';A'A.: 1¥ .,005 + 8.513 x 10 z 2.128 x 10 3 + 8.513 x 10 z : 0.2路一
= 8.726 x 10' [W/(m 0 K)]
因みに. Vargaftikの便覧では圧力50[bar].300["C1C=573.15 [K])において8.21x 10-'
[W, (m' K)Jと与えられている。また. 1 [bar 1 • 300[.C]では8.01x W[W/(rn • K)J
と与えられており.300[.C]における50[barlと1[bar]との差(,l-AりはO.2XlO-2 (W/
(rn・IOJとなり.上述の値とほぼ同じである。
-91-

JAEKI-M 93-029
f-t»2 fefUfiKSC^S*
* * ! * . B*fiK*"-3S.2 [K] . B»ffi**«l-S2 IMP a] "CAU. H T T R W M W H l * ® *
- 9 2 -
.JAEHI -~I 93 -029
付録2 飽和温度及び圧力
一酸化炭素.二酸化炭素及びメタンの飽和温度と飽和圧力の関係を付図2・1に示す。なお.
水素は,臨界温度が33.2[K] .臨界圧力が1.32[MP a]であり. HTTR水蒸気改質器の使
限条件では気相にある。
-92-

JAKK1 M itt tK29
300
Gas Phase
f ^
Carbon Dioxide
Liquid Phase
200
Gas Phase 4 «*3
1 Liquid Phase
1 0 0 -
Critical Point
Methane
Critical Point
Carbon Monoxide
_L 1 2 3 4
Pressure P [MPa]
f+02.1 -m<tmn. ~aitmm&.v*?>a>tkm&mti£j]a
- 9 3 -
.f九五1¥1 ¥1 ~I:I O~9
300
〔〉ニCriticol Point
Gos Phose
Lilt』idPh脱
200
トー
ω』コ
』
ロ
』
ωaEω
↑Criticol Point
Monoxide
Gos Phose ~
i~ o
Liquid Phose 100
5 4
(MPo) 3
P
2
Pressure
一酸化炭素.二酸化炭素及びメタンの飽和温度と圧力。
-93-
11図乙 1

JAEKI-M 93-029
1. *x.A*§
* « £ » K f c l ' T a ^ m * * ® © « t t * S « - r 5 ± T J t e © + ^ 4 : L f c i i ^ « * « . fT PR
SIEBB*<HTTR*StiaSii©«fflfiR*#«-*'<-L-Cl»<£l»»^*<y<C^t.f*ofc 0
«« l tS i t©^St4 l? f f l ^ i iLT . cnST-&®m«tt*«JJit-C4-^ofclHVS© Vargaftik ©ffiJSli. J£tAt'©®S»Col,»T)i;i»fiffi-EA(Effllc*5fc-,-ca^tt*^SftTl'5CtA*
* w T . c c t l t VargaftikfflffiH^^Se*fflit^iLT. 8%!t*JttDSaf£61Tff U #£TfflJti£fFffl*£3l£fiiJE-fSo «4s. Vargaftik® <££(*. * ^ t t « - 4 x r i » 5 f i S © * f i t<9Uk [°C] Tfe5fc«>. *rA\?>BX. [K] *f f f f l tT l»*l f iO«««l l t©t t l»Mi*<*L i-o C©!ta6. : : m S^J tg iU; : <k § « £ * ¥ ( : : t * j . Ctifc Vargaftik®fiE^©££
^ - t j > h » g = y ' d - " y " t - xlOO ( f t - i l ) >*est.
: : T , y . . , . : iMt t t t«7©S%«
* £ T i * . y „ , . ( 4 & 2 & i £ g £ i O . y . s . . (c(i]l^filSst!cS0^((fi©^^16*©i[t,tor
2. it«I¥fl&*S3l
*£-c©h:8fcff©*§£, *^»S^;©m«1±i¥«^+i}-r'f^ofc«Jc©4-3Jc^)i«T. VargaftikOflHEifcJfctt-rSo
*XT'ffl«lf*(C*>l»r«. JtRfiffilBEH** 600 [K] J«Tt iaf i©*t*)^fco -tttt««:**fc-WfcK*
**{C-?l'-C(i. E*S)im©it«iSKIEffl*< 600 [K] «T©fif i©^T'*ofco ~fi*ffc/*j t i : - 5 f t « , S E « T © * * S ^ e © S t ' i - o T l ' 5 G A l / * - h ^ S < . HH&aMgl^
it5ff.ffllt '©»**^*©*tnCoTl'5GAU.-tJ- h*<£<. HKft7i<fS^tfil«!^*xfco m%mW3.k Vargaftik©ffiK^©a^*t©it««S**#@3.1*Ma.-'[email protected]*-ro Ctl £ffl@tf>£, Vargaftik©ffiKS^*^fiMf^ffl^JSttJcoi»rjJtfflCt*H^.J;-5„ (1) VargaftikOflEJStt. 1ifSt!fejJ<i5t'fl&0jS£tffl£Kgffiffl<'*—fr > YWMXh*), *<D
- 9 4 -
J .-¥Elil -;¥1 93 -029
付録3 ワルガフチックの便覧を中心とした.選定推算式と推定値との比較評価
1. まえカ、き
本報告書において選定綾算式の信頼性を評価する上で比較の中心とした選定値集は. fTPR
CデータシリーズJと『熱物性ハンドブック j であ司た。しかし.本文での検討から明らかにさ
れたとおり.選定値集といえども信頒性の低いケースがある。また.選定値か与えられている温
度範囲かHTTR水蒸気改質器の使用温度条件をカバーしていない場合が少なからずあ司た。
選定推算式の信頼性評価を通して.これまでその信頼性が明確でなかったi日ソ速の Vargaflik
の便覧li.ほとんどの物質について広い温度・圧力範囲にわたって選定値が示されていることが
わか--.1.こ。
そこで.ここでは. Vargaftikの便覧を選定値集の基準として.選定推算式の信頼性を評価し,
本文での比較評価結果を補足する。なお. Vargaft ikの便覧は.選定値を与えている温度の単位
か狽氏 [.c]であるため,ケルビン温度 [KJを採用している他の選定値集との比較評価が難し
l '0 このため.ここでは,選定推算式による値を基準にとり.これと Vargaftikの便覧等の選定
値と比較することとする。即ち,付録3では.パーセント誤差を次式で定義する。
y ー -yfーセント誤差一一一ーヱ!:...xl∞ -・(付-3. 1 )
.Yf'Sl
ここで Yst' L 熱物性優yの選定値
y @st.熱物性値yの選定推算式による値
本文でli. Y...は基準選定値をとり Y....,こは選定推算式に加え他の選定値集の値もと勺て
t 、るので注意か必要である。
2. 比較評価結果
本文での比較検討の結果,選定推算式の信頼性評価が十分でなか司た次の 4つについて.
Vargaftikの便覧等と比較する。
一密 度:メタン
本文での検討においては,比較温度範囲が 600[1¥]以下と低温のみであった。
一粘性係数:水素と二酸化炭素
水素については,圧力効果の比較温度範囲が 600[K]以下の低温のみであった。二酸化炭
素については.高圧倒での基準選定値の基となっているGAレポートが古く.信願性が低い
と推測された。
一熱伝導率:二酸化炭素
高圧倒での基準選定値の基とな司ているGAレポートが古<.信頼性:リ、低いと推測された。
選定推算式と Vargaftikの便覧等の選定値との比較絵果を付図3.1から守図3.4に示す。これ
らの図から. Vargaftikの便覧及び選定推算式の信頼性について次のことカ、いえよう。
(1l Vargaf t ikの便覧は.信頼性が高い他の選定値集と同程度のパーセント誤差であり,その
-94-

•IAKKI M M 029
[° 0] « T . 1200-1300 [K] <OM&Xb\0 [%] t lToQK-C^^TfcO, +##1Sigte
L A - U A A ^ , VargaftikfflfEK-rii. -S?{fcK*©lfte#¥^«ET:ffli[L75^$*vTJs
- 9 5 -
.1礼ト:1¥1 ~I 9:1 O:!9
温度.圧力に関する傾向も大きく異な「てはL、ないので.十分な信較性を有している。
12) メタシの密度並びに二酸化炭素の粘性係強について. 600 [K]以上の高温におけるパー
セント誤差の猛度,圧力に関する傾向は.低温側からの延長上にあり,選定推算弐の翁I.lI立
十分良い。
(3) 二機化炭素の枯位係数及び熱伝導率の選定雄算式は. Vargaflikの便覧の選定値と鍍ね5
[ 00 ]以下. 1200-1300 [)¥]の高温でも¥0[ooJ以下の精度で合っており,十分な信頼性
を有している。
しかしながら Varg畠ftikの便覧では.一酸化炭素の熱伝導率か常圧での値しか示されてお
らず.誤値も少なからずある。さらには.温度の単位が摂氏であるため.ケルビンで与えてい
る他の選定値集との比較が難しいという欠点がある。これらの理由から.本文では基準選定値
にnlUしなか司た。
-95-

JAEKI-M 93-029
+ 1
? -1
-3 200
#03. 1
Pressure = 0.11 MPo!
(MPoI
[MPol
Density
Methane
Estimated by
Varaaftift Handbook Varaaftift Handbook
JSTPt Handbook
400 600 800 tOOO t200
Temperature T IKJ
+10
i + 5
o a. a> Q
Hydrogen Viscosity
-51— 200
Pressure = 0.1 [MPol
Estimated by
Vartotf i f t Hwdboot Vartotf i f t Hwdboot TPHC Dtti Strict JSTfs Handboot
400 600 800 1000 Temperature T IK)
1200
# 0 3 . 2 **K-3i»TttttttR©»£ttWi$j«.... tglZVin,,, Ottttffflo
- 9 6 -
,1:¥EHI-:¥1 93 -O:!9
+1
Pres鈎re= 0.1 I MPo ) 話宅
〆グコ1.0[ 附
o
Esli冊。ledb, t一一一一!拘rg・fIIk¥凶酷似測量
'一一一lお前陶働暗
-2
岬曲目見¥(』叫白色『一世師、
mw』コ↑』
oa山口
-3 200 12,α〉1000 8∞
T 600
Temperoture 400
[ KJ
メタンについて密度の選定推算式P~stーと選定値ρ ‘. I の比較評価。付図3.1
白IIMI・db, 一一一 IYarta1'帥帥輔崎
一一打開抽S1ries-.-IJST内崎l1li111帥
+10
窃
;【 +5、、、
-." .... 司.
‘' ."
司‘
o 出
』
三
』
oam相口
{
、宅》
1200 1000 800
T
政治
Temperoture 4∞
-5 200
l K)
水素について粘性係数の選定推算式μ." と選定値μ,.I の比較評価。
-96-
付図3.2

JAKK1 - M S*3 029
+10 Estimated by
Vorialtls's Hadknk Vorialtls's Hadknk
TPSC M o Series
jJSTPs Itwdboot
200 400 600 800 1000 Temperature T [K]
1200
f*H& 3 zmit8ixtzr>[.*xim&iiL<Dm%.mmzit.... tmmmu.,1. ©ittxiffto
f:+2o
ts
Corbon Dioxide
Thermol Conductivity |
X Estimated by
Vargaftlt's Handbook Vargaftlt's Handbook
TPRC Oata Series JSTPs HoMlboak
400 600 800 1000 Temperature T [K]
1200
tfH3. 4 Z l » f t » * « w O l > r « i e # * f f l « ^ * * S C A . . , . t « S « [ A . . , . ©ffctxfftto
• 9 7 -
EslilHltd bJ
一ー一Iva咽・fllk',H圃・曲
一一ー!~抽加国
一一一:JSTPも畑働融
029 !J:l .J:¥EHI. :¥[
-s-au-
岨一一uz
Ei
Dでω
nでEM--
『一
v
nu
一
PL
一
Pressure = 0.1 [M Po 1
+10
,、話、
三+5、、、
1;; ・9:::l..
.. ゐ。司.
mw』コ七oa山口
t200
4.0 [MPol
1α)0 8∞ T
t.5Tc
600
Temperofure
4∞ -5 2∞
[ Kl
二費量化炭素について粘性係数の選定推算式μ."と選定値μ..1の比較評価。付図3.3
、、、、、、、、、、、、、、¥
¥ ¥ 、
¥ 、
ーーーーーー』--ー~ー
Pressure = 0.' [MPo ]
fcorbon Dioxide
lrherm日ICon伽凶vityI 、。三 +20
可苫
‘s ..-< 、、、
言+10CI>
..-<
・3ωn ..-<
O Q,)
:::;)
E Q,)
cコー10
12∞ 1∞o 8∞ T
6∞ Temperoture
400 2∞ IKl
二酸化炭素について熱伝導率のき定推算式λ."と選定値A,. I の比較評価。
-97-
付図3.4

JAEK1- M 93-029
itIBlJfcfi. *fcS#g^£5£l lJ fc&C.£;£&«:&C.**». c©i fcC, /C , i :Uf f5f f l*«-
•rztzircti < »*££&*» < <cs.
*££• f-tl4. l d ^ - r i - J I C HTTR*jgmaSS©ffiffl*tH*J-C*nii'ft2 [°o] « T © +
_ Cp.mp] _ C p
* _ C p . m o l - R - Cp-R/M ( f * 4 - 1 }
: : t , C P . . „ , : *A£EJti!fc [ J . g - m o 1 • K] CP :£EEJt& [ J / g - K ] M : # ? ! [ J g - m o 1] R =8.31433[ J / g - m o l • K] : -&ttf*/£&
r»is«=fci<r. S (ft-4. i) icfv;A-r«Cp omRu-itmitcDmfemt tmm."> vf-y
-98-
.JAEHl 九I93-029
付録4 比較比Kの縫算について
プロセスガスを内包する配管や伝熱管の破断事故に対する安全解析.熱過度解析においては,
臨界流を取級う場合があり.熱物性値として本文中で検討した 4つの他に比熱比κが必要になる。
比熱比は.状態方程式から定圧比熱c.と定容比熱c.を求め.この比c./c曹として得るのが一
般的である。しかし. c.に加えてc.を状態方程式から別個に求めることは.計算時間を膨大に
するだけでなく推算誤差も大きくなる。
そこで.次式で簡単に表わす理想気体に対する比熱比推算式の実在気体への適用性を検討した
結果.付表4.1に示すように. HTTR水蒸気改質器の使用条件内であれば約2[OD]以下の十
分な楕度で推算できることが明らかにな司た。
κーじ'p.mol Cp 一一Cp.mol -R Cp -R/M
ここで CP. .01 モ J~定圧比熱 [J/'g-mo 1・1¥]
c. 定圧比熱 [J/ g ・K]
M 分子量 [J,"g-moIJ
R=8.31433[J/g-mo l' Kl:一般気体定数
……(付-4. I )
同表において.式(付-4. 1 )に代入するc.の値及び比熱比の選定値は「熱物性ハンドブッ
クj 与えられている値を用いた。
-98-

.I.XK
hl M
VU
(fj
8 ft Q
«M
o 1
•
O o 1
CM 1
- 0. 57 -0.88 - 0.57 1 - 0. 33 ! CO
m 1 CD 1
o CM 1
cr CD
CM CD-
S ft! S if
•^
CO CO
CO CO
o CO CO o 00
CM CO
CO CO
CO o CM
CO CO
CO r-CM
r— CO CO
CO CO CO
33
Q m
CD L.O CO
OS CO
CM CO CO
CO CM
an CM CO
U3 CO
CO o CO
CM Csl
CO CO
CO CO
CO
2 •R co
LT3 CM o
o O
o to o
o o
o IT) o
o
51
IT)
CO CM
O o CO
O o o -3-
CD o o CO
CO t— CM
CD o o
CO CM
o o o CO
O o o in
o o CD o
CO CM
o o o o
*
m AJ
A « *£
-£
-D
<
•99-<D にD
流 体 温
水 素
一徴化炭素
二散化炭素
メ タ 、J
* 蒸 気
ヘリウム
付表~. 1 比熱比推算法の評価
度[Kl 圧力 [MP a 1 比熱比の俄算値 比熱i七の選定1直
273.15 0.1 1. 410 1. 410
600.0 5. 0 1.395 1. 396
400.0 0.2 1. 395 1.398
1000.0 5.0 1.332 1. 340
273.15 0.1 1. 296 1.308
1100.0 5. 0 1.175 1.182
273.15 0.1 1. 312 1. 316
600.0 5.0 1.185 1.203
500.0 0.1 1.303 1. 313
1000.0 5.0 1. 242 1.273
273.15 0.1 1.667 1.667
1000.0 5.0 1.667 1.663 」
lト tjf~~V~ [01) 1
0.0
-O. 09
-O. 24
-O. 57
-0.88
-O. 57
-O. 33
一1.53
-O. 7,1
-2. 40
0.0
0.24
戸'
・τ・
ヤ'
一., -w
占
h
v

mm&% (si) tmm m i simtmaaxifmsuma.
m K ft ffi «?
tk S / - (• rt- m
n m * • 7' 7 i kg IS Bl » s
* at T y t r A mtjf&m f «r YZ V K ft H It * ; t mol it 8 *T V 7"* 7 cd
•P as ft 7 •/ T y r&d a <* ft x-7-7 ^ 7 y sr
» 2 SIi»f83*l5*{t
S 3 g ) 6 f f l £ f * £ t > o S ! H 5 ! : ! » > e
• 8 * £ % ffe»si»(a
a * a. 'x JU -y Hz s ' A - i - h y N m-kg/s'
i£ n . & n >< 7. ii >\- Pa N / m 1
x*;u*-. ft*. « • 's =. - l\> J N-m
c * . » « * •7 -/ V W J / s * a It . « «r 9 — a y c A-s «(*. sgft. KfE^ *' *• Y V W/A
s» 3 s a 7 7 7 K F C/V
* a « is * - i- n V/A =i s 9 9 9 * 7. s - f s 7. s A/V
m * • » * - ' < Wb V - s « * ffi HE T *• 7 T Wb/m 2
-r y y ? 5> y x ^ y M - H Wb/A -<; <!< v* 9 X & 8 •bins') x& °C )t * IV - / S lm cd-sr .(ft BE IV 9 7 lx Im/m 2
ft « ffi *< 9 u >v Bq s"'
« « 8 • f \s 4 Oy J /kg
a 8 is a >> — ~Oi- h Sv J /kg
g ft id <t » . RJ. B C . 9s. » 'J v h * h y
min. h. d
1. L t
3 -f # * h eV u
IeV=l.60218xlO-'M I u=I.66054xl<r"kg
* 4 S l iJ t icBSWK
?, ft ie % * y ? ' x ho-- i . A
"' - V b y < — IV bar
*' IV Gal * ^ ') - Ci \s 's t- Y 'S R 7 V rad u L. rem
1 A=0.1nm=10-"'m lb=100fm'=10- ! ,m !
lbar=0.1MPa=10sPa 1 Gal= 1 cm/s* = 10- m/s-" lCi=3.7xl0'"Bq lR=2.58xlO'C/kg lrad = lcGy=10 !Gy lrem=lcSv=10 :Sv
S S S I * * S
(Stt K i K S a ^ 10" X 9 * E 10" •*4 9 p 10" T - 7 T 10' * It G 10« y ti M 10' * a k 10' * v 9 h h 10' T * da
i o - X •s d 10"' * •s f c 10"' £ ') m 1 0 - -7-1 9a it i o - + J n 1 0 " f 3 P i o - : 1 7 Z.L. h r
KT" r h a
1. & 1 - 5 l i rHIS»&JfcJ » 5 S . BIB nCSKEg 1985Jffllfflci5 0 fcfc'L. leV fcj: tf 1 ufflBli CODATA ffl 1986 if HIS ttlCfc,fc,,
a « 4 I C ( i « S . / v b. T-'U. -v?>
3. barli. J]ST-im»<DiEt}£&t>-f)$,
? . 4. EClHWSVStfrftTlibar. barntsi
a rfflHErollGtJ mmHg?>iS2ffl*T=i^
tl N( = 10'dyn)
9.60665
4.44822
kgf
0.101972
1
0.453592
Ibf
0.224809
2.20462
1
tt HE lPa-s(N-s/mO=10P(*TX)(g/(cm-s))
mm Im7s=10 , St (x t - -7x ) ( cmVs)
rE MPa!=10bar) kgf/cm' atm mmHg(Torr) lbf/in'(psi>
1 10.1972 9.86923 7.50O62 x 10' 145.038
ft 0.09806F5 1 0.967841 735.659 14.2233
0.1013=5 1.03323 1 760 14.6959
1.33322 x 10"' 1.35951 x 1 0 - 1.31579x10-' 1 1.93368 x 10"'
6.89476 x 10"' 7.03070 x 1 0 - 6.80460 xlO" 3 51.7149 1
X J(=10'erg) kgf'm k W - h c a l G H t i £ ) Btu ft • Ibf eV
+' 1
1 0.101972 2.77778x10"' 0.238889 9.47813 x 1 0 - 0.737562 6.24150x10"' +' 1 9.80665 1 2.72407 x 1 0 - 2.34270 9.29487 x 10-' 7.23301 6.12082x10"
% 3.6 x 10' 3.67098x10' 1 8.59999 x 10' 3412.13 2.65522 x !0" 2.24694 x 10" % 4.18605 0.426858 1.16279 x 1 0 - 1 3.96759x10"' 3.08747 2.61272x10"
« 1055.06 107.586 2.93072 x 1 0 - 252.042 1 778.172 6.58515 x 10"
1.35582 0.138255 3.76616 x 10"' 0.323890 1.28506 x 10-' 1 8.46233x10"
1.60218 x 10"" 1.63377x10-'° 4.45050x10"" 3.82743x10-'° 1.51857x10"" 1.18171x10-" 1
lcal = 4.18605J(itWffi)
= 4.184J mil?)
= 4.1855 J (15-C)
= 4.1868J(gR5*a*>
f t 'W lPSUUfift)
= 75 kgf-m/s
= 735.499 W
Bq
1
3.7 x 10"
Ci
2.70270x10-"
1
Gy
1
0.01
rad
100 1
C/kg
2.58 x 10-
3876
1
S»
1
0.01
100 1
(86?12fl26BSffi)
国際単位系 (81)と換算表
ma 篠頭経 記号
101!I エクザ E
10・‘ '‘E タ P
10・2 テ ラ T
10・ ギ ガ G
10・ J1 ガ M
10' キ ロ k
10' へテト h
10・ デ カ da
¥0-' ア シ d
¥0-' セ Y チ ε
tiI-' 、. リ m ¥0・ マイヲロ /1
10-' ナ ノ n 10-1% ピ コ p
¥0-" 7~ ムト,
10--・ 7 ト •
51鰻重量語.5 .2 51と併用される噂位
leV=I.邸1218x10-"J
1 u=1脱却54x¥o-"kg
名 倖 l記号
分.時. Blmin. h. d JI:・分.秒 l ¥・リ フ ト , レ 11.L
ト ン Il
電子ボルト IeV 隠;;i.f質・暇位 1u
.' SI;底本単位および緬助単位
記号
m
kg
s
A
K mol
cd
r~d
sr
置 |跡
長 さメートル
質 量キログラム
時間|抄
電 流 J7 ンベ 7
'"力学温度 iケルビン
物 質鑑 lモ ル
定 度 lカンデラ
."面角 lラジアン
主体 角 lステラジ 7 ン
f注】
1 表 1-5は『同際単位系』第S庖.同際
度量衡局 1弼5年刊行による。ただし.leV
および 1uの値はα)DATAの1鎖国B年提実
値11:よ,た。
2. &41Cは海軍.ノヲ~. 7ール.ヘクタ
ールも含まれているが日常の峨位なのでζ
ζでは3・3Lた。
3. OOr l:l. JISでは涜体の圧力を表わす崎
合に限り&2のカテゴリーに分領されてい
る。
4. EC閣僚煙事会街令では bar.barnおよ
び『血圧の憎位JmmHgを&2のカテゴリ
ーに入れている。
表4 SIと共IC雷定的『と
縫録される単位
名 τ「τ号
オングストローム A
"1 b パー,レ OOr
ガル GBI
キュリー Ci
レ ン ト ゲ "1 R ラド rsd
レJ..I rem
1 A= 0.1 nm=10-"m
1 b=1∞fm1= 10-2• m!
1 OOr=O.1 MPa=IO'Pa
1 Gal= 1 cm/s' = 10-' m/s'
1 Ci=3.7x IO"Bq
1 R=2鴎 xlO.'C/kg
1 rad=lcGy=lo-'Gy 1四皿=1 cSv= 10 'Sv
値 名綜 記号 他にのよSるI表単位現
周 担宣 政 へ Jレツ Hz s'
力 ニュートン N m.kg/s'
If 力. 応力 パスカ Jレ Pa N/mz
エヰルギー.仕事.'"・ ジュ-," J N.m
E率 .敏射来ワ ツ ト w .Jls
電気鑑.屯荷 クーロン C A.s
電111..電圧.起電力 ポル ト v W/A
D 電容量ファラド F C/V Q V/A
コンゲクタンス ジーメンス s A/V
信 来ウェーパ Wb V.s
磁 東密度 テ ス ヲ T Wb/m'
インダクタンス へンリー H Wb/A
セルシ ウス温度 セルシウス度 ℃
;1: 来 』レ ー メ ン 1m cd.sr 臨, 度 ,レ ク ス Ix 1m/m'
紋 身J 能 ベクレル Bq 5-'
吸 収線 量 グ レ イト|E Gy J/kg
線 櫨 苛 母 シーベル Sν J/kg
同省の名体をもっ51組立単位表 3
&
正 MPa:= 10 OOr) kgf/cm' atm mm可g(Torr) Ibf/in'(psil
10.1972 9.86923 7.5肌162x 1日a 145.038
力 1 0.967841 735.559 14.2お3
0.1013<5 1.03323 1 7印 14.6959
1.33322 x ¥0-' 1.35951 x 10→ 1.31579 x 10・z 1.9:却問 x10・2
6.89416 x /0・, 17.03070 x 10.' 16.80460 x /0.' 51.7149
n. 換
力
1 cs1 = 4. 18605 J (討蹴法】
= 4.I84J (豊島化学】
= 4.I855J 05 'C)
=4.1邸8J(国際蒸気表》
仕事率 1問(仏馬均}
= 75 kgf.m/s
= 735.4鈎 W
エ J( =10' erg) kgr'm kW・h 国I(Jt量法} Btu れ・ Ibr eV ネ,レ 0.101972 2.77778 x 10"' 凪23881抱 9.47813 x 10-' 0.737鎚2 6.241釦 x10" ギ
9.80665 2.72407)( 10・ 2.34270 9.29487)( 10.' 7.23301 6.12(82)( 10" . 仕事 3.6x 10' 3.67098 x 10' 1 8.59侠淘 x10' 3412.13 2.65522 x!O・ 2.24694 x 10"
. 4.18605 0.426858 1.16279 x 10・ 1 3.96759 x 10-' 3.08747 2.61272 x 10"
処置1055.06 107路6 2.93072 x 10-' 252.042 778.172 6.犯515x 10"
1.35582 0.138255 3.7郎16x¥O-' 0.323890 1.28506)( 10寸 8.462:招X 101•
1.60218 x 10・8・ 1.63377 x 10." 4.45050 x 10-" 3.82743x 10-" 1.51857x 10寸 E 1.18171 x 10・B・
{白E年 12月26日現在〕
繍量当竃
R-一副
E
照射線量
則一
ml
吸収線量
政
射
能





![japan press conference jp KH.pptx[読み取り専用]...2017/04/27 · 日本における石炭火力発電所からの 排出増加による疾病負担 シャノン・コプリッツ1,3、ダニエル・ジェイコブ1、ラウリ・ミルヴィエルタ2、](https://static.fdocuments.nl/doc/165x107/5f030b087e708231d40740d4/japan-press-conference-jp-khpptxec-20170427-oecccce.jpg)

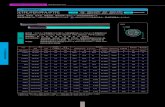
![4000chigasakischool.com/sample/sample_4000.pdfト・テスト acid [ǽsid]〔n. adj〕 酸,酸の,すっぱい;acid rain 酸性雨 類 sour acknowledge [æknálidʒ/-nɔ l-]〔v〕(](https://static.fdocuments.nl/doc/165x107/5f09e60b7e708231d429087f/ffff-acid-sidn-adj-eioeeioeiacid-rain.jpg)










